
题目列表(包括答案和解析)
11.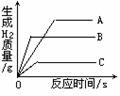 将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示。根据图中所提供的信息,得出的结论正确的是(已知:A、B、C在生成物中均为+2价) :
将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示。根据图中所提供的信息,得出的结论正确的是(已知:A、B、C在生成物中均为+2价) :
A.放出H2的质量是C>B>A
B.金属活动性顺序是A>B>C
C.反应速率最大的是A D.相对原子质量是C>B>A
10.物质的颗粒达到纳米级时,具有特殊的性质。如将单质铜制成“纳米铜”时,“纳米铜”具有非常强的化学活性,在空气中可以燃烧。下列叙述中正确的是
A.常温下,“纳米铜”与铜片的还原性相同
B.常温下,“纳米铜”比铜片更易失电子
C.常温下,“纳米铜”比铜片的金属性强
D.常温下,“纳米铜”比铜片的氧化性强
9.向一定量的Fe、FeO和Fe2O3的混合物中加入120mL 4mol·L-1的稀硝酸,恰好使混合物完全溶解,放出1.344L NO(标准状况),往所得溶液中加入KSCN溶液,无血红色出现。若用足量的氢气在加热下还原相同质量的混合物,能得到铁的物质的量为
A.0.24 mol B.0.21 mol C.0.16 mol D.0.14 mol
8.把SO2通入Fe(NO3)3溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,这时候若滴入BaCl2溶液,会产生白色沉淀,在上述一系列变化过程中,最终被还原的是
A.SO2 B. Cl- C. Fe3+ D .NO3-
7.某酸性溶液中只有Na+、CH3COO-、H+、OH-四种离子。则下列描述正确的是
A.该溶液可能是由pH=3的CH3COOH与pH=11的NaOH溶液等体积混合而成
B.该溶液由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成
C.加入适量NaOH,溶液中离子浓度为c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
D.加入适量氨水,c(CH3COO- ) 一定大于c(Na+ )、c(NH4+)之和
6.重庆市天原化工厂2006年4月16日发生特大氯气泄漏和三氯化氮爆炸事故,造成多人死亡和失踪。已知三氯化氮分子结构与氨相似,下列有关说法不正确的是
A、消除储气罐上空泄漏出的高浓度氯气,可喷洒碱液
B、发生氯气泄漏时,附近人员可用浸有碳酸钠溶液的毛巾捂住鼻孔进行自我保护
C、氯气能腐蚀金属及非金属材料,这种腐蚀主要属于电化学腐蚀
D、三氯化氮分子是极性分子
10. (14分)工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2 CH3OH(g)
(14分)工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2 CH3OH(g)
(1)图1是反应时CO和CH3OH(g)的浓度随时间变化情况。从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)= __________________
(2)图2表示该反应进行过程中能量的变化。曲线________(“a” 或“b”)表示不使用催化剂时反应的能量变化,曲线_________(“a” 或“b”)表示使用催化剂后的能量变化,写出反应的热化学方程式_________________________________________________
选择适宜的催化剂,______________(填“能”或“不能”)改变该反应的反应热。
(3)该反应平衡常数K的表达式为__________________________,
温度升高,K_________(填“增大” “不变” “减小”)
(4)恒容条件下,下列措施中能使 n(CH3OH)/n(CO) 增大的方法有______________
A. 升高温度 B.充入氦气
C. 再充入1molCO和2molH2 D.使用催化剂
(5)甲醇可与氧气构成燃料电池,该电池用多孔的惰性电极浸入浓氢氧化钾溶液,写出该电池的正极反应式和总反应的离子方程式:
正极反应式____________________________________
总反应离子方程式________________________________________________
天津一中2010届高三第四次月考
9.(18分)
相对分子质量为92的某芳香烃X是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物,合成路线,反应条件略去)。其中A是一氯代物,H是一种功能高分子,链节组成为C7H5NO.
请根据所学知识与本题信息回答下列问题:
(1)写出阿司匹林分子式_______________
(2)请根据合成反应流程图
判断上述从前到后的各步的反应类型为_______________(填字母序号)
A. 加成、消去、加成、取代 B. 还原、消去、加成、水解
C. 还原、水解、加成、水解 D. 还原、水解、氯代、水解
(3)写出反应④的化学方程式___________________________________________________
(4)写出反应⑤的化学方程式__________________________________________________
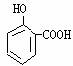 (5)已知
有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共
(5)已知
有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共
有____________种;写出其中核磁共振氢谱中有四个吸收峰的结构简式_____________
(6)请写出G的结构简式________________________
2.实验过程中,同学们发现上述装置存在以下问题,
①实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸不能顺利滴入锥形瓶。
②稀硫酸滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积
__________(填“偏高”、“偏低”或“无影响”)
③实验结束时,连接广口瓶和量筒的导管中有少量水存在,使所测氢气体积
__________(填“偏高”、“偏低”或“无影响”)
于是他们设计了下图所示的实验装置。
装置中导管a的作用是_______________________________________
1. 同学们拟选用下列实验装置完成实验:
①你认为最简易的装置其连接顺序是:
A接( ) ( )接( ) ( )接( )(填接口字母,可不填满)
②实验结束时,在读取测量实验中生成氢气的体积时,你认为合理的是:
A.待实验装置冷却后再读数
B.上下移动量筒F,使其中液面与广口瓶液面相平
C.视线与凹液面最低点水平读取量筒中水的体积
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com