
题目列表(包括答案和解析)
24、某主族元素R的单质可被稀HNO3氧化为R3+,R3+最外层有两个电子,在碱性条件下,R3+可被Cl2再氧化成带一个单位负电荷的含氧酸根离子,该阴离子在酸性条件下能将MnSO4溶液中的Mn2+氧化成高锰酸根离子,同时本身被还原成R3+。R元素与Cs元素同周期。写出R3+与Cl2反应、R的含氧酸根离子氧化MnSO4的离子方程式
(1)__________________________________________
(2)__________________________________________
标出反应(1)中电子转移的方向和总数,反应(2)可否用HCl酸化溶液__________(不可以的话要简述理由)?
23、下表是周期表的一部分
|
族 周期 |
I A |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
1 |
① |
|
|
|
|
|
|
|
2 |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
|
|
3 |
|
|
⑧ |
|
|
⑨ |
⑩ |
以下填空都要用符号表示:
(1)由表中①⑥⑩三种元素形成的离子化合物的电子式___________,据说王水中含有由表中⑥⑦⑩三种元素组成的三原子分子的物质,该分子中所有原子都达到了稳定结构,试写出此种分子的电子式_____________。
(2)周期表中同一主族元素性质相似,但我们发现主族中左上方元素与右下方元素的性质也相似,如:③和⑧。写出③的氢氧化物与强碱溶液反应的离子方程式__________________________________;②的单质在空气中燃烧可能生成的物质的化学式_______________。
(3)表中原子⑧的电子排布式为_____________,原子④核外有_____个运动状态不同的电子,原子⑤核外有_______个未成对电子。
(4)俗称“矾”的一类物质通常含有的共同元素是表中的______。一般认为能构成物质种数最多的是表中的元素⑤,但也有人认为是表中的元素___。
22、在Fe2(SO4)3溶液中,加入ag Cu,完全溶解后,又加入bg Fe,充分反应后得到cg 残余固体,且a>c,则下列判断不正确的是( )
A、最后溶液中一定不含Fe3+ B、残余固体可能是Fe、Cu的混合物
C、最后溶液中一定含Fe2+ D、残余固体一定是Cu
第Ⅱ卷(共84分)
21、标准状况下,H2S和O2的混合气体100mL经点燃反应完全后,恢复至原状态,测得气体的体积50mL,此50mL气体可能是( )
A、H2S SO2 B、H2S C、O2、SO2 D、SO2
20、下列离子方程式正确的是( )
A.硫化亚铁与稀硫酸反应制硫化氢气体:S2+ + 2H+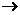 H2S
H2S
B.次氯酸钠溶液中通入过量的SO2气体:ClO- + SO2 + H2O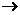 HClO + HSO
HClO + HSO
C.已知NaAlO2溶液中通少量的CO2生成Al(OH)3沉淀和Na2CO3,则NaAlO2溶
液与NaHCO3溶液混合:AlO + HCO
+ HCO + H2O
+ H2O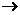 Al(OH)3
Al(OH)3 + CO
+ CO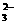
D.Ca(HCO3)2溶液与Ca(OH)2溶液混合:Ca2+ + HCO + OH-
+ OH-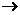 CaCO3
CaCO3 + H2O
+ H2O
19、草酸是二元弱酸,草酸氢钾溶液呈酸性。在0.1mol/L的KHC2O4溶液中,下列关系不正确的是( )
A、 c(K+)+c(H+)=c(HC2O4-)+c(OH-)+2c(C2O42-)
B、 c(C2O42-)< c(H2C2O4)
C、 c(H2C2O4)+ c(C2O42-)+ c(HC2O4-)=0.1mol/L
D、 c(H+)–c(C2O42-)= c(OH-) –c(H2C2O4)
18、下列各组反应,Q1<Q2的是( )
A、CH4(g)+2O2(g)→CO2(g)+2H2O(g)+Q1
CH4(g)+ O2(g)→CO(g)+2H2O(g)+Q2
O2(g)→CO(g)+2H2O(g)+Q2
B、S(s)+O2(g) →SO2(g)+Q1
S(g)+O2(g) →SO2(g)+Q2
C、HCl(aq)+NaOH(aq) →NaCl(aq)+H2O(l)+Q1
CH3COOH(aq)+KOH(aq) →CH3COOK(aq)+ H2O(l)+Q2
D、 CaCO3(s) →CaO(s)+CO2(g)+Q1
CaO(s)+ H2O(l) →Ca(OH)2(aq)+Q2
17、下列提纯有机物的操作正确的是( )
A、乙醇(乙酸),加入新制的生石灰后蒸馏

B、 加浓溴水后,过滤
C、CH3COOC2H5(CH3CH2OH)加适量的CH3COOH和浓H2SO4加热
D、C2H6(C2H4)混入适量的H2,加催化剂镍后充分加热
16、对于平衡体系 mA(g)+nB(g)  pC(g)+qD(g)+Q,下列说法不正确的是( )
pC(g)+qD(g)+Q,下列说法不正确的是( )
A、若温度不变,将容器扩大1倍,此时A的浓度变为原来的0.48,则m+n<p+q
B、若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n
C、若平衡体系中共有a mol气体,在其它条件不变时,再向其中加入b mol B,当重新达到平衡时,气体的总压与原平衡时的总压之比为(a+b):a,则m+n=p+q
D、温度不变时,若压强增大至原来的2倍,达到新的平衡时,总体积一定小于原体积的
15.埋在地下的铸铁输油管道,在下列各种情况下,被腐蚀最慢的是( )
A.在含铁元素较多的地壤中 B.在潮湿疏松的碱性地壤中
C.在干燥致密不透气的地壤中 D.在含碳粒较多,潮湿透气的中性地壤中
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com