
题目列表(包括答案和解析)
11、羟基扁桃酸是药物合成的重要中间体,它可由苯酚和乙醛酸反应制得。
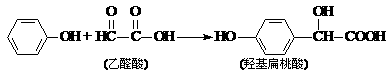
下列有关说法正确的是 学
学
A.苯酚和羟基扁桃酸互为同系物
B.常温下,1mol羟基扁桃酸只能与1mol Br2反应
C.乙醛酸的核磁共振氢谱中只有1个吸收峰
D.羟基扁桃酸分子中至少有12个原子共平面
10、已知25℃时有关弱酸的电离平衡常数:
|
弱酸化学式 |
CH3COOH |
HCN |
H2CO3 |
|
电离平衡常数(25℃) |
1.8×l0_5 |
4.9×l0_10 |
K1=4.3×l0_7 K2=5.6×l0_11 |
则下列有关说法正确的是
A.等物质的量浓度的各溶液pH关系为:pH(Na2CO3)>pH(NaCN)>pH(CH3COONa)
B.a mol·L-1 HCN溶液与b mol·L-1 NaOH溶液等体积混合,所得溶液中
c(Na+)>c(CN-),则a一定小于b
C.冰醋酸中逐滴加水,则溶液的导电性、醋酸的电离度、pH均先增大后减小
D.NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+ c(H+)=c(OH-)+ c(HCO3-) +2c(CO32-)
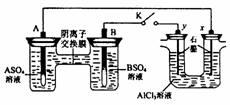
9、某同学按右图所示的装置进行实验。 A、B为两种常见金属,它们的硫酸盐可溶于水。当 K 闭合时,在交换膜处 SO42一从右向左移动。下列分析正确的是
A.溶液中(A2+)浓度减小
B.B 的电极反应: B-2eˉ==B2+
C.y 电极上有 H2 产生,发生还原反应
D.反应初期, x 电极周围出现白色胶状沉淀,不久沉淀溶解
8、某反应体系中的物质有NaOH、Au2O3,Na2S4O6,Au2O,H2O,Na2S2O3。Au2O3为反应物,则下列有关说法正确的是
A.该反应体系中有三种元素的价态发生了变化
B.Au2O在反应中作还原剂
C.Na2S2O3发生还原反应
 D.1molAu2O3发生反应,转移电子4mol
D.1molAu2O3发生反应,转移电子4mol
7、设NA为阿伏加德罗常数的值,下列说法中正确的是
A.1mol乙基中含有的电子数为17NA
B.标准状况下,22.4L三氯甲烷中共价键数目为4NA
C.1mol硫粉与足量的Cu粉共热,转移的电子数为2NA
D.6.4gCaC2晶体中含有阴阳离子总数为0.3NA
6、下列各组离子,一定能大量共存的是
A.常温下,c(H+)/c(OH-)=1×10-12的溶液:I-、Cl-、HCO3-、Na+
B.含有大量Fe3+的溶液:Na+、HCO3-、NO3-、CO32-
C.加入铝粉能产生氢气的溶液:Cl-、Na+、SO42-、NO3-
D.由水电离出的c(H+)=1×10-12 mol•L-1溶液中:K+、Cl- 、NO3- 、Na+
不定项选择题(本题包括6小题,每小题4分,共24分。每小题只有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就为0分。)
5、下列实验方法使用合理的是
A.将200g10%的盐酸加热蒸发,得到100克溶液,其浓度为20%
B.用蒸发结晶法可提纯混有少量KNO3的NaCl
C.在制备乙酸丁酯的实验中,将得到的粗产品先用水洗,再用NaOH溶液洗, 然后分液,可得到乙酸丁酯的精品
D.为了提高KMnO4溶液的氧化能力,用盐酸将其酸化
4、下列有关工业生产的叙述正确的是
A.合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率
B.硫酸工业中,在接触室安装热交换器是为了利用SO3转化为H2SO4时放出的热量
C.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室
D.电解精炼铜时,阳极溶解铜的质量比阴极析出铜的质量小
3、有一无色溶液,可能含有K+、A13+、Mg2+、NH4+、Cl-、SO42-、HCO3-、MnO4-中的几种。为确定其成分,做如下实验:①取部分溶液,加入适量Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生。下列推断正确的是
A.肯定有A13+、Mg2+、NH4+、Cl- B.肯定有A13+、Mg2+、SO42-
C.肯定有K+、HCO3-、MnO4- D.肯定有A13+、Mg2+、HCO3-
2、下列化学用语或模型表示正确的是
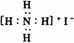
 A.HCl的电子式
A.HCl的电子式
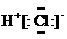 B.CO2分子比例模型
B.CO2分子比例模型
C.NH4I的电子式 D.HCN的电子式 
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com