
题目列表(包括答案和解析)
18.(12分)某研究性学习小组用如上图所示的装置进行Na2O2和H2O反应的实验。
(1)可以验证有氧气生成的实验方法是:
。
(2)将导管q放入水中,反应过程中导管口有气泡冒出,说明: 。
(3)往试管中加水至固体完全溶解且不再有气泡生成后,取出试管,往试管中滴入实验室常用无色指示剂试液A,可观察到溶液变红,后红色褪去,则该指示剂为 。
小组同学经查阅资料后得知红色褪去的原因有二:一是NaOH溶液的浓度过大;二是反应过程中可生成H2O2,H2O2氧化漂白了酚酞试液。为了排除前者因素影响,可采取的方法是: 。
(4)为进一步探究H2O2是否能够氧化指示剂试液,某同学向3mL30% H2O2的溶液中滴入2滴品红指示剂,充分振荡并放置约3min,溶液红色无明显改变。后加入少量0.5mol/LNaOH的溶液后,可看到产生许多小气泡,且溶液红色可迅速褪去。该现象表明: ,产生气泡的反应方程式为 。
17.(1)下列操作会导致实验值较实际值(或要求值)偏低(或偏小)的是__________ (填代号)。
A.测定硫酸铜晶体中结晶水含量时,将加热后的坩埚(内盛药品)置于干燥器中冷却后再称量
B.中和热测定实验中以环形铁丝搅拌棒代替环形玻璃搅拌棒
C.酸碱中和滴定实验中,将待测NaOH溶液装于碱式滴定管,标准HCl溶液盛于锥形瓶(以酚酞作指示剂),进行滴定
D.配制100 mL2 mol/L的NaCl溶液,以胶头滴管加水定容时,液面稍超出容量瓶刻度线,反复摇匀后,凹液面最低点恰好与刻度线平齐
(2)(6分)乙二酸(HOOC-COOH)俗称草酸,常见的草酸晶体是含有两分子结晶水的无色晶体(H2C2O4·2H2O)。现有某同学欲加热草酸晶体制取CO。
(1)写出反应的方程式: ;
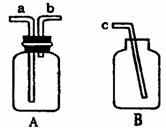
(2)该同学拟用如下图如示的仪器A、B和胶管组成装置收集CO气体(①仪器A已经气密性检查;②装置可以重复使用)
则该收集装置的连接顺序为(用a、b、c表示): ,
此外,完成CO气体收集除水外还需要 试剂。
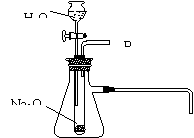
16.500ml KNO3和Cu(NO3)2 的混合溶液中C(NO3-)=6.0mol·L-1 ,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L气体(标况下),假定电解后溶液体积仍为500mL,下列说法正确的是
A.原混合溶液中C(K+)为2mol·L-1
B.上述电解过程中共转移4mol电子
C.电解得到的Cu的物质的量为0.5mol
D.电解后溶液中C(H+)为2mol·L-1
第Ⅱ卷(非选择题 共86分)
15.下列各溶液中,微粒的物质的量浓度关系正确的是:
A.10mL 0.5mol/L CH3COONa溶液与6mL 1mol/L盐酸混合:
c(Cl-)>c(Na+)>c(OH-)>c(H+)
B.c(NH4+)相等的(NH4)2SO4溶液,(NH4)2CO3溶液和NH4Cl溶液:
c[(NH4)2SO4]<c[(NH4)2CO3]<c(NH4Cl)
C.0.1mol/L pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-)
D.在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-)
14.在下列指定条件下,各组离子能够大量共存的是
A、某无色溶液中:K+、Na+、Cl-、ClO-
B、中性溶液中:Fe3+、Na+、SO42-、CO32-
C 、PH=10的溶液中:K+、Na+、S2-、NO3-
D、由水电离出的c(H+)=10-13mol/L的溶液中:NH4+、Na+、Cl-、SO32
13.下列离子方程式正确的是
A.Fe(OH)3溶于过量的氢碘酸中: Fe(OH)3+3H+=Fe3++3H2O
 B.过量SO2通入次氯酸钙溶液中:Ca2+ + 2ClO- + SO2 + H2O
==CaSO3↓+ 2HClO
B.过量SO2通入次氯酸钙溶液中:Ca2+ + 2ClO- + SO2 + H2O
==CaSO3↓+ 2HClO
C.铁作电极电解饱和食盐水:2Cl-+ 2H2O 2OH-+ H2 ↑+ Cl2↑
D.向过量苏打溶液中逐滴加入少量稀硫酸:CO32- + H+ ==HCO3-
12.下列对生产、生活有关化学问题的分析正确的是
A.液氯罐中的液氯泄漏时,可将其移入水塘中,并向水塘中加入生石灰
B.铝合金的大量使用归功于人们能用焦炭等还原剂从氧化铝中获取铝
C.“百炼成钢”的化学含义是使用氧化剂提高生铁中碳的含量
D.医疗上进行胃部造影前,患者服用的“钡餐”是BaCO3等不溶于水的物质
10.用NA表示阿伏加德罗常数的值,下列说法中正确的是
A.6.8 g熔融的KHSO4中含有0.1NA个阳离子
B.如果5.6LN2含有n个氮分子,则NA一定约为4n
C.在SiO2晶体中,若含有1mol Si原子,则Si-O键数为4NA
D.用含有0.1molFeCl3的饱和溶液制得的氢氧化铁胶体中,胶粒数等于0.1NA
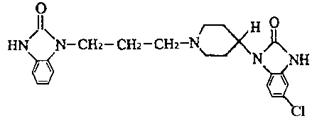 11.吗丁啉是一种常见的胃药,其有效成分的结构简式可用下图表示。关于该物质的下列说
11.吗丁啉是一种常见的胃药,其有效成分的结构简式可用下图表示。关于该物质的下列说
法不正确的是 ( )
A.该物质的分子式为C22H25ClN5O2 B.该物质具有碱性,能与酸反应
C.该物质不能发生水解反应 D.该物质能发生取代反应和加成反应
9.短周期元素A、B、C,原子序数依次递增。已知:A、C同主族,而且三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最外层电子数的一半。下列叙述正确的是
A.原子半径:A<B<C
B.2.32g四氧化三铁与足量的B完全反应转移0.09mol电子
C.常温下B的硫酸盐溶液pH<7
D.等质量B单质分别与足量A、C单质反应时前者反应放出的热量多
8.在硫酸的工业制法中,下列生产操作及说明生产操作的主要原因二者都正确的是
A.从沸腾炉出来的炉气须净化,因为炉气中SO2会与杂质发生反应
B.硫铁矿燃烧前需要粉碎,否则块状的硫铁矿石不能燃烧
C.SO3用98.3%的浓H2SO4吸收,目的是防止形成酸雾,以便使SO3吸收完全
D.SO2氧化为SO3时需使用催化剂,这样可以提高SO2的转化率
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com