
题目列表(包括答案和解析)
5.3×10-5 mol·L-1,向浓度均为0.1 mol·L-1的MgCl2和CaCl2混合溶液中逐滴加入0.1 mol·L-1 的Na2CO3溶液,首先生成CaCO3沉淀
B.向硫酸亚铁溶液中加入氯水,再加入KSCN溶液,溶液变为红色,说明硫酸亚铁溶液中存在Fe3+
C.向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成,该溶液中一定含有SO42-
D.除去Cu粉中混有的CuO,可将混合物加入到稀硝酸中,充分反应后过滤、洗涤
10.下列叙述正确的是
A.25 ℃时,MgCO3饱和溶液中c(Mg2+)=2.6×10-3 mol·L-1,CaCO3饱和溶液中c(Ca2+)=
8.主族元素W、X、Y、Z位于同一周期,原子序数依次增大,W、X是金属元素,Y、Z是非金属元素。W、X的最高价氧化物对应的水化物可以相互反应, W与Y 可形成化合物W2Y,Y的最外层电子数是核外电子层数的2倍。下列说法正确的是
A.Y的气态氢化物比Z的气态氢化物稳定
B.W的最高价氧化物对应的水化物是最强的碱
C.Y单质和氧气、氢气都能发生化合反应,且产物都具有还原性
D.W、X、Y、Z四种元素的原子半径由小到大的顺序是:W<X<Y<Z
|
|




|
|
|
|

7.石墨烯是碳原子构成的单层二维蜂窝状晶格结构(如右图所示)的一种碳质新材料,是构建富勒烯、纳米碳管的基本单元,有广泛的用途。下列说法正确的是
 A.石墨烯是一种有机物
A.石墨烯是一种有机物
B.石墨烯中碳原子间以共价键结合
C.石墨烯具有和乙烯相同的性质
D.12 g石墨烯中约含6.02×1023个e-
6.下列说法正确的是
A.多数合金的熔点比各成分金属的高
B.陶瓷、塑料、橡胶是常说的三大合成材料
C.油脂是重要的体内能源,是人体不可缺少的营养物质
D.以NaClO为有效成分的漂白液不能作游泳池和环境的消毒剂
2010. 5
可能用到的相对原子质量
H 1 C 12 N 14 O 16 Na 23 Cl 35.5 Fe 56 Cu 64 Zn 65
30.(16分)下图中A、B、C、D、E、F、G、H均为有机化合物。
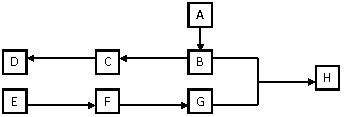
回答下列问题:
(1)链状有机化合物A的相对分子质量介于60到70间,A能发生银镜反应,1molA在催化剂作用下能与3 mol H2反应生成B,则A的结构简式是_______________________ ;
(2)B在浓硫酸中加热可生成C,C在催化剂作用下可聚合生成高分子化合物D,由C生成D的化学方程式是________________________________________________________;
(3)①芳香化合物E的分子式是C8H8Cl2。E的苯环上的一溴取代物只有一种,则E的所有可能的结构简式共有______________种 ;
②E在NaOH溶液中可转变为F,F用酸性高锰酸钾溶液氧化生成G(C8H6O4)。1 mol G与足量的 NaHCO3溶液反应可放出 44.8 L CO2(标准状况),由此确定E的结构简式是______________________ ;G的名称是_______________________________________ ;
(4)1 mol G 和足量的B在浓硫酸催化下加热反应可生成H,则由G和B生成H的化学方程式是_____________________________________________________________________,该反应的反应类型是______________________。
29.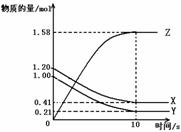 (12分)I.在温度为500K,2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:
(12分)I.在温度为500K,2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:
(1)反应的化学方程式为 ;
(2)反应开始到10s,用X表示的该段时间的反应速率为 ;(保留3位有效数字)
(3)达平衡后再升高温度,测知X的转化率增大,则该反应的ΔH
0(填“<”、“>”或“=” )
II.如果在相同的温度(500K)和固定的压强下进行上述反应:
(1)若开始时放入3.60 molX和3.00 mol Y,达平衡后,生成Z的物质的量是 mol;
(2)若开始时放入a molX,b mol Y和1.00 molZ,到达平衡后, Z的物质的量分数
与(1)中Z的物质的量分数相同,则a、b应满足的关系是 ;
若b = 1.50 mol,则a = mol.
28. (16分)纯碱、烧碱等是重要的化工原料。
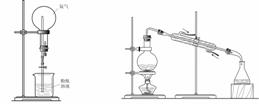
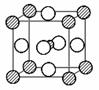
⑴利用如图所示装置可间接证明二氧化碳与烧碱溶液发生了反应。将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是 ;
若其它操作不变,将A与C连接,可观察到的现象是 。
⑵向100mL 2mol/L的NaOH溶液中通入一定量CO2,低温结晶,得到9.3g白色固体,该白色因体的组成是 (写化学式)。请你设计实验确定该白色固体存在的阴离子,试完成下列方案:
|
实验操作 |
实验现象 |
结论 |
|
①取少量白色固体于试管中,加适量水溶解,再加足量BaC12溶液 |
|
|
|
②过滤,取2mL滤液于试管中 |
 |
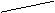 |
|
③ |
|
|
27.(16分) X、Y、Z、Q、R五种元素原子序数依次增大,且X和Y,Z和Q分别同周期,Q、R同主族且相邻,X的低价氧化物与Y单质分子的电子总数相等,Z和Q的核电荷数相差4,Q的2价简单离子与Ar原子的电子层结构相同。根据以上信息填空:
(1)Q离子的结构示意图______________;R的元素符号为___________;
(2)Y的气态氢化物空间构型是_______________;X和Q形成的共价化合物的电子式是_________________,属于__________分子(填“极性”或“非极性”);
(3)Y的最高价氧化物对应的水化物的稀溶液与Z的单质反应时,Y被还原到最低价,该反应的化学方程式是 ;
(4)据报道,只含Z、镍(Ni)和X三种元素的晶体竟然具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该晶体的晶胞结构如图,试写出该晶体的化学式 ;
|
 (5)核电荷数比Q多1的元素T,在298K时,T的最高价氧化物为无色液体,0.25 mol该物质与一定量水混合得到T的最高价氧化物的水化物的稀溶液,并放出a kJ的热量。该反应的热化学方程式为 。
(5)核电荷数比Q多1的元素T,在298K时,T的最高价氧化物为无色液体,0.25 mol该物质与一定量水混合得到T的最高价氧化物的水化物的稀溶液,并放出a kJ的热量。该反应的热化学方程式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com