
题目列表(包括答案和解析)
13.下列除杂质的方法不可行的是( )
A.用过量氨水除去Al3+溶液中的少量Fe3+
B.将混合气体通过灼热的铜网除去N2中的少量O2
C.用新制的生石灰,通过加热蒸馏,以除去乙醇中的少量水
D.用盐酸除去AgCl中少量的Ag2CO3
12.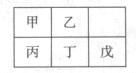 短周期金属元素甲~戊在元素周期表中的相对位置如右表所示,下
短周期金属元素甲~戊在元素周期表中的相对位置如右表所示,下
面判断正确的是
A.原子半径: 丙<丁<戊
B.金属性:甲>丙
C.氢氧化物碱性:丙>丁>戊
D.最外层电子数:甲>乙
11.在下列各溶液中,离子一定能大量共存的是
A)强碱性溶液中: K+、Al3+、Cl-、SO42-
B)在由水电离产生的H+浓度为1×10-13mol·L-1的溶液中,Na+、K+、Cl-、HCO3-
C)含有0.1 mol·L-1Ca2+溶液在中: Na+、K+、CO32-、Cl-
D)室温下,pH=1的溶液中: Na+、Fe3+、NO3-、SO42-
10.下列分离物质的方法中,根据微粒大小进行分离的是:①分液 ②过滤 ③分馏 ④重结晶 ⑤渗析
A)①③⑤ B)②④ C)①② D)②⑤
9.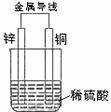 关于如图所示装置的叙述,正确的是( )
关于如图所示装置的叙述,正确的是( )
A、铜是阳极,铜片上有气泡产生
B、溶液中阴离子向正极移动
C、电流从锌片经导线流向铜片
D、氢离子在铜片表面被还原
8.下列推断正确的是
A.SiO2 是酸性氧化物,能与NaOH溶液反应
B.Na2O、Na2O2组成元素相同,与 CO2反应产物也相同
C.CO、NO、 NO2都是大气污染气体,在空气中都能稳定存在
D.新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色
7.已知还原性Cl-<Fe2+<H2O2<I-<SO2,判断下列反应不能发生的是
A)2Fe3++SO2+2H2O=SO42-+4H++2Fe2+ B)I2+SO2+2H2O=H2SO4+2HI
C)H2O2+2H++SO42-=SO2+O2+2H2O D)2Fe3++2I-=2Fe2++I2
6.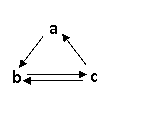 下表所列各组物质中,物质之间通过一步反应就能实现如右图所示转化的是
下表所列各组物质中,物质之间通过一步反应就能实现如右图所示转化的是
|
|
a |
b |
c |
|
A) |
Al |
AlCl3 |
Al(OH)3 |
|
B) |
HNO3 |
NO |
NO2 |
|
C) |
Si |
SiO2 |
H2SiO3 |
|
D) |
CH2=CH2 |
CH3CH2OH |
CH3CHO |
5.下列离子方程式正确的是
A)向盐酸中滴加氨水:H+ + OH- = H2O
B)Fe(OH)3溶于氢碘酸:Fe(OH)3 + 3H+ = Fe3+ + 3H2O
C.Cu2+溶液中滴加过量的氨水: Cu2+ +2NH3·H2O = Cu(OH)2↓+ 2NH4+
D.稀释氯化钴溶液,溶液颜色由蓝色逐渐变为粉红色:
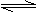 [CoCl4]2- + 6H2O
[Co(H2O)6]2++ 4Cl-
[CoCl4]2- + 6H2O
[Co(H2O)6]2++ 4Cl-
3.下列有关物质结构的表述正确的是
 A.次氯酸的电子式
A.次氯酸的电子式 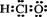 B.二氧化硅的分子式 SiO2
B.二氧化硅的分子式 SiO2
C. 碳-12原子 126C D.钠离子的结构示意图
4下列说法错误的是
A. 食醋用氢氧化钠溶液滴定开始时,溶液的PH通常变化缓慢,当接近完全反应时(即
滴定终点),PH出现突变,称为滴定突跃。
B. 硝酸钾饱和溶液冷却未出现结晶时,可以用玻棒充分磨擦器皿壁促使晶体析出。
C. 甲烷的标准燃烧热为△H=-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1
D 应用盖斯定律,可计算某些难以直接测定的反应焓变
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com