
题目列表(包括答案和解析)
1.“碳捕捉和储存(CCS)技术”是指通过碳捕捉技术,将工业和有关能源产业所产生的二氧化碳分离出来再利用。当前,二氧化碳及其产品的开发、应用是很多科学家致力研究的课题。下列有关说法不正确的是 ( )
A.对捕捉到的二氧化碳进行净化,然后用于制造干冰
B.以捕捉到的二氧化碳为原料,用来制备甲醇等产品
C.用捕捉到的二氧化碳与海藻发生光合作用,可提高海藻产量
D.人类应将大气中的二氧化碳全部捕捉,以防产生温室效应
33、(8分)1) I2 + 5Cl2 + 6H2O = 2HIO3 + 10HCl
2) KI,I2; 3) 橙色,HBrO3 >Cl2 >HIO3
4)10.58 L。
32、(10分)(1)b;(2)取C中少量溶液加入足量的稀盐酸,再加入少量BaCl2溶液,若产生白色沉淀,则Na2SO3 已有被氧化。
(3)HCO3- + Cl2 = CO2↑ + Cl- + HClO。
(4)Cl2有毒,缺少氯气的尾气吸收装置(氢氧化钠溶液)。
(5)35. 75%
31、(4分)5.6g,0.2mol。
30、(8分)(1)13.6 mL (2)①③⑤⑦; 胶头滴管。 (3)搅拌(加速稀释);引流。(4) “偏低”,“偏低”, “不影响”
29、(8分)
(1)m/M ;(2)(m/M)*2*NA;(3)(m/M)*22.4
(4)m/(1000+m)*100%。
28、(6分)

27、(4分)NO,3Cu + 8H+ + 2NO3- = 3Cu2+ + 2NO↑ + 4H2O
33、(8分)向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。
完成下列填空:
1)写出并配平CCl4层由紫色变成无色的化学反应方程式(如果系数是1,不用填写):

2)整个过程中的还原剂是 。
3)把KI换成KBr,则CCl4层变为_ _色:继续滴加氯水,CCl4层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是 。
4)加碘盐中含碘量为20mg-50mg/kg。制取加碘盐(含KIO3的食盐)1000kg,若用Kl与Cl2反应制KIO3,至少需要消耗Cl2 L(标准状况,保留2位小数)。
2010年杭西高高三化学开学考答案
选择题:
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
|
C |
B |
C |
B |
B |
C |
C |
C |
D |
D |
A |
D |
D |
|
14 |
15 |
16 |
17 |
18 |
19 |
20 |
21 |
22 |
23 |
24 |
25 |
26 |
|
A |
D |
B |
A |
A |
B |
D |
C |
A |
A |
D |
A |
A |
32、(10分)某研究性学习小组查阅资料得知,漂白粉与硫酸反应可以制得氯气,化学方程式为:Ca(ClO)2+CaCl2+2H2SO4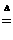 2CaSO4+2Cl2↑+2H2O 。他们设计了如下制取氯气并验证其性质的实验。
2CaSO4+2Cl2↑+2H2O 。他们设计了如下制取氯气并验证其性质的实验。
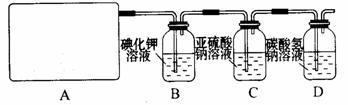
试回答:
(1)该实验中A部分的装置是 (填写装置的序号)。
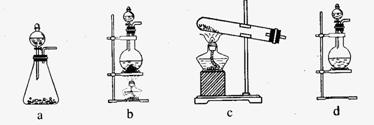
(2)请你设计一个实验,证明洗气瓶C中的Na2SO3已经被氧化(简述实验步骤):
。
(3)写出D装置中发生反应的离子方程式 。
(4)该实验存在明显的缺陷,请你提出改进的方法 。
(5)该小组又进行了如下实验:称取漂白粉2.0 g ,研磨后溶解,配制成250 ml 溶液,取25 ml 加入到锥形瓶中,再加入过量的KI溶液和过量的H2SO4溶液,静置。待完全反应后,用0.1 mol/L的Na2S2O3溶液作标准溶液滴定反应生成的碘,已知反应式为:
2Na2S2O3 + I2 = Na2S4O6 + 2NaI
反应完成时,共用去Na2S2O3 20.0 ml。则该漂白粉中Ca(ClO)2的质量分数为:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com