
题目列表(包括答案和解析)
3.在含有FeCl3和BaCl2的酸性溶液中,通入足量的SO2后有白色沉淀生成,过滤后,向溶液中滴加KSCN溶液,无明显现象,下列叙述正确的是 ( )
A.白色沉淀是BaSO4和BaSO3 B.溶液的酸性减弱
C.白色沉淀是BaSO3 D.FeCl3全部被还原为FeCl2
2、物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度有关。下列各组物质:①Cu与HNO3溶液 ②Cu与FeCl3溶液 ③Zn与H2SO4溶液 ④Fe与HCl溶液 由于浓度不同而能发生不同氧化还原反应的是
A.①③ B.③④ C.①② D.①③④
1.下列叙述正确的是 ( )
A.在氧化还原反应中,肯定有一种元素被氧化,另一种元素被还原
B.有单质参加或生成的反应一定属于氧化还原反应
C.失电子难的原子,获得电子的能力一定强
D.元素由化合态变成游离态时,它可能被氧化,也可能被还原
20、(12分)
(1)连接好装置,关闭分液漏斗活塞,将导气管插入盛水的烧杯中,用酒精灯微热烧瓶, 导气管中有气泡产生,停止微热后导管中形成一段水柱,则气密性好. (2分)
(2)浓硝酸(1分)
(3)防止倒吸,(1分) 有害气体能被完全吸收 (1分)
(4)①坩埚钳、干燥器、玻璃棒(写出药匙、研钵不算错) (2分)
②再次加热冷却称量,直到连续两次称量的质量差不超过0.lg (2分)
③4 (1分)
④偏高,(1分) a (1分)
19、(14分)
(1) (2分)
(2分)
(2)水解反应 酯化反应 (每个1分共2分)
(3)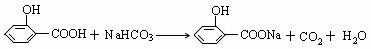 (2分)
(2分)
(4)3mol (2分)
(5)
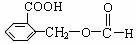
 (每个2分共6分)
(每个2分共6分)
18、(12分)
(1) 负(1分); 4OH--4e-=2H2O + O2↑(2分)
(2)5.6 L (2分)
(3)2CuSO4+2H2O 2Cu+O2↑+2H2SO4(2分)
2Cu+O2↑+2H2SO4(2分)
(4)能,因为CuSO4溶液已转变为H2SO4溶液,反应变为电解水的反应(3分)
(5)向丙烧杯中加4.5g水(2分)
17、(14分)
(1)3Fe3++3H2O=Fe(OH)3(胶体)+3H+ (2分) ①②④ (2分,选一个不得分,选两个得1分,选3个得2分)
(2)A:Fe ; B:FeS; H:H2SO4(稀) (各1分共3分)
(3)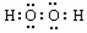 (1分)
(1分)
2Fe2++2H2O2+2H+=2Fe3++2H2O (2分)
(4)取少量E于试管中,用胶头滴管滴入NaOH溶液,加热试管可观察到试管口处湿润的红色石蕊试纸变蓝。(或其他合理答案)(2分)
(5)4Fe2++4 Na2O2+6H2O=4 Fe(OH)3↓+O2↑+8Na+(2分)
20、(12分) 硫酸铜是一种应用极其广泛的化工原料.某课外兴趣小组将适量浓硝酸分多次加到铜粉与稀硫酸的混合物中,加热使之反应完全(装置如图I、图Ⅱ所示),通过蒸发、结晶得到硫酸铜晶体,并同时测定硫酸铜晶体中结晶水的含量.
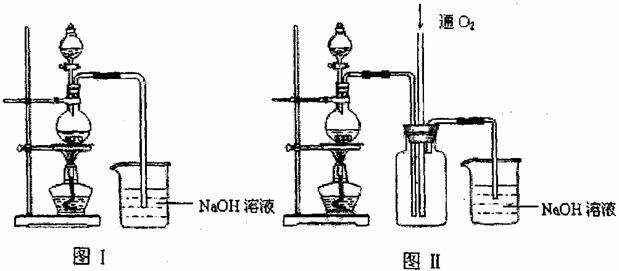
(1)怎样检查图I装置的气密性 。
(2)图I中分液漏斗内装的液体是 。
(3)图Ⅱ是图Ⅰ的改进装置,与图I相比,图Ⅱ装置的明显优点是 ,
, ,(可不答满).
(4)课外兴趣小组同学在测定胆矾(CuSO4·χH2O)晶体中结晶水的含量时.测得有关数据如下表:
|
加热前质量 |
加热后质量 |
|
|
m1(容器) |
m2(容器+晶体) |
m3(容器+无水CuSO4) |
|
5.4g |
7.9g |
6.8g |
①为完成测定,图Ⅲ中还缺少的仪器名称是 。

②判断样品已恒重的方法是 。
③测定所得胆矾(CuSO4·χH2O)中结晶水含量的实验中,称量操作至少进行 次。
④课外兴趣小组的测定结果x值(与CuSO4·5H2O相比) (填“偏高”、“偏低”、“不变”),可能的原因是 。(填字母序号)
a.加热温度过高
b.胆矾晶体的颗粒较大
c.加热后放在空气中冷却
d.胆矾晶体部分风化
万州二中高2011级高三秋季入学考试理科化学答卷
19、(14分)有机物A可发生如下转化:
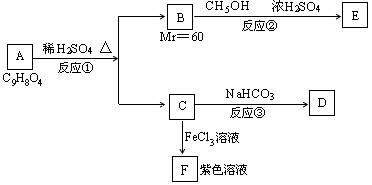
(1)化合物A是一种邻位二取代苯,其中一个取代基是羧基,则A的结构简式是_____。
(2)反应①②都可属于取代反应。其中①是__________反应,②是________反应
(3)反应③的化学方程式是 _______________________________。
(4)A与NaOH溶液共热,可发生反应生成B与C的钠盐。与1mol A反应所消耗的NaOH物质的量为_________mol。
(5)与A具有相同官能团(-COOH和-COO-)的A的同分异构体很多,请写出其中三种邻位二取代苯的结构简式____________、________________、_______________________。
18、(12分)A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
|
阳离子 |
Na+、K+、Cu2+ |
|
阴离子 |
SO42- 、OH- |
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极。
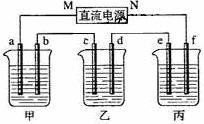
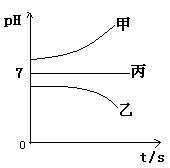
接通电源,经过一段时间后,测得乙中c电极质量增加了16g。常温下各烧杯中溶液的pH与电解时间t的关系图如上。据此回答下列问题:
(1)M为电源的 极(填写“正”或“负”)电极b上发生的电极反应为 ;
(2)计算电极e上生成的气体在标准状态下的体积: ;
(3)写出乙烧杯的电解池反应
(4)如果电解过程中B溶液中的金属离子全部析出,此时电解能否继续进行,为什么?
(5)若经过一段时间后,测得乙中c电极质量增加了16g,要使丙恢复到原来的状态,操作是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com