
题目列表(包括答案和解析)
13. KClO3和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为





 KClO3+ HCl(浓)= KCl+ ClO2↑+
Cl2↑+ H2O
KClO3+ HCl(浓)= KCl+ ClO2↑+
Cl2↑+ H2O
(1)请配平上述化学方程式(计量数填入框内)
(2)浓盐酸在反应中显示出来的性质是___________(填编号)
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)产生0.1mol Cl2,则转移的电子的物质的量为________mol。
12. 将一定量的Fe和Fe2O3的混合物投入250mL、1.8mol/L的HNO3溶液中,当固体混合物完全溶解后,在标准状况下生成1.12LNO(HNO3的还原产物仅此一种),再向反应后的溶液中加入1.0mol/LNaOH溶液,若要使铁元素完全沉淀下来,所加入的NaOH溶液体积最少应为
A.300mL B.400mL C.450mL D.500mL
11.5.12克铜和一定质量的硝酸反应,当铜消耗完时,共收集到标准状况下的气体3.36升,若把装有这些气体的集气瓶倒立在盛水的水槽中,需通入多少升标准状况下的氧气才能使集气瓶充满溶液。
A 0.336升 B 0.224升 C 0.896升 D 1.12升
10.在浓盐酸中H3AsO3与SnCl2反应的离子方程式为:3SnCl2+12Cl-+2H3AsO3+6H+=2As+3SnCl62-+6M 关于该反应的说法中正确的组合是
① 氧化剂是H3AsO3 ② 还原性:Cl->As;③ 每生成1molAs,反应中转移电子的物质的量为3mol;④ M为OH-;⑤ SnCl62-是氧化产物。
A.①③⑤ B.①②④⑤ C.①②③④ D.只有①③
9.已知Cu2S与一定浓度的HNO3可发生以下反应: 3Cu2S+26HNO3=3CuSO4+3Cu(NO3)2+15NO2↑+5 NO↑+13H2O 下列说法正确的是( )
A、Cu2S既是还原剂,又是氧化剂 B、3mol Cu2S发生反应,有24mol电子转移
C、产物中只有CuSO4是氧化产物 D、参加反应的HNO3中有10/13氧化剂
8.锑(Sb)在自然界一般以硫化物的形式存在,我国锑的蕴藏量占世界第一。从硫化物中提取单质锑一般是先在高温下将硫化物转化为氧化物,再用碳还原:
2Sb2S3+3O2+6Fe=Sb4O6+6FeS ……………………①
Sb4O6+6C=4Sb+6CO ………………………………②
关于反应①、反应②的说法正确的是
A. 反应①②中的氧化剂分别是Sb2S3、Sb4O6
B.反应①中每生成3 mol FeS时,共转移6 mol电子
C.反应②说明高温下Sb的还原性比C强
D.每生成4 mol Sb时,反应①与反应②中还原剂的物质的量之比为4︰3
7.金属钛(Ti)性能优越,被称为继铁、铝制后的“第三金属”。工业上以金红石为原料制取Ti的反应为:aTiO2 + bCl2 + cC 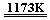 aTiCl4 + cCO
……反应①
aTiCl4 + cCO
……反应①
TiCl4 +2Mg 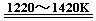 Ti + 2MgCl2 ……反应②
Ti + 2MgCl2 ……反应②
关于反应①、②的分析不正确的是
① TiCl4在反应①中是还原产物,在反应②中是氧化剂;② C、Mg在反应中均为还原剂,被还原;③ 在反应①、②中Mg的还原性大于C,C的还原性大于TiCl4;④ a=1,b=c=2;⑤ 每生成19.6 g Ti,反应①、②中共转移4.8 mol e-。 (Ti 相对原子质量49)
A.①②④ B.②③④ C.③④ D.②⑤
6.氢化铵(NH4H)与氯化铵的结构相似,又如NH4H与水反应有氢气生成,下列叙述正确的是 ( )
A.NH4H是共价化合物
B.NH4H溶于水所形成的溶液显酸性
C.NH4H与水反应时,NH4H是氧化剂
D.NH4H固体投入少量水中,有两种气体生成
5.实验室用Na2SO3还原MnO4-,如果还原含有2.4×10-3 mol MnO4-的溶液时,消耗30 mL0.2 mol•L-1的Na2SO3溶液,则Mn元素在还原产物中化合价为 ( )
A.+1 B.+2 C.+4 D.+5
4.有下列三个反应:①C12+FeI2 = FeC12+I2 ②2Fe2++Br2 = 2Fe3++2Br-
③Co2O3+6HC1 = 2CoC12 + Cl2↑+3H2O,下列说法正确的是( )
A.①②③中氧化产物分别是FeC12、Fe3+、C12
B.根据以上方程式可以得到氧化性C12>Co2O3>Fe3+
C.在反应③中生成1molCl2时,有2molHC1被氧化
D.根据反应①②一定可以推理得到C12+FeBr2 = FeC12+Br2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com