
题目列表(包括答案和解析)
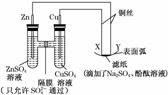
8.金属镍有广泛应用。粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知氧化性Fe2+<Ni2+<Cu2+)
A.阳极发生还原反应,其主要电极反应式:Ni2++2e-===Ni
B.电解过程中,阳极质量的减少与阴极质量的增加不相等
C.电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+
D.电解后,电解槽底部的阳极泥中含有Cu和Pt
7.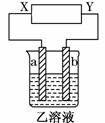 如图所示,X、Y分别是直流电源的两极,通电后发生a极板质量增加,b极板处有无色无臭气体放出.符合这一情况的是
如图所示,X、Y分别是直流电源的两极,通电后发生a极板质量增加,b极板处有无色无臭气体放出.符合这一情况的是
|
|
a极板 |
b极板 |
X电极 |
Z溶液 |
|
A |
锌 |
石墨 |
负极 |
CuSO4 |
|
B |
石墨 |
石墨 |
负极 |
NaOH |
|
C |
银 |
铁 |
正极 |
AgNO3 |
|
D |
铜 |
石墨 |
负极 |
Cu(NO3)2 |
6.某溶液中含有两种溶质NaCl与H2SO4,它们的物质的量之比为3∶1.用石墨作电极电解该混合溶液时,根据电极产物,可明显分为三个阶段.下列叙述不正确的是
A.阴极自始至终只有H2 B.阳极先析出Cl2后析出O2
C.电解最后阶段为电解水 D.溶液pH不断增大,最后为7
5. 市场上经常见到的标记为Liion的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料。这里锂离子电池的电池反应式为:
市场上经常见到的标记为Liion的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料。这里锂离子电池的电池反应式为:
Li+2Li0.35NiO2 2Li0.85NiO2
下列说法不正确的是
A.放电时,负极的电极反应式:Li-e-===Li+
B.充电时,Li0.85NiO2既发生氧化反应又发生还原反应
C.该电池不能用水溶液作为电解质
D.放电过程中Li+向负极移动
4.2006年,科学家们发明了一种能够给电子设备提供动力的生物燃料电池。该电池包括两
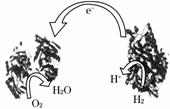 个涂覆着酶的电极,它们处于充满空气和少量氢气的玻璃槽中。由于气体可以混合从而省
个涂覆着酶的电极,它们处于充满空气和少量氢气的玻璃槽中。由于气体可以混合从而省
去了昂贵的燃料隔离膜,其工作原理如图所示。下列说法
正确的是
A.左边为该电池的负极
B.该电池可在高温环境下使用
C.该电池负极反应为:H2-2e-===2H+
D.该电池正极反应为O2+4e-===2O2-
3.茫茫黑夜中,航标灯为航海员指明了方向,航标灯的电源必须长效、稳定。我国科技工作者研制出以铝合金、Pt-Fe合金网为电极材料的海水电池。在这种电池中
①铝合金是阳极 ②铝合金是负极
③海水是电解液 ④铝合金电极发生还原反应
A.②③ B.②④ C.①② D.①④
2.已知热化学方程式:2SO2(g)+O2(g) 2SO3(g) ΔH=-Q kJ·mol-1(Q>0)。下列说法
2SO3(g) ΔH=-Q kJ·mol-1(Q>0)。下列说法
正确的是
A.相同条件下,2 mol SO2(g)和1 mol O2(g)所具有的能量小于2 mol SO3(g)所具有的能量
B.将2 mol SO2(g)和1 mol O2(g)置于一密闭容器中充分反应后,放出热量为Q kJ
C.增大压强或升高温度,该平衡都向逆反应方向移动
D.如将一定量的SO2(g)和O2(g)置于某密闭容器中充分反应后放热Q kJ,则此过程中有2 mol SO2(g)被氧化
1.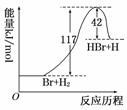 参照反应Br+H2―→HBr+H的能量对反应历程的示意图,下列叙
参照反应Br+H2―→HBr+H的能量对反应历程的示意图,下列叙
述中正确的是
A.正反应为吸热反应
B.正反应为放热反应
C.加入催化剂,该化学反应的反应热增大
D.从图中可看出,该反应的反应热与反应途径有关
29.(物质结构与性质)(8分)已知A、B、C、D、E、F都是短周期的元素,它们的原子序数依次递增。A原子的电子层数与它的核外电子总数相同,而B原子的最外层电子数是次外层的2倍,C的氢化物可使湿润的红色石蕊试纸变蓝,B和D可以形成两种气态化合物,E原子核外电子总数比B的2倍少1,F在本周期元素中原子半径最小。则:
(1)A、B、C、D、E、F的名称分别是 。
(2)在A至F中任选元素,写出一种含极性键的非极性分子的分子式 ,写出一种含非极性键的离子化合物的电子式 。
(3)由B和D组成,且B和D的质量比为3∶8的化合物的结构式是 ,
该化合物分子中B原子的杂化方式为
(4)E和F形成的化合物为 晶体 。
29.(有机化学)(8分)300多年前,著名化学家波义耳发现了铁盐与没食子酸的显色反应,并由此发明了蓝黑墨水。没食子酸的结构式为:
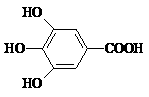
(1)用没食子酸制造墨水主要利用了___________________类化合物的性质(填代号)。
A、醇 B、酚 C、油脂 D、羧酸
(2)没食子酸丙酯且有抗氧化作用,是目前广泛应用的食品添加剂,其结构简式为________________________________________________。
(3)尼泊金酯是对羟基苯甲酸与醇形成的酯类化合物,是国家允许使用的食品防腐剂。尼泊金丁酯的分子式为_________________________,其苯环只与-OH和-COOR两类取代基直接相连的同分异构体有___________种。
(4)写出尼泊金乙酯与氢氧化钠溶液加热反应的化学方程式:
__________________________________________________ ___________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com