
题目列表(包括答案和解析)
7.氢化铵(NH4H)与氯化铵的结构相似,又如NH4H与水反应有氢气生成,下列叙述正确的( )
A.NH4H是共价化合物 B.NH4H溶于水所形成的溶液显酸性
C.NH4H与水反应时,NH4H是氧化剂 D.NH4H固体投入少量水中,有两种气体生成
6.实验室用Na2SO3还原MnO4-,如果还原含有2.4×10-3 mol MnO4-的溶液时,消耗30 mL0.2 mol•L-1的Na2SO3溶液,则Mn元素在还原产物中化合价为 ( )
A.+1 B.+2 C.+4 D.+5
5.下列关于Li、Na、K、Rb、Cs的叙述均正确的一组是 ( )
①金属性最强的是铯 ②氧化性最强的是锂原子 ③在自然界中均以化合态形式存在 ④密度按Li-Cs 顺序呈依次递增趋势 ⑤铯与水反应十分剧烈,甚至会发生爆炸 ⑥它们的氧化物都只有M20和M202两种形式 ⑦粒子半径:Rb+>K+>Na+,Cs>Cs+>K+, K>Na>Li
A.①②③④ B.④⑤⑥⑦ C.②⑥ D.①③⑤⑦
4.有下列三个反应:①C12+FeI2 = FeC12+I2 ②2Fe2++Br2 = 2Fe3++2Br-
③Co2O3+6HC1 = 2CoC12 + Cl2↑+3H2O,下列说法正确的是 ( )
A.①②③中氧化产物分别是FeC12、Fe3+、C12
B.根据以上方程式可以得到氧化性C12>Co2O3>Fe3+
C.在反应③中生成1molCl2时,有2molHC1被氧化
D.根据反应①②一定可以推理得到C12+FeBr2 = FeC12+Br2
3.在含有FeCl3和BaCl2的酸性溶液中,通入足量的SO2后有白色沉淀生成,过滤后,向溶液中滴加KSCN溶液,无明显现象,下列叙述正确的是 ( )
A.白色沉淀是BaSO4和BaSO3 B.溶液的酸性减弱
C.白色沉淀是BaSO3 D.FeCl3全部被还原为FeCl2
2.下列各项中的“黄色”,不属于因化学反应而产生的现象的是 ( )
A.无色试剂瓶中的浓硝酸呈黄色 B.蛋白质遇到浓硝酸颜色变黄
C.久置的碘化钾溶液呈黄色 D.食盐在无色的火焰上灼烧时,火焰呈黄色
1.下列叙述正确的是 ( ) A.在氧化还原反应中,肯定有一种元素被氧化,另一种元素被还原
B.有单质参加或生成的反应一定属于氧化还原反应
C.失电子难的原子,获得电子的能力一定强
D.元素由化合态变成游离态时,它可能被氧化,也可能被还原
24.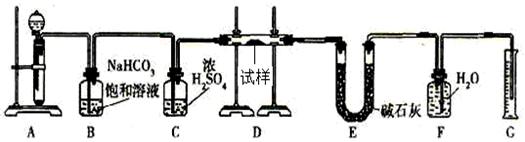 (12分)现有一定量含有Na2O杂质的Na2O2试样,用下图的实验装置测定Na2O2试样的纯度。(可供选用的反应物只有CaCO3固体、6mol/L盐酸、6mol/L硫酸和蒸馏水)
(12分)现有一定量含有Na2O杂质的Na2O2试样,用下图的实验装置测定Na2O2试样的纯度。(可供选用的反应物只有CaCO3固体、6mol/L盐酸、6mol/L硫酸和蒸馏水)
回答下列问题:
(1)实验前必须检查装置的气密性。仪器连接好后,在__________中加适量的水,关闭A中分液漏斗活塞后微热试管,若看到_______________________说明装置气密性好。
(2)装置A中液体试剂选用盐酸而不用硫酸,理由是___________________
____________________________________。
(3)装置B的作用是_______________________________;装置C的作用是_______________________;装置E中碱石灰的作用是__________________。
(4)装置D中发生反应的化学方程式是:_______________,_____________。
(5)若开始时测得样品的质量为2.0g,反应结束后测得气体体积为224mL(标准状况),则Na2O2试样的纯度为__________________。
23、(8分)软性隐形眼镜可由聚甲基丙烯酸羟乙酯(HEMA)制成超薄镜片,其合成路线可以是:
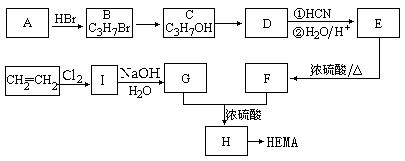
已知:① 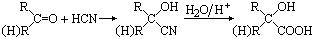
② CH3COOCH2CH2OH的名称为乙酸羟乙酯。
试写出:
(1)A、E的结构简式分别为:A 、E 。
(2)写出下列反应的反应类型:C→D ,E→F 。
(3)写出下列转化的化学方程式:
I→G ;
G+F→H 。
www.k@s@5@ 高#考#资#源#网
22.(10分)市场销售的某种食用精制盐包装袋上有如下说明:
|
产品标准 |
GB5461 |
|
产品等级 |
一级 |
|
配 料 |
食盐、碘酸钾、抗结剂 |
|
碘含量(以I计) |
20-50 mg/kg |
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处)
KIO3+ KI+ H2SO4= K2SO4+ I2+ H2O
(2)上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
①Na2SO3稀溶液与I2反应的离子方程式是 。
②某学生设计回收四氯化碳的操作步骤为:
a.将碘的四氯化碳溶液置于分液漏斗中;
b.加入适量Na2SO3稀溶液;
c.分离出下层液体。
以上设计中遗漏的操作及在上述步骤中的位置是 ;所缺步骤为 。
(3)已知:I2+2S2O32-=2I-+S4O62-。某学生测定食用精制盐的碘含量,其步骤为:
a. 准确称取12.7g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为6.0×10-4mol·L-1的Na2S2O3溶液20.0mL,恰好反应完全。
①判断c中反应恰好完全依据的现象是 。
②根据以上实验和包装袋说明,所测精制盐的碘含量是 mg/kg
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com