
题目列表(包括答案和解析)
17.某种混合气体,可能含有N2、HCl、CO, 把混合气体依次通过足量的NaHCO3溶液和灼热CuO,气体体积都没有变化;再通过足量Na2O2固体,气体体积缩小。最后通过灼热的铜网,经充分反应后气体体积又减小,但还有剩余气体。以下对混合气体组成的判断,正确的是( )
A. 一定没有N2;CO和HCl中至少有一种 B. 一定有N2、CO和HCl
C. 一定有N2;CO和HCl中至少有一种 D. 一定有N2和HCl;没有CO
16.对下列各种溶液中所含离子的判断合理的是
A.向无色溶液中加氯水变橙色,溶液中可能含:SO42-、Br-、OH-,Ba2+
B.使紫色石蕊试液变红色的溶液中可能含:K+,Na+,Ba2+,HCO3-
C.某溶液,加铝粉有氢气放出,则溶液中可能含:K+,Na+、H+,NO3-
D.在c(H+)=10-14mol/L的溶液中可能含:Na+,AlO2-,CO32-,SO32-
15.在密闭容器中充入CO2、CO、CH4的混合气体共mg,若加入足量的Na2O2,充分振荡并不断用电火花引燃至反应完全,测得固体质量增加mg;则CO2与CH4的体积比为
A.3:1 B.2:l C.1:1 D.缺少条件,无法计算
14.已知:H2O (g) = H2O (l);△H = Q1 kJ/mol C2H5OH (g) = C2H5OH (l);△H = Q2 kJ/mol
C2H5OH (g) + 3O2 (g) =2CO2 (g) + 3H2O (g) ;△H = Q3 kJ/mol
若使23g 酒精液体完全燃烧,最后恢复到室温,则放出热量为
A.Q1+ Q2 +Q3 B.0.5(Q1 + Q2 +Q3)
C.0.5Q1 -1.5Q2 + 0.5Q3 D.1.5Q1 -0.5Q2 + 0.5Q3
13、下列反应的离子方程式正确的是
①硫酸铜溶液与氢氧化钡溶液反应: Ba2++ SO42_= BaSO4↓
②将金属钠加入水中 2Na + 2H2O = 2Na+ + 2OH - + H2 ↑
③石灰石溶于醋酸CaCO3+2CH3COOH=2CH3COO-+ Ca2++CO2↑+H2O
④氟气与水反应: F2+H2O=H+ +F -+ HFO
⑤小苏打溶液中加入少量的石灰水:Ca2+ +2OH-+2HCO3-=CaCO3↓+CO32- +2H2O
⑥次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO- + CO2 + H2O =CaCO3↓+ 2HClO
⑦钠与硫酸铜溶液反应:Cu2++2Na =2Na+ +Cu
⑧氯气与水反应Cl2 + H2O = 2H+ + Cl - + ClO-
⑨纯碱溶液中滴加少量盐酸CO32- + H+ = HCO3-
A.①②⑤⑨ B.②③⑤⑨ C ④⑤⑥⑦ D.②③⑧⑨
12.NA为阿伏加德罗常数,下列说法正确的是 ( )
A.标准状况下,11.2L三氧化硫所含有的原子数目为2NA
B.分解H2O2制O2,每生成1 mol O2转移2NA个电子
C.62 g Na2O溶于水后所得溶液中含有O2-数为NA
D.常温常压下,1 g H2含有中子数目为NA
11.下列说法或表示正确的是 ( )
A.将等质量硫蒸气和硫粉分别完全燃烧,前者放出热量多
B.由“C(石墨) C(金刚石);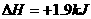 ·mol-1可知金刚石比石墨稳定
·mol-1可知金刚石比石墨稳定
C.稀的强酸和稀的强碱溶液反应的热化学方程式均为:
H++OH- H2O(1);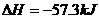 ·mol-1
·mol-1
D.在25℃、101 kPa时,1克氢气完全燃烧生成H2O放出热量142.9kJ。则:
2H2O(1) 2H2(g)+O2(g);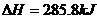 ·mol-1
·mol-1
10.金属钛(Ti)性能优越,被称为继铁、铝制后的“第三金属”。工业上以金红石为原料制取T的反应为①aTiO2 + bCl2 + cC  aTiCl4 + cCO ,② TiCl4 +2Mg
aTiCl4 + cCO ,② TiCl4 +2Mg 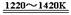 Ti + 2MgCl2
Ti + 2MgCl2
关于反应①、②的分析不正确的是
① TiCl4在反应①中是还原产物,在反应②中是氧化剂;② C、Mg在反应中均为还原剂,被还原;③ 在反应①、②中Mg的还原性大于C,C的还原性大于TiCl4;④ a=1,b=c=2;⑤ 每生成19.6 g Ti,反应①、②中共转移4.8 mol e-。 (Ti 相对原子质量49)
A.①②④ B.②③④ C.③④ D.②⑤
9. 等质量的Na2CO3、NaHCO3与足量盐酸作用,符合下列情况的是
A. Na2CO3比NaHCO3反应速率快 B. 相同条件下Na2CO3产生的CO2体积大
C. NaHCO3比Na2CO3反应剧烈 D. 两者放出CO2的体积一样
8.下列物质属于电解质的是
①硫酸 ②甲酸 ③蔗糖 ④ Cu ⑤ NH3 ⑥ CaCO3 ⑦ 熔化的KCl ⑧KCl溶液
A.① ② ⑤ ⑥ ⑦ B.① ⑥ ⑦ C.除③ ④ 外都是 D.以上答案均错误
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com