
题目列表(包括答案和解析)
20.(18分)A、B、C、D是短周期元素所形成的单质,也是中学化学中常见的物质,通常情况下,A、B为固体,C、D为气体,电解H的水溶液生成X、C和D,此反应是一个重要的化工反应,这些物质间相互转化关系如下图所示。试回答:
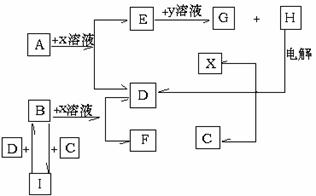 ⑴H的化学式为
;
⑴H的化学式为
;
⑵B单质为 晶体(填晶体类型)。
⑶X的电子式为 , F水溶液显性 (填:酸性、中性或碱性)。
⑷E和G化合物的水溶液混合发生反应,其离子方程式为:
⑸用惰性电极电解含0.2molH物质的水溶液,在阳极产生0.2mol气体时,此时溶液的体积为200ml。则溶液的pH= 。
19.(18分)有一瓶澄清的溶液,其中可能含有NH4+、K+、Na+、Ba2+、Al3+、Fe3+、Cl-、I-、
NO3-、CO32-、SO42-、MnO4-,取该溶液进行以下实验:
(1)取pH试纸检验,溶液呈强酸性。
(2)取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡后CCl4层呈紫红色。
(3)另取出部分溶液逐渐加入NaOH溶液,使溶液从酸性逐渐变为碱性,在滴加过程中和滴加完毕后,溶液均无沉淀产生。
(4)取出部分上述碱性溶液加Na2CO3溶液后,有白色沉淀生成。
(5)将(3)得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
①根据上述实验事实确定:
该溶液中肯定存在的离子是 ,
肯定不存在的离子是 ,
还不能确定是否存在的离子是
②请写出(2)(4)步骤中发生的离子方程式:
步骤(2)
步骤(4)
18.(6分)磷在氧气中燃烧,可能生成两种固态氧化物。3.1g的单质磷(P)在3.2g的氧气中燃烧,至反应物耗尽,并放出X KJ热量。
⑴通过计算确定反应产物的组成(用化学式表示)是 。
⑵已知单质磷的燃烧热为Y KJ/mol,则1mol P与O2反应生成固态P2O3的热化学反应方程式:__ _
_ 。
17.(10分)A、B、C三只烧杯中,依次分别盛有NaOH溶液、KSCN溶液、煮沸的蒸馏水,各滴入FeCl3溶液,试根据实验现象分别回答以下问题:
⑴分别写出三只烧杯中形成分散系的名称:
A , B ,C 。
⑵写出B中形成分散系的离子方程式 。
⑶写出C中形成分散系的化学方程式 。
16.在铁和铜的混和物中,加入一定量的稀硝酸,使之充分反应,剩余金属m1 g,再向其中加入一定量的稀硫酸,充分振荡后,剩余金属m2 g,则m1与m2关系是
A.m1一定大于m2 B.m1可能大于m2
C.m1可能等于m2 D.m1一定等于m2
第Ⅱ卷 (非选择题共52分) 高-考*资/源+网
15.将15 mL 2 mol·L-1Na2CO3溶液逐滴加入到40 mL 0.5 mol·L-1MCln盐溶液中,恰好将溶液中的Mn+离子完全沉淀为碳酸盐,则MCln中n值是
A.4 B.3 C.2 D.1
14.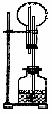 在如图所示的装置中,烧瓶中盛有空气,广口瓶中盛放下列物质时可发生喷
在如图所示的装置中,烧瓶中盛有空气,广口瓶中盛放下列物质时可发生喷
泉的选项是
A.块状大理石和稀硫酸
B.NH4Cl与稀NaOH溶液
C.Na2O2与NaOH溶液
D.铜片与稀盐酸
13.物质的量之比为2∶5的锌与稀硝酸反应,若硝酸被还原的产物为N2O,反应结束后锌没有剩余,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是
A.1∶4 B.1∶5 C.2∶3 D.2∶5
12.镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd
+ 2NiOOH + 2H2O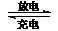 Cd(OH)2 + 2Ni(OH)2
Cd(OH)2 + 2Ni(OH)2
有关该电池的说法正确的是
A、充电时阳极反应:Ni(OH)2 -e- + OH- ﹦ NiOOH + H2O
B、充电过程是化学能转化为电能的过程
C、放电时负极附近溶液的碱性不变
D、放电时电解质溶液中的OH-向正极移动
11.设NA为阿伏加德罗常数,下列叙述正确的是
A.24 g镁的原子最外层电子数为NA B.1 L 0.1 mol·L-1乙酸溶液中H+数为0.1NA
C.1 mol甲烷分子所含质子数为10NA D.标准状况下,22.4 L乙醇的分子数为NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com