
题目列表(包括答案和解析)
6、浓度不等的两种硫酸溶液等质量混合后,溶液的质量分数为a%,而等体积混合后,溶液的质量分数为b%;浓度不等的两种氨水等质量混合后,其质量分数为a%,而等体积混合后,溶液的质量分数为c%,那么a、b、c数值的关系是
A.a>b>c B.b>a>c C.c>b>a D.c>a>b
5、下列物质的溶液中通入过量的CO2,有沉淀的是 ( )
A.CaCl2 B.NaAlO2 C.Ca(ClO)2 D.C6H5ONa
4、 (NH4)2PtCl6晶体受热分解,生成氮气、氯化氢、氯化铵和金属铂,在此分解反应中,氧化产物与还原产物的物质的量之比是 A.2:3 B.3:2 C.4:3 D.1:3
3、.2010年8月8日我国甘肃舟曲发生特大泥石流灾害,卫生防疫人员要紧急配制0.01 mol/L的KMnO4 消毒液,下列操作导致所配溶液浓度偏高的是
A.取KMnO4样品时不慎在表面沾了点蒸馏水
B.溶解搅拌时有液体飞溅
C.定容时俯视容量瓶刻度线
D.摇匀后见液面下降,再加水至刻度线
2、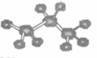 下列化学用语使用正确的是 ( )
下列化学用语使用正确的是 ( )

A.NH4H的电子式: B.丙烷分子的比例模型
C.次氯酸的结构式:H-O-Cl D.二氧化硅的分子式:SiO2
1、下列叙述中正确的是 A、凡是强电解质在离子方程式中都要以离子的形式来表示 B、离子反应一定使溶液中所有离子的浓度都发生变化 C、复分解反应必须具备离子反应的某个条件 D、酸碱中和反应都能用离子方程式:H+ + OH- =H2O表示
24、重铬酸铵 [(NH4)2Cr2O7]是一种橘黄色的晶体,常用于石油精炼、制革、印染、烟火、陶瓷等行业,是一种重要的化工原料。
(1)已知在酸性条件下,重铬酸盐有强氧化性。向冷的酸性重铬酸铵溶液中通入H2S,
可得到Cr3+和S,写出反应的离子方程式:
。
(2)在150℃时,重铬酸铵迅速呈膨胀式分解,发生如下主要反应:
(NH4)2Cr2O7=Cr2O3+4H2O+N2↑,
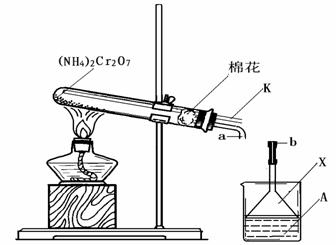
但同时也发生副反应。某同学设计了如下装置,探究副反应的生成物:
①装置中棉花的作用是 ;加热前,该同学先通过导管K向试管中通一会N2,其目的
是 ;
②连接a、b,关闭导管K,加热使反应发生。若装置A中所盛溶液为酚酞溶液,且
溶液变红,说明有 产生,仪器X的作用是 ;若装置A中所盛溶液为新制的硫酸亚铁溶液,且出现棕红色的沉淀,说明副反应中
有 产生,写出产生该沉淀的
离子方程式
25.
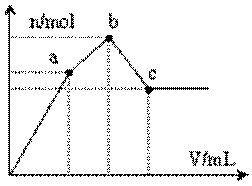
取来两份等浓度的NaOH溶液A和B,每份10ml,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,
试回答下列问题:
(1)原NaOH溶液的物质的量浓度为 _______________mol/L
(2)曲线A表明,原NaOH溶液中通入CO2后,所得溶液中的溶质为(写
化学式)___________________;其物质的量之比为_____________。
(3)曲线B表明,原NaOH溶液中通入CO2后,所得溶液加盐酸产生CO2气体体
积(标准状况)的最大值为________________ml。

21、向100mL 3mol·L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴加入1mol·L-1Ba(OH)2溶液。(1)写出当刚好出现沉淀物质的量总量的最大值时的离子方程式(用一个式子表示):
_____ 。
(2)随着Ba(OH)2溶液体积的变化,沉淀总物质的量的变化如下图所示(Y代表沉淀总物质的量/mol;X代表Ba(OH)2溶液体积/mL)。写出B点和C点所对应的Ba(OH)2溶液的体积:b_____________ mL ,c_____________ mL。
 Y
Y
X
X
22.(1)请将5种物质:N2O、FeCl2、Fe(NO3)3、HNO3和FeCl3分别填入下面对应的横线上,组成一个未配平的化学方程式。
_________+__________→__________+__________+__________+H2O
(2)反应物中发生氧化反应的物质__________,被还原的元素是_________。
(3)反应中1 mol氧化剂_______(填“得到”或“失去”)___________ mol电子。
(4)请将反应物的化学式及配平后的系数填入下列相应的位置中.
__________+ __________
21.有一种白色粉末,含有下列阴离子和阳离子中的几种:阴离子:S2-、Cl-、NO3-、SO42-、CO32-、HCO3- 、MnO4-,阳离子:Na+、Mg2+、Al3+、Ba2+、Fe2+、Fe3+、Cu2+、NH4+,将该白色粉末进行下列实验,观察到的现象如下:
|
实验操作 |
现象 |
|
a.取少量粉末,加水、振荡 |
全部溶解、溶液无色透明 |
|
b.向所得溶液中慢慢滴入苛性钠并加热 |
无明显现象 |
|
c.取少量粉末,加盐酸 |
无明显现象 |
|
d.取少量粉末,加稀HCl和稀BaCl2混合液 |
有白色沉淀生成 |
根据实验推断(多填不得分)
根据实验推断(多填不得分)
(1)从a实验中,可推断粉末中,不可能有 离子;
(2)从b实验中,可推断粉末中,不可能有 离子;
(3)从c实验中,可推断粉末中,不可能有 离子;
(4)从d实验中,可推断粉末中,不可能有 离子;
(5)综上所述,粉末中肯定含 离子;还可能含有 离子。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com