
题目列表(包括答案和解析)
8.已知A+B=C+D为放热反应,对该反应的下列说法正确的是
A.A的能量一定高于C B.反应中A与B的总能量一定高于C与D的总能量
C.B的能量一定高于D D.因该反应是放热反应,故不加热该反应就能反应
7.根据以下四个反应:(1)H2S+I2=2H++2I-+S¯ (2)H2SO3+2H2S=3S¯+3H2O
(3)2I-+Br2=2Br-+I2 (4)H2SO3+I2+H2O=H2SO4+2HI
确定Br-、I-、H2S和H2SO3还原性由强到弱的顺序是
A.H2S>H2SO3>I->Br- B.Br->I->H2SO3>H2S
C.H2SO3>H2S>Br->I- D.I->Br->H2S>H2SO3
6.观察下列几个装置示意图,有关叙述正确的是
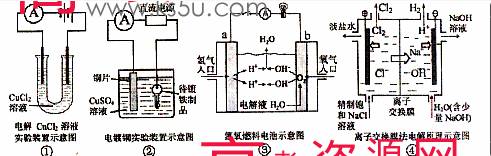
A.装置①中阳极上析出红色固体
B.装置②的待镀铁制品应与电源正极相连
C.装置③中闭合电键后外电路电子由a极流向b极
D.装置④的离子交换膜允许阳离子、阴离子、水分子自由通过
18. Ⅰ.(18分) 氮元素是构成生物体的最主要元素之一,在动植物生命活动中起着重要作用。下图是自然界中氮循环以及有机物在生物体内代谢的部分过程示意图,请分析回答:
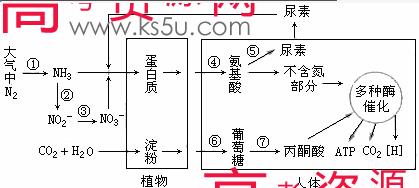
(1) 微生物在氮循环中有重要作用,例如根瘤菌能参与图中[ ] 过程。根瘤菌与大豆的关系在生物学上称为 。
(2) 土壤中能完成②③过程的生物不多,这种生物属于生态系统中的 。
(3) 中耕松土是农业中的一个重要手段,疏松土壤能促进图中的 过程(填序号)同时还能抑制 作用,从而有利于增加并保持土壤的肥力。当土壤中氮元素含量增加时,作物的光合作用效率会提高,其原因是:氮是光合作用的各种酶及 、 的组成成分。
(4) 人体中的 (激素)和 (激素)能促进⑦的进行,从而保证内环境的动态平衡。
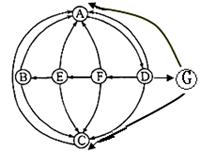 Ⅱ.(10分) 下图是生态系统中碳循环示意图,图中箭头表示碳流动方向,根据示意图回答:
Ⅱ.(10分) 下图是生态系统中碳循环示意图,图中箭头表示碳流动方向,根据示意图回答:
(1) 构成该生态系统中群落的有_____________________ (填字母),图中最长的一条食物链是___________(用字母和箭头表示)。
(2) 该生态系统中生物群落与无机环境间联系的纽带是______________(填字母),土壤中的纤维素分解菌属于图中的成分 (填字母)。
(3) 该生态系统中有一鼠群,黑毛鼠占80%,白毛鼠占20%,在下列环境中生活两年后,下列哪一项最能显示黑毛鼠和白毛鼠百分率的变化?( )
|
选项 |
黑暗丛林 |
光亮沙地 |
||
|
黑毛鼠 |
白毛鼠 |
黑毛鼠 |
白毛鼠 |
|
|
A B C D |
90% 70% 90% 70% |
10% 30% 10% 30% |
70% 90% 90% 70% |
30% 10% 10% 30% |
西南师大附中高2011级第一次月考
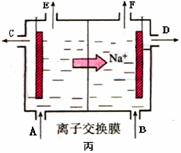
17. (16分) 下图中甲、乙、丙的电极材料都是石墨和铁,其中丙是氯碱工业生产示意图。
(1) 若甲、乙两烧杯均盛放CuSO4溶液,
①甲中铁棒上的电极反应式为_______________________________________。
②乙装置工作一段时间后,向烧杯中加入适量的碱式碳酸铜[Cu2(OH)2CO3],能使溶液恢复到起始状态,请写出这段时间内乙装置发生的所有反应的化学方程式
________________________________________________________________________。
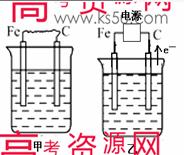
(2) 若甲、乙两烧杯均盛放饱和NaCl溶液,
①甲中石墨棒上的电极反应式为___________________。
②将湿润的淀粉碘化钾试纸放在乙烧杯______(填“Fe”或“C”)电极的上方,发现试纸先变蓝后褪色,这是因为过量的Cl2氧化了生成的I2。若反应物Cl2和I2的物质的量之比为5∶1,且生成两种酸,则其对应的化学方程式为_________________________。
③假设产生的气体全部逸出溶液,当乙反应有0.01 mol电子转移后停止实验,此时烧杯中溶液的体积为100 mL,则溶液混合均匀后的pH = ____________。
④当乙中的反应用于工业生产时,为了阻止两极产物之间的反应,通常使用如丙图所示的装置,其中离子交换膜只允许Na+通过,Na+的移动方向如图中标注,则H2的出口是________(填代号)。
16. (18分) 根据以下有机物之间的转化关系框图,回答问题:

(1) 已知:B、C的分子结构中均带有支链,B的结构简式为__________,C在浓硫酸加热条件下只能得到一种结构的烯烃D,C的结构简式可能为___________或___________,D的高名称为(用系统命名法命名)_________________。
(2) F中含有的官能团的名称为____________________。
(3) ③和⑥的反应类型分别是_____________、___________。
(4) H能与H2在催化剂加热条件下1:1反应生成K,写出满足下列条件的K的所有同分异构体的结构简式:a.能发生银镜反应,b.属于酯类
___________________________________________.
(5) 分别写出反应④⑦⑧和⑨的化学方程式:
④_____________________________________________________;
⑦_____________________________________________________;
⑧_____________________________________________________;
⑨_____________________________________________________。
15.
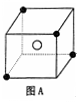 (12分) Ⅰ.某离子晶体特征结构如图A所示。X●位于立方体部分顶点,Y○位于立方体中心。试分析:
(12分) Ⅰ.某离子晶体特征结构如图A所示。X●位于立方体部分顶点,Y○位于立方体中心。试分析:
(1) 每个Y同时吸引着_______个X,该晶体的化学式为______________。
(2) 晶体中每个X周围与它最接近且距离相等的X共有__________个。
(3) 晶体中距离最近的2个X与1个Y形成的夹角∠XYX是___________。
(4)
设该晶体的摩尔质量为M g/mol,晶体密度为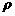 g/cm3,阿伏加德罗常数的值为NA,则晶体中两个距离最近的X中心间距为__________cm。
g/cm3,阿伏加德罗常数的值为NA,则晶体中两个距离最近的X中心间距为__________cm。
Ⅱ.B4Cl4是一种淡黄色并具有挥发性的固体化合物,在70℃以下,它存在于真空中。结构测定表明:该化合物中每个氯原子均结合一个硼原子,其键长都是0.170nm,任意两个硼原子之间为0.171 nm。每个硼原子周围各有4个共价键。根据上述性质和参数画出B4Cl4分子空间构型的示意图______________________。
14. (14分) 某些化学反应可表示为:A+B→C+D+H2O。请回答下列问题:
(1) 若A、C、D均含有氯元素,且A中氯元素的化合价介于C与D之间,则该反应的离子方程式为_________________________________。
(2) 若A为黑色固体,C是黄绿色气体,则该反应的离子方程式为__________________。
(3) 若A为第二周期的单质,B为第二周期某元素最高价氧化物的水化物,C、D均为气体,则该反应的化学方程式为____________________________________。
(4) 若C为NaCl,D是能使澄清石灰水变浑浊的无色无味的气体,则A是______或_______,B为_____________(填化学式,下同)。
(5) 若C、D均是能使澄清石灰水变浑浊的气体,则A与B的组合为_____________。
8. 将质量相等的Ag片和铂片插入硝酸银溶液(足量)中,银片与电源正极相连,铂片与电源负极相连。以电流强度1A通电10min,然后反接电源,以电流强度2A继续通电10min。下列为表示银电极的质量、铂电极的质量、电解池中产生气体的质量和电解时间的关系图,正确的是
A.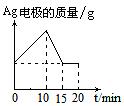 B.
B.
C.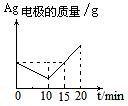 D.
D.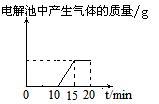
第Ⅱ卷 非选择题(共174分)
本卷共10个大题.
7. 已知反应:C2H2(g)+H2(g) C2H4(g)在降低温度时平衡向右移动,则下列两个反应:
C2H4(g)在降低温度时平衡向右移动,则下列两个反应:
C(s)+1/2H2(g) 1/2C2H2(g);ΔH=-Q1
1/2C2H2(g);ΔH=-Q1
C(s)+H2(g) 1/2C2H4(g);ΔH=-Q2 (Q1、Q2均为正值),
1/2C2H4(g);ΔH=-Q2 (Q1、Q2均为正值),
“Q值”大小比较正确的是
A.Q2>Q1 B.Q1>Q2 C.Q2=Q1 D.不能确定
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com