
题目列表(包括答案和解析)
1.下列化学名词正确的是 ( )
A.笨酚 B.乙醇 C.乙酸乙脂 D.戍烷
29.(16分)某芳香烃A,其蒸气的密度是同状态下H2密度的53倍;某烃类衍生物X,分子式为C15H14O3,能使FeCl3溶液显紫色:J分子内有两个互为对位的取代基在一定条件下有如下的转化关系:(无机物略去)
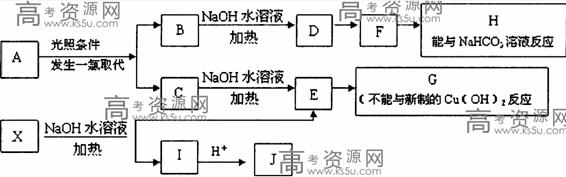
(1)属于芳香烃类的A的同分异构体中,若其苯环上的一氯代物只有一种则结构简式表示为_________。
(2)J中所含的含氧官能团的名称为________________________。
(3)E与H反应的化学方程式是______________________________________________;反应类型是__________________。
(4)B、C的混合物在NaOH乙醇溶液中加热可以生成同一种有机物I,以I为单体合成的高分子化合物的名称是__________。
(5)已知J有多种同分异构体,写出符合下列性质的J的所有同分异构体的结构简式。
①与FeCl3溶液作用显紫色;②与新制Cu(OH)2悬浊液作用产生红色沉淀;③苯环上的一卤代物有2种。.___________________,___________________,___________________
28.(16分)(1)在298K时,1molC2H6在氧气中完全燃烧生成二氧化碳和液态水,放出热量1558.3 kJ。写出该反应的热化学方程式 。若C2H6和氧气以KOH溶液组成燃料电池,其负极反应式为 。
(2) A、B、C、D、E、F六种短周期元素的原子序数依次增大。已知A、C、F三原子的最外层共有11个电子,且这种三元素的最高价氧化物的水化物之间两两皆能反应,均能生成盐和水,D元素原子的最外层电子数比次外层电子数少4个,E元素原子的次外层电子数比最外层电子数多3个。试回答: ① 写出下列元素的符号A ,D 。 ② 用电子式表示B、F形成的化合物为 。 ③ A、C两种元素最高价氧化物的水化物之间反应的离子方程式为 。 ④ D的固态氧化物是 晶体。含nmolD的氧化物的晶体中含D-O共价键为 mol。
27.(14分)下图是有关硫及其化合物的实验装置:

实验中用到的实验试剂在下列中选择:①浓硫酸;②70%硫酸;③25%硫酸;④新开封的亚硫酸钠粉末;⑤硫化亚铁;⑥氢氧化钠溶液;⑦溴水;⑧碳酸钠溶液。
在实验开始不久即在B瓶中析出固体粉末状物质。试回答:(有编号的必须填编号)
(1)A中分液漏斗盛放的试剂是 。
(2)B中反应的氧化产物和还原产物的物质的量比是 。
(3)E(启普发生器)中盛有的两种试剂是 ,发生反应的离子方程式是 。
(4)如果A、E两装置气体发生速度相同,流量也相同时,在D中反应的离子方程式是 。
(5)D的作用是 ,C的作用是 。
26.(14分)-如图所示,以石墨为电极电解A的水溶液,并做下面一系列实验。试根据实验现象完成下列问题(电解质A的水溶液焰色反应呈紫色)。
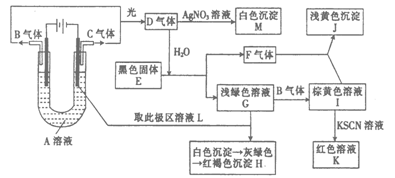
(1)A的化学式为 ,E的名称为 。
(2)I和F反应的离子方程式是 。
(3)若将电解装置中的阳极换成铁棒,则在U型管底部可观察到的现象是
,阳极的电极反应式为 ,阴极的电极反应式为 ,电解的化学方程式为 。
13.某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中P表示压强,T表示温度,n表示物质的量):
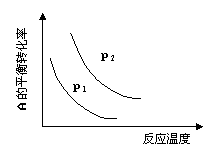
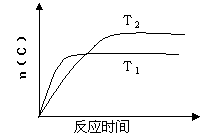
|
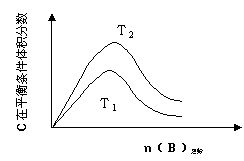
反应Ⅲ:3A(g)+B(g) 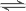 2C(g)
反应Ⅳ:A(g)+B(g)
2C(g)
反应Ⅳ:A(g)+B(g) 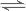 2C(g)
2C(g)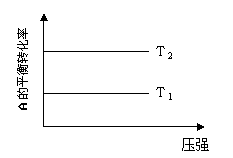
根据以上规律判断,下列结论正确的是
A.反应Ⅰ:ΔH>0,P2>P1
B.反应Ⅱ:ΔH>0,T1>T2
C.反应Ⅲ:ΔH>0,T2>T1;或ΔH<0,T1>T2
D.反应Ⅳ:ΔH<0,T2>T1
第Ⅱ卷(非选择题,共174分)
12.向体积为0.05mol·L-1CH3COOH溶液中加入体积为Vb的0.05mol·L-1KOH溶液,下列关系错误的是
A.Va>Vb时:c (CH3COOH) + c (CH3COO-)>c (K+)
B.Va=Vb时:c (CH3COOH) + c (H+)>c (OH-)
C.Va<Vb时:c (CH3COO-)>c (K+)> c (OH-)> c (H)
D.Va与Vb任意比时:c (K+)+ c (H+) =c (OH-)+ c (CH3COO-)
11.用惰性电极电解2L硝酸银溶液,当在电路中通过0.1mol电子后,调换正负极,电路中又通过了0.2mol电子,此时溶液pH值为(假设溶液体积不变)是
A.2 B.3 C.1 D.无法确定
10.一种新型燃料电池,它是用两根惰性金属做电极插入KOH溶液中,然后向两极上分别通入甲烷和氧气,发生的电极反应为: X极:CH4+10OH-―8e-=CO32-+7H2O Y极:4H2O+2O2+8e-=8OH-
关于此燃料电池的下列说法中错误的是
A.X极为负极,Y极为正极
B.工作一段时间后,KOH的物质的量不变
C.在标准状况下通入5.6LO2完全反应,则有1.0mol电子发生转移
D.该电池工作时甲烷一极附近溶液的pH降低
9.用惰性电极电解一定质量的某浓度的NaCl溶液,一段时间后停止电解,此时若加入100g 36.5%的浓盐酸,所得溶液正好与原溶液完全相同,则下列说法正确的是
A.电解过程中,两极所得到的气体,在相同的条件下体积相等
B.电解过程中,在相同的条件下,阳极所得到的气体的体积比阴极的大
C.电解过程中转移电子的物质的量约为8mol
D.原某浓度的NaCl溶液中溶有117g NaCl
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com