
题目列表(包括答案和解析)
9. 下列离子方程式正确的是 ( )
A. 向盐酸中滴加氨水:H+ + OH- = H2O
B. Fe(OH)3溶于氢碘酸:Fe(OH)3 + 3H+ = Fe2+ + 3H2O
C. 铜溶于稀硝酸:3Cu + 8H+ + 2NO3- = 3Cu2+ + 2 NO ↑+ 4H2O
 D. 向Na2SO3溶液中通入足量氯气:Na2SO3+Cl2+H2O=SO42-+2Cl-+2H++2Na+
D. 向Na2SO3溶液中通入足量氯气:Na2SO3+Cl2+H2O=SO42-+2Cl-+2H++2Na+
8. 下列物质中微粒的个数比不是1 : 1的是( )
A.NaHCO3晶体中的阴离子和阳离子
B.Na2O2固体中的阴离子和阳离子
C.重氢(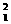 H)原子中的质子和中子
H)原子中的质子和中子
D.NH3分子中的质子和电子
7. 下列物质与其用途相符合的是( )
①Cl2-可做消毒剂 ②AgBr-制胶卷,感光纸 ③AgI-人工降雨 ④碘元素-预防甲状腺肿大 ⑤淀粉-检验I2的存在 ⑥NaClO-可漂白纺织物
A.②③④⑤⑥ B.①②③④⑤ C.②③④⑤ D.全部
6.漂白粉在空气中容易变质的原因是( )
A.CaCl2易吸收空气中的水分 B.Ca(ClO)2易与盐酸反应
C.Ca(ClO)2见光易分解 D.Ca(ClO)2易与空气中的CO2和水作用
5.下列氯化物中既能由金属和氯气直接反应制得,又能由金属和盐酸反应制得的是( )
A. CuCl2 B.FeCl2 C.AlCl3 D.FeCl3
4.2.3g纯净的金属钠在干燥的空气中被氧化后得到3.5g固体,由此可判断其氧化产物是 ( )
A.只有Na2O B.只有Na2O2 C.Na2O和Na2O2 D.无法确定
3.将CO2气体通人CaCl2溶液,若要有白色沉淀产生,可加入的试剂是( )
A.氯化钾溶液 B.碳酸氢钙溶液 C.氯水 D.氢氧化钠溶液
2.下列微粒化学性质最活泼的是 ( )
A.C12 B.Cl- C.C1 D.Na+
1.下列关于氯水的叙述,正确的是( )
A.新制氯水中只含Cl2和H2O 分子
B.新制氯水可使蓝色石蕊试纸变红且不褪色
C.光照氯水有气泡逸出,该气体是Cl2
D.氯水放置数天后pH将变小
24.土壤中有机物质含量的高低是判断土壤肥力的重要指标,通常通过测定土壤中碳的含量来换算。方法如下:
准确称量一定量的风干土样(m g),加入已知过量的K2Cr2O7酸性溶液煮沸,使土壤中的“碳”被氧化,反应的化学方程式为:2K2Cr2O7+3C+8H2SO4 ==== 2K2SO4+2Cr2(SO4)3+3CO2↑+8H2O;然后用FeSO4溶液(浓度为c mol·L-1)滴定剩余的K2Cr2O7,用去FeSO4溶液V1 mL。另取一份同量的K2Cr2O7酸性溶液,也用相同的FeSO4溶液滴定,用去V2 mL。
(1)写出FeSO4溶液和酸性K2Cr2O7溶液反应的离子方程式。
(2)若上述实验中m=2.0 g,c=0.2 mol·L-1, V1=19.50 mL,V2=42.60 mL;另知上述方法中只有96%的碳被氧化,且有机物质中碳的平均含量为58%。试计算上述土壤中有机物质的质量分数。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com