
题目列表(包括答案和解析)
5.下列实验操作中错误的是

A.用规格为10mL的量筒量取6mL的液体
B.用药匙或者纸槽把粉末状药品送入试管的底部
C.过滤时玻璃棒的末端应轻轻靠在三层的滤纸上
D.如果没有试管夹,可以临时手持试管给固体或液体加热
4、在标准状况下,下列气体所含分子个数最多的是
A、35.5 g 氯气 B、32 g 氧气 C、1120 mL 二氧化硫气体 D、280 mL 氢气
3、设NA为阿伏加德罗常数,下列说法正确的是( )
A、2.3g金属钠变为钠离子时失去电子数目为0. 2NA
2NA
B、2克氢气所含的原子数为NA
C、32g氧气所含的电子数为16NA
D、11.2L氯气所含的原子数目为N
2、下列说法正确的是
A.摩尔质量就等于物质的式量 B.摩尔质量就物质式量的6.02×1023倍
C.HNO3的摩尔质量是63g D.硫酸和磷酸的摩尔质量相等
1.下列实验仪器不宜直接用来加热的是
A.试管 B.坩埚 C.蒸发皿 D.烧杯
24.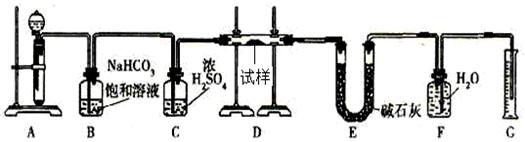 (12分)现有一定量含有Na2O杂质的Na2O2试样,用下图的实验装置测定Na2O2试样的纯度。(可供选用的反应物只有CaCO3固体、6mol/L盐酸、6mol/L硫酸和蒸馏水)
(12分)现有一定量含有Na2O杂质的Na2O2试样,用下图的实验装置测定Na2O2试样的纯度。(可供选用的反应物只有CaCO3固体、6mol/L盐酸、6mol/L硫酸和蒸馏水)
回答下列问题:
(1)实验前必须检查装置的气密性。仪器连接好后,在__________中加适量的水,关闭A中分液漏斗活塞后微热试管,若看到_______________________说明装置气密性好。
(2)装置A中液体试剂选用盐酸而不用硫酸,理由是___________________
____________________________________。
(3)装置B的作用是_______________________________;装置C的作用是_______________________;装置E中碱石灰的作用是__________________。
(4)装置D中发生反应的化学方程式是:_______________,_____________。
(5)若开始时测得样品的质量为2.0g,反应结束后测得气体体积为224mL(标准状况),则Na2O2试样的纯度为__________________。
23、(8分)软性隐形眼镜可由聚甲基丙烯酸羟乙酯(HEMA)制成超薄镜片,其合成路线可以是:
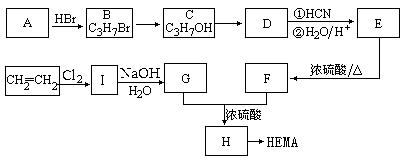
已知:① 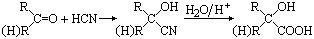
② CH3COOCH2CH2OH的名称为乙酸羟乙酯。
试写出:
(1)A、E的结构简式分别为:A 、E 。
(2)写出下列反应的反应类型:C→D ,E→F 。
(3)写出下列转化的化学方程式:
I→G ;
G+F→H 。
www.k@s@5@ 高#考#资#源#网
22.(10分)市场销售的某种食用精制盐包装袋上有如下说明:
|
产品标准 |
GB5461 |
|
产品等级 |
一级 |
|
配 料 |
食盐、碘酸钾、抗结剂 |
|
碘含量(以I计) |
20-50 mg/kg |
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处)
KIO3+ KI+ H2SO4= K2SO4+ I2+ H2O
(2)上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
①Na2SO3稀溶液与I2反应的离子方程式是 。
②某学生设计回收四氯化碳的操作步骤为:
a.将碘的四氯化碳溶液置于分液漏斗中;
b.加入适量Na2SO3稀溶液;
c.分离出下层液体。
以上设计中遗漏的操作及在上述步骤中的位置是 ;所缺步骤为 。
(3)已知:I2+2S2O32-=2I-+S4O62-。某学生测定食用精制盐的碘含量,其步骤为:
a. 准确称取12.7g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为6.0×10-4mol·L-1的Na2S2O3溶液20.0mL,恰好反应完全。
①判断c中反应恰好完全依据的现象是 。
②根据以上实验和包装袋说明,所测精制盐的碘含量是 mg/kg
21.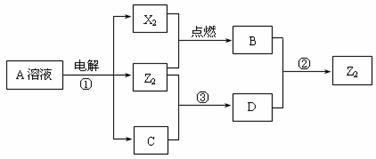 (10分)短周期元素X、Y、Z的原子序数依次增大,X和Y同主族,Y和Z同周期,Y与Z能形成离子个数比为1︰1的离子化合物A,X与Z能形成原子个数比为1︰1的共价化合物B,它们之间能实现如下图所示转化(部分产物已略去):
(10分)短周期元素X、Y、Z的原子序数依次增大,X和Y同主族,Y和Z同周期,Y与Z能形成离子个数比为1︰1的离子化合物A,X与Z能形成原子个数比为1︰1的共价化合物B,它们之间能实现如下图所示转化(部分产物已略去):
(1)Y在周期表的位置是______________________;Z2的结构式是________。
(2)反应①的离子方程式____________________________________________。
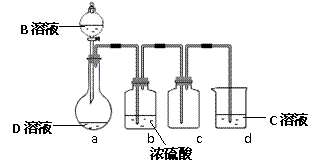 (3)D是很多漂白剂中含有的有效成分,这些产品不能与洁厕灵(含有有机酸和无机酸)一起使用,其原因就是在常温时能发生与反应②相似的反应。某校的学生在实验室利用反应②的原理来制备纯净、干燥的Z2,仪器装置如右图所示(夹持固定装置的仪器已略去)。
(3)D是很多漂白剂中含有的有效成分,这些产品不能与洁厕灵(含有有机酸和无机酸)一起使用,其原因就是在常温时能发生与反应②相似的反应。某校的学生在实验室利用反应②的原理来制备纯净、干燥的Z2,仪器装置如右图所示(夹持固定装置的仪器已略去)。
I、写出反应②的离子方程式_____________________
II、上述实验装置不够完善,改进方法是
Ⅲ、足量Z2 通入FeBr2溶液中发生反应的离子方程式是 。
www.k@s@5@ 高#考#资#源#网
20.将足量的CO2不断通入KOH、Ca(OH)2、KAlO2的混合溶液中,生成沉淀与通入CO2的量的关系可表示为 ( )

Ⅱ卷(非选择题40分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com