
题目列表(包括答案和解析)
7.在含有碳酸根离子,且能使酚酞变红的无色溶液中,能大量共存的离子组是( )
A.Na+、SO、SO、K+
B.Na+、Cu2+、Br-、Ba2+
C.K+、MnO、NO、Na+
D.K+、Ca2+、SO、Cl-
6.用下图装置测定水中氢、氧元素的质量比,其方法是分别测定通氢气前后玻璃管的质量差和U形管的质量差.李松同学通过实验得出的结论是m(H)∶m(O)>1∶8.下列对导致这一结果原因的分析中,一定不合理的是( )

A.Ⅰ、Ⅱ装置之间缺少干燥装置
B.Ⅲ装置后缺少干燥装置
C.Ⅱ装置中的CuO粉末可能不干燥
D.CuO没有全部被还原
5.配制一定物质的量浓度溶液时,会导致所配溶液浓度偏大的操作是( )
A.在用蒸馏水洗涤烧杯时,洗液未全部注入容量瓶中
B.定容摇匀后,发现液面低于刻度线,又加水到刻度
C.定容时俯视刻度线
D.用来配制溶液的容量瓶用蒸馏水洗涤后未进行干燥处理
4.在某一澄清、透明的浅黄色溶液中,可能含有下列八种离子:H+、NH、Fe3+、Ba2+、Al3+、SO、HCO、I-,在检验方案设计时初步分析其溶液中最多可含离子(不包括OH-)有( )
A.4种 B.5种 C.6种 D.7种
3.下列实验设计和结论相符的是( )
A.将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中
B.某气体能使湿润的红色石蕊试纸变蓝,该气体水溶液一定显碱性
C.某无色溶液中加Ba(NO3)2溶液,再加稀盐酸,沉淀不溶解,则原溶液中一定有SO
D.在含FeCl2杂质的FeCl3溶液中通足量Cl2后,充分加热,除去过量的Cl2,即可得到较纯净的FeCl3溶液
2.NA代表阿伏加德罗常数.下列有关叙述正确的是( )
A.标准状况下,2.24 L H2O含有的分子数等于0.1NA
B.常温下,100 mL 1 mol/L Na2CO3溶液中阴离子总数大于0.1 NA
C.分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g
D.3.4 g NH3中含N-H键数目为0.2 NA
1. 下列关于Fe(OH)3胶体的说法不正确的是( )
A.Fe(OH)3溶胶与硅酸溶胶混合将产生凝聚现象
B.Fe(OH)3胶体在电场作用下;向阳极运动
C.Fe(OH)3胶体微粒不停地作布朗运动
D.光线通过Fe(OH)3溶胶时会发生丁达尔现象
21.50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在下图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是________。
(2)大烧杯上如不盖硬纸板,求得的中和热数值将_______(填“偏大”、“偏小”或“无影响”)。
(3)实验中改用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比较,所放出的热量________(填“相等”或“不相等”),但中和热应_________(填“相等”或“不相等”),简述理由_________________________________。
20.《硫酸铜晶体里结晶水含量的测定》是中学化学中的重要实验,请回答下列该实验的相关问题。
(1)实验中能直接加热的仪器名称为____________;进行的称量操作至少为________次。
 (2)下列操作会引起测定结果偏高的是__________________
(2)下列操作会引起测定结果偏高的是__________________
A.加热时温度过高CuSO4发生分解 B.加热后在空气中冷却再称量
C.加热过程中有晶体溅出 D.晶体部分风化
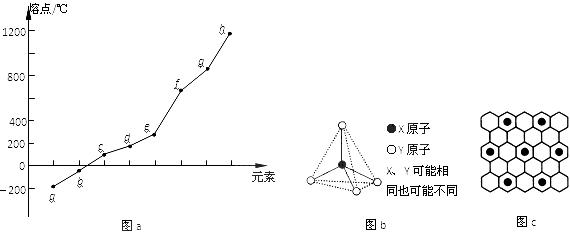 (4)碳元素的某种单质具有平面层状结构,该单质的名称为__________;同一层中的原子构成许多的正六边形,单质与熔融的钾相互作用,形成某种青铜色的物质(其中的元素钾用“●”表示),原子分布如图c所示,该物质的化学式为
。
(4)碳元素的某种单质具有平面层状结构,该单质的名称为__________;同一层中的原子构成许多的正六边形,单质与熔融的钾相互作用,形成某种青铜色的物质(其中的元素钾用“●”表示),原子分布如图c所示,该物质的化学式为
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com