
题目列表(包括答案和解析)
4.在3Cl2+8NH3=6NH4Cl+N2反应中,还原性最强的物质是( )
A. Cl2 B. NH3 C. NH4Cl D. N2
3.制备单质硅时,主要化学反应如下( )
①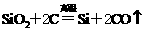
②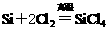
③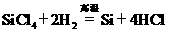
下列对上述三个反应的叙述中,不正确的是( )
A. ①③为置换反应
B. ①②③均为氧化还原反应
C. ②为化合反应
D. 三个反应的反应物中硅元素均被氧化
2.下列化合物中,只能在溶液中才能导电的电解质是( )
A.NaCl B.H2SO4 C.NH3 D.CaO
1.下列关于化学学习和研究的说法错误的是
A.化学模型有助于解释一些化学现象 B.质量守恒定律是大量试验事实的总结
C.化学家提出的假设都能被试验证明 D.化学基本原理的应用是有一定条件的
15、(1)FeSO4+HNO3→Fe2(SO4)3+Fe(NO3)3+N2O
(2)FeSO4 ,+5价N。
(3)得到 4
(4)24FeSO4 + 30HNO3
16答案:
.(1)1、5、3、3、3、3 (2分)。
(2)①I2+SO32-+H2O = 2I-+SO42 - +2H+(2分);
②在步骤b后,增加操作:将分液漏斗充分振荡后静置(1分)。
(3)①溶液由蓝色恰好变为无色(1分)。 ②20(2分)
14. (1)KHCO3 (2)2.4×1022 (3)碳(C) (4)H2O2作氧化剂,其产物是H2O;H2O没有毒性及污染性。
16、 .(8分)市场销售的某种食用精制盐包装袋上有如下说明(部分):
|
产品标准 |
 |
|
产品等级 |
一级 |
|
配料 |
食盐、碘酸钾、抗结剂 |
|
碘含量(以I计) |
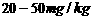 |
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处): 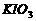 +
+
 +
+ 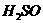 4
=
4
= 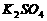 +
+
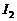 +
+ 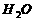
(2)上述反应生成的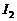 可用四氯化碳检验。向碘的四氯化碳溶液中加入
可用四氯化碳检验。向碘的四氯化碳溶液中加入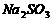 稀溶液,将
稀溶液,将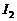 还原,以回收四氯化碳。
还原,以回收四氯化碳。
①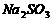 稀溶液与
稀溶液与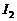 反应的离子方程式是
反应的离子方程式是
②某学生设计回收四氯化碳的操作步骤为:
a、将碘的四氯化碳溶液置于分液漏斗中; b、加入适量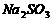 稀溶液;
稀溶液;
c、分离出下层液体。
以上设计中遗漏的操作及在上述操作中的位置是
(3)已知: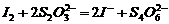
某学生测定食用精制盐的碘含量,其步骤为:
a、准确称取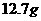 食盐,加适量蒸馏水使其完全溶解;
食盐,加适量蒸馏水使其完全溶解;
b、用稀硫酸酸化所得溶液,加入足量 溶液,使食用盐中
溶液,使食用盐中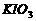 与
与 反应完全;
反应完全;
c、以淀粉溶液为指示剂,逐滴加入物质的量浓度为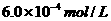 的
的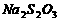 溶液
溶液 ,恰好反应完全。
,恰好反应完全。
①判断c中反应恰好完全依据的现象是
②根据以上实验和包装说明,所测精盐的碘含量是
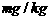
DADCB DDBDA C
13(1)2,4=2,2,1,2; (2)②; (3)0.2。
15.(1)请将5种物质:N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个未配平的化学方程式。
_________+__________→__________+__________+__________+H2O
(2)反应物中发生氧化反应的物质__________,被还原的元素是_________。
(3)反应中1 mol氧化剂_______(填“得到”或“失去”)___________ mol电子。
(4)请将反应物的化学式及配平后的系数填入下列相应的位置中,并用单线桥表示:
__________+ __________→
14. “绿色试剂”双氧水可作为矿业废液消毒剂,如要消除采矿业废液中的氰化物(如KCN),化学方程式为:KCN+H2O2+H2O=A+NH3↑
(1)生成物A的化学式为 。
(2)在标准状况下有0.448L氨气生成,则转移的电子数为 。
(3)反应中被氧化的元素为 。
(4)H2O2被称为绿色氧化剂的理由是 。
13. KClO3和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为





 KClO3+ HCl(浓)= KCl+ ClO2↑+
Cl2↑+ H2O
KClO3+ HCl(浓)= KCl+ ClO2↑+
Cl2↑+ H2O
(1)请配平上述化学方程式(计量数填入框内)
(2)浓盐酸在反应中显示出来的性质是___________(填编号)
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)产生0.1mol Cl2,则转移的电子的物质的量为________mol。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com