
题目列表(包括答案和解析)
5.设nA为阿伏加德罗常数的值,下列叙述正确的是 ( )
 A.常温常压下,16g14CH4所含中子数目为8nA
A.常温常压下,16g14CH4所含中子数目为8nA
B.标准状况下,22.4 LCCl4所含分子数目为nA
C.1 L 0.5 mol·L-1的CH3COONa溶液中所含的CH3COO-
离子数目为0.5n
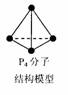
D.6.2g白磷(分子式为P4,分子结构如右图所示)所含P-
键数目为0.3nA
4.下列有关说法错误的是 ( )
A.利用铝热反应可以冶炼熔点较高的金属
B.用作“钡餐”的物质主要成分是硫酸钡
C.常温下,可以用铁制容器来盛装冷的浓硫酸
D.人造刚玉熔点很高,可用作高级耐火材料,其主要成分是二氧化硅
3.下列离子方程式式书写正确的是 ( )
A.明矾溶液中加入过量的氢氧化钡溶液:
Al3++2SO42++2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O
B.氯气溶于水:Cl2+H2O=2H++Cl-+ClO-
C.苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32-
D.硝酸亚铁溶液和稀盐酸混合:Fe2++4H++NO3-=Fe3++2H2O+NO↑
2. 下列化学用语或命名正确的是 ( )
A.Cl-的结构示意图: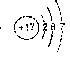 B.NH4Cl的电子式:
B.NH4Cl的电子式: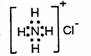
C.丙烯的实验式(最简式):CH2 D.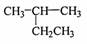 的名称:2-乙基丙烷
的名称:2-乙基丙烷
1.以节能减排为基础的低碳经济是保持社会可持续发展的战略举措。下列做法违背发展低碳经济的是 ( )
A.尽量用纯液态有机物代替水作溶剂
B.限制塑料制品的使用
C.提高原子利用率,发展绿色化学
D.发展氢能和太阳能
15、请根据下列实验数据确定某水合含Fe(II)的盐的化学式。①将0.784g该含亚铁的盐强烈加热至质量恒定,得到0.160gFe2O3;②将0.784g该盐溶于水,加入过量的BaCl2溶液,得到0.932gBaSO4;③0.392该盐溶于水,加入过量的NaOH溶液后煮沸,释放出的氨气用50.0mL 0.10 mol/L盐酸吸收后,吸收液需要30.0mL 0.10mol/LNaOH溶液恰好中和。
14、2 L容器中,分别将物质的量均为2.00 mol的SO2、O2混合,在不同温度(T) 下发生如下反应:2SO2(g)+O2(g) 2SO3(g)。并在第10 s时分别测定其中SO3的体积分数(SO3%)并绘成如图所示曲线:
下发生如下反应:2SO2(g)+O2(g) 2SO3(g)。并在第10 s时分别测定其中SO3的体积分数(SO3%)并绘成如图所示曲线:
(1)此反应的正反应为 热反应;
(2)A、B两点正反应速率的大小关系是:vA vB(填=、>或<,);以O2表示T0对应的平均反应速率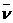 (O2)=
;
(O2)=
;
(3)温度T<T0时,SO3%逐渐增大的原因是
;
(4)若B点SO3的体积分数为40.0%,则SO2的转化率为 (保留3位有效数字);
(5)若将B点的混合气体的5%通入过量的BaCl2溶液,生成沉淀 g。(保留3位有效数字)
13、 12.0g某液态有机化合物A完全燃烧后,生成14.4gH2O和26.4g CO2。测得有机化合物A的蒸气与H2的相对密度是30,求:
12.0g某液态有机化合物A完全燃烧后,生成14.4gH2O和26.4g CO2。测得有机化合物A的蒸气与H2的相对密度是30,求:
(1)有机物A的分子式 。 (2)用如图所示装置测定有机物A的分子结构,实验数据如下(实验数据均已换算为标准状况):a mL(密度为ρ g/cm3)的有机物A与足量钠完全反应后,量筒液面读数为bmL,若1mol A分子中有x mol氢原子能跟金属钠反应,则x的计算式为 (可以不化简)
12、硫酸亚铁铵又称莫尔盐,浅绿色晶体,在空气中比一般的亚铁盐稳定,溶于水但不溶于乙醇,化学式为[(NH4)2SO4·FeSO4·6H2O],相对分子质量为392,是常用的分析试剂。在实验室,将FeSO4和(NH4)2SO4两种溶液按一定比例混合,蒸发浓缩、冷却结晶,很容易得到硫酸亚铁铵晶体。某研究性学习小组已制备得到莫尔盐,准备分析研究他们得到的产品。请你帮助完成部分项目:
(1)预测现象:向盛有莫尔盐溶液的大试管中滴加浓NaOH溶液,并不断振荡。
。
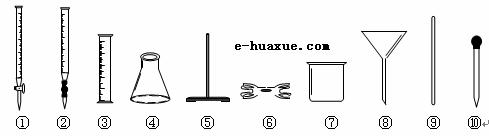
(2)为了确定产品中亚铁含量,研究小组经查阅资料后,打算用KMnO4(酸化)溶液滴定莫尔盐溶液中的Fe2+。离子方程式为:5Fe2++MnO4-+8H+=5Fe2++Mn2++4H2O。滴定时必须选用的仪器有 (从下图所列仪器中选填编号,同种仪器数量不限);滴定时是否需要加加指示剂? 。若需要,请指出加什么指示剂;若不需要,请说明理由。 。
(3)取莫尔盐产品23.520g,配成250mL溶液,取出25.00mL用0.0500mol/LKMnO4溶液滴定,消耗KMnO4溶液19.50mL,则产品中莫尔盐的质量分数 。
11、废旧印刷电路板的回收利用可实现资源再生,并减少污染。废旧印刷电路板经粉碎分离,能得到非金属粉末和金属粉末
(1)废旧印刷电路板中回收的铁是新型电池的使用材料,如制成LiFePO4电池,它可用于电动汽车。电池反应为:FePO4+Li  LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨,含Li+导电固体为电解质。放电时其正极反应方程式为:
LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨,含Li+导电固体为电解质。放电时其正极反应方程式为:
(2)用H2O2 和H2SO4 的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) △H=64.39kJ·mol-1
2H2O2(l)=2H2O(l)+O2(g) △H=-196.46kJ·mol-1
H2(g)+1/2O2(g)=H2O(l) △H=-285.84kJ·mol-1
则在H2SO4 溶液中Cu 与H2O2 反应生成Cu2+和H2O的热化学方程式为: 。
(3)部分金属的回收需要氧化性很强的溶液,如金常用 和 的混合溶液溶解
(4)为了分离金属粉末常用到氰酸(HCN)溶液,HCN是一种有毒且较弱的酸,已知:常温下HCN的电离程度非常小,其Ka=6.2×10-10,0.1mol/L的NaCN的pH=11.1,0.1mol/L的NH4CN的pH=9.2, 则浓度都是0.1mol/L的NaCN和NH4CN溶液中,CN-水解程度大小为:NaCN NH4CN(填:> = < ),理由是:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com