
题目列表(包括答案和解析)
22. (8分)(1) 。(2) 杂化。
(3) 。(4) 。(请用相应的编号填写) (5) kJ/mol。
(6) 。
21.(6分)(1)X是__________,Z是_____________。(填写元素符号)
(2) ________________________________。
(3) _________________________________。
25.(10分)有一废水样品10L,经分析得知含游离氯(Cl2)浓度为0.012mol/L,其H+浓度为1×10-3mol/L。已知Cl2+Na2SO3+H2O=Na2SO4+2HCl。现欲除去其中的游离氯,并成为中性溶液,问需加浓度为0.1mol/L的Na2SO3溶液的体积是多少?需加入固体烧碱的质量是多少?
哈三中2009--2010学年度上学期高三学年九月考试
化学答案卷 序号
(共计 45分)
23.(9分)在已提取氯化钠、溴、镁等化学物质后的富碘卤水中,采用下面的工艺流程生产单质碘:

试回答:
(1)书写化学式:沉淀甲 ,丙中的溶质 。
(2)步骤③中加铁屑的量为__________。
(3)第④步操作中用稀H2SO4浸洗的目的是 。(填写字母编号)
a.除去未反应的NO3- b.除去未反应的I-
c.除去未反应的Fe d.除去碱性物质
(4)第⑦步提纯操作你认为最合适的是 。(填写字母编号)
A.分液 B.减压蒸馏 C.渗析 D.重结晶
(5)第⑥步操中反应的离子方程式 。
(6)鉴别丙和丁可选用的试剂是 。分离混合物和丁的方法是 。
 24.(12分)下图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。化合物B在常温常压下为气体,B和C的相对分子质量之比为4︰5,化合物D是重要的工业原料。
24.(12分)下图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。化合物B在常温常压下为气体,B和C的相对分子质量之比为4︰5,化合物D是重要的工业原料。
(1)写出A在加热条件下与H2反应的化学方程式 。
(2)写出E与A的氢化物反应生成A的化学方程式 。
(3)写出一个由D生成B的化学方程式 。
(4)将5 mL0.10 mol·L-1的E溶液与10 mL0.10 mol·L-1的NaOH溶液混合。
①写出反应的离子方程式 ;
②反应后溶液的pH ____7(填“大于”、“小于”或“等于”),理由是 ;
③加热反应后的溶液,其pH_____(填“增大”、“不变”或“减小”),理由是_____。
22. (8分)水是生命之源,也是一种常用的试剂。请回答下列问题:
(1)水分子中氧原子在基态时核外电子排布式为 。
(2)H2O分子中氧原子采取的是 杂化。
(3)水分子容易得到一个H+形成水合氢离子(H3O+)。对上述过程的下列描述不合理的是 。
A.氧原子的杂化类型发生了改变 B.微粒的空间构型发生了改变
C.微粒中的键角发生了改变
(4)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是______。(请用相应的编号填写)


(5)在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图所示),已知冰的升华热是51 kJ/mol,除氢键外,水分子间还存在范德华力(11 kJ/mol),则冰晶体中氢键的“键能”是_________kJ/mol。
(6)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子。请写出生成此配合离子的离子方程式: 。
21.(6分)已知:
①A、B、C、D四种物质均含元素X,有的还可能含有元素Y、Z。元素Y、X、Z的原子序数依次递增。
②X在A、B、C、D中都不呈现它的最高化合价。
③室温下单质A与某种常见一元强碱溶液反应,可得到B和C。
④化合物D受热催化分解,可制得元素Y的单质。
(1)元素X是__________,Z是_____________。(填写元素符号)
(2)写出③中反应的离子方程式:________________________________。
(3)写出④中反应的化学方程式:_________________________________。
19.有下列四种判断:①两种弱酸相互反应生成两种强酸;②两种弱酸盐相互作用后生成两种强酸盐;③一种弱酸和一种盐溶液作用后,得到一种强酸和一种盐;④两种酸溶液混合后,溶液的酸性减弱。其中有具体例证的是
A.①② B.②③
C.②③④ D.①②③④

 20.标准状况下,a g锌与一定量的浓硫酸反应生成SO2和H2的混合气体,经测定反应消耗硫酸的物质的量为b mol,则反应生成H2的体积为www.
20.标准状况下,a g锌与一定量的浓硫酸反应生成SO2和H2的混合气体,经测定反应消耗硫酸的物质的量为b mol,则反应生成H2的体积为www.
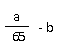


 A.
A.

 B.
B. 

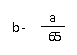
C. 
 D. 无法确定
D. 无法确定
Ⅱ 卷 (共计 45分)
18.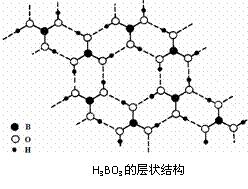 正硼酸(H3BO3)是一种片层状结构白色晶体,层内的H3BO3分子通过氢键相连(如下图)。下列有关说法正确的是
正硼酸(H3BO3)是一种片层状结构白色晶体,层内的H3BO3分子通过氢键相连(如下图)。下列有关说法正确的是
A.正硼酸晶体属于原子晶体
B.H3BO3分子的稳定性与氢键有关
C.分子中硼原子最外层为8e-稳定结构
D.含1molH3BO3的晶体中有3mol氢键
17.下列不能使溴水因发生化学反应而褪色的物质是
A.NaOH B.CCl4
C.乙烯 D.Na2SO3溶液
16.下列说法正确的是
A.二氧化硫能使品红溶液褪色是因为SO2具有氧化性www.
B.新制氯水的氧化性强于久置氯水
C.检验HCl气体中是否混有Cl2方法是将气体通入硝酸银溶液
D.浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com