
题目列表(包括答案和解析)
7.通过复习总结,你认为下列对化学知识概括合理的是 ( )
A.金属离子只有氧化性,非金属离子只有还原性
B.一种元素可能有多种氧化物,但同种化合价只对应一种氧化物
C.发生化学反应时失去电子越多的金属原子,还原能力越强
D.在化学反应中,一定有化学键的断裂和形成,并伴有能量的变化
6.下列说法正确的是 ( )
A.根据酸分子中含有的氢原子个数可将酸分为一元酸、二元酸等
B.胶体与溶液的本质区别是分散质的大小,Fe(OH)3胶体和MgCl2溶液均有丁达尔现象
C.因为NO2与NaOH反应为2NO2+2NaOH=NaNO2+NaNO3+H2O,所以NO2是酸性氧化物
D.铝粉和氧化镁粉末混合,不能发生铝热反应
5.用NA表示阿伏加德罗常数的值。下列叙述正确的是 ( )
A.17g甲基(-14CH3)所含中子数为9NA
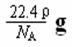 B.1mol C10H22分子中共价键总数为32 NA
B.1mol C10H22分子中共价键总数为32 NA
C.标准状况下,密度为ρg•L-1的某气体纯净物一个分子的质量为
D.常温下,0.2molCl2溶于等体积水中,转移电子数为0.2 NA
4.下图分别表示四种操作,其中有两处错误的是 ( )
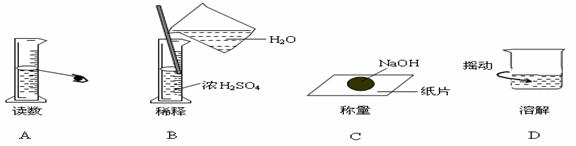
3.分类是化学学习和研究的常用手段。下列分类依据和结论都正确的是 ( )
A.H2O、HCOOH、(NH3)2Fe(SO4)2均含有氧,都是氧化物
B.HCl、H2SO4、HNO3均具有氧化性,都是氧化性酸
C.赤铁矿、磁铁矿、黄铁矿、孔雀石都是常见的铁矿石
D.Na2CO3、Ba(OH)2、NH4Cl、Na2O2都属于离子化合物
2.下列的叙述,其中正确的是 ( )
A.一定温度和压强下,某气体体积大小取决于其物质的量多少
B.摩尔是一个物理量,摩尔既能用来计量纯净物,又能用来计量混合物
C.若1mol某气体所占的体积为22.4L,则此时一定是在标准状况下
D.在标准状况下,1mol Cl2体积取决于其分子间隙大小,且Cl2具有很强的氧化性,只能作氧化剂
1.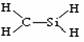 下列有关化学用语的说法中不正确的是( )
下列有关化学用语的说法中不正确的是( )

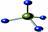 A.-OH与 都表示羟基 B.CH4Si的结构式:
A.-OH与 都表示羟基 B.CH4Si的结构式:
C.CH4分子的球棍模型:
D.次氯酸分子的电子式: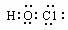
(三)已知 (注:R,R’为烃基)
(注:R,R’为烃基)
A(分子式为C4H8O2)为有机合成中间体,在一定条件下发生消去反应,可能得到两种互为同分异构体的产物,其中的一种B可用于制取合成树脂、染料等多种化工产品。A能发生如下图所示的变化。

试回答:
(1)写出符合下述条件A的同分异构体结构简式(各任写一种):
a.具有酸性______________________b.能发生水解反应______________________
(2)A分子中的官能团是_____________,D的结构简式是_____________。
(3)C→D的反应类型是___________,E→F的反应类型是___________
a.氧化反应 b.还原反应 c.加成反应 d.取代反应
(4)写出A与银氨溶液反应的化学方程式:
________________________________________________________________________________。
(5)写出C生成高聚物的化学方程式:
________________________________________________________________________________。
(二)碳碳双键有如下的断裂方式:
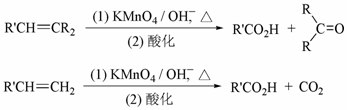
高分子单体A(C6H10O3)可进行如下反应(反应框图):

对框图中某些化合物性质说明:
室温下A不与NaHCO3溶液反应,但可与Na反应放出H2;B可与NaHCO3溶液反应放出CO2;C可与Na作用放出H2而D不能;G在室温下既不与NaHCO3溶液反应,也不与Na作用放出H2。
(1)写出A、D、E的结构简式。
A: D: E:
(2)B在浓H2SO4存在下与甲醇反应的产物能在一定条件下聚合,写出这个聚合物的结构简式: 。
(3)写出F→G的化学反应方程式: 。
(一)根据下面的反应路线及所给信息填空。
A\s\up7(Cl2,光照Cl2,光照① 
 \s\up7(NaOH,乙醇NaOH,乙醇△,②
\s\up7(NaOH,乙醇NaOH,乙醇△,② 
 \s\up7(Br2的CCl4溶液Br2的CCl4溶液③B\s\up7(④
\s\up7(Br2的CCl4溶液Br2的CCl4溶液③B\s\up7(④ 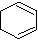

(1)A的结构简式是 ,B的名称是 。
(2)①的反应类型是 ,③的反应类型是 。
(3)反应④的化学方程式是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com