
题目列表(包括答案和解析)
27.(14分)香兰素存在于香草豆等植物中,是有机合成的重要原料。

 w_w w. k#s5_u.c o*
w_w w. k#s5_u.c o*
(1)香兰素含有C、H、O 3种元素,相对分子质量为152,氧元素的质量分数为31.6 %,
碳、氢元素质量比为12︰1。香兰素易溶于乙醇,熔点为81℃~ 83℃,沸点为284℃。
 ①
从香草豆等植物中可以提取香兰素,部分流程如下图所示。
①
从香草豆等植物中可以提取香兰素,部分流程如下图所示。
操作1的名称是 。
② 香兰素的分子式是 。
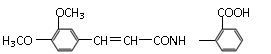 (2)以香兰素为原料,经过一系列转化,可以得到药物利喘贝
(2)以香兰素为原料,经过一系列转化,可以得到药物利喘贝
( )。
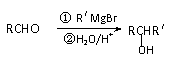
已知:
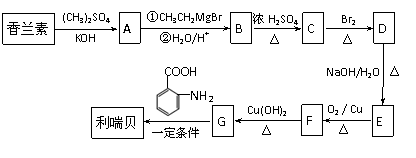
① 写出实现下列转化的化学方程式:

 w_w w. k#s5_u.c o*
w_w w. k#s5_u.c o*
G→利喘贝 。
E→F 。
② D分子内含有碳碳双键,C→D的反应类型为 。
③ B的结构简式是 。
④香兰素能发生银镜反应,其分子中苯环上取代基的数目和位置均与A相同。
1 mol香兰素与饱和溴水发生取代反应生成1 mol HBr,且最多能与1 mol Na反应。则香兰素
的结构简式是 。
26.(15分)硝酸是一种重要的化工原料,工业上生产硝酸的主要过程如下。

 w_w w. k#s5_u.c o*
w_w w. k#s5_u.c o*
(1)以N2和H2为原料合成氨气。反应:N2(g)+3H2(g) 2NH3(g) ΔH<0。
2NH3(g) ΔH<0。
① 下列有关反应速率的叙述,正确的是(选填序号) 。
a. 升高温度可增大活化分子百分数,加快反应速率
b. 增大压强不能增大活化分子百分数,但可以加快反应速率
c. 使用催化剂可以使反应物分子平均能量升高,加快反应速率
d. 在质量一定的情况下,催化剂颗粒的表面积大小,对反应速率有显著影响
② 一定温度下,在密闭容器中充入1 mol N2和3 mol H2发生反应。若容器体积恒定,达到平衡状态时,N2的转化率为α1 ;若容器压强恒定,达到平衡状态时,N2的转化率为α2,则α2 α1(填“>”、“<”或“=”)。
(2)以氨气、空气为主要原料制硝酸。
① NH3被氧气催化氧化生成NO的反应的化学方程式是 。
② 在容积恒定的密闭容器中进行反应2NO(g)+O2(g) 2NO2(g) ΔH>0。该反应的反
2NO2(g) ΔH>0。该反应的反
应速率(υ)随时间(t)变化的关系如右图所示。若t2、t4时刻只改变一个条件,下列说法正确的是(填选项序号) 。
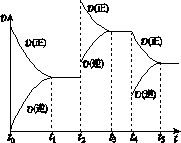 a.在t1 ~ t2时,可依据容器内气体的压强保持
a.在t1 ~ t2时,可依据容器内气体的压强保持
不变判断反应已达到平衡状态
b.在t2时,采取的措施可以是升高温度
c.在t3 ~ t4时,可依据容器内气体的密度保持
不变判断反应已达到平衡状态
d.在t5时,容器内NO2的体积分数是整个过程
中的最大值
(3)硝酸厂常用以下方法处理尾气:
ⅰ.碱液吸收法:用Na2CO3溶液吸收NO2生成CO2。若每9.2 g NO2和Na2CO3溶液反应时转移电子数为0.1 mol,则反应的离子方程式是 。
ⅱ.氨催化吸收法,原理是NH3与NOx反应生成无毒的物质。某同学采用以下装置和
步骤模拟工业上氮的氧化物处理过程。

 w_w w. k#s5_u.c o*
w_w w. k#s5_u.c o*
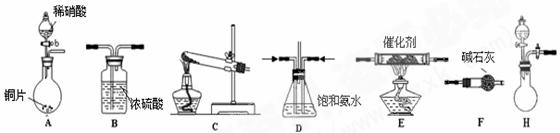
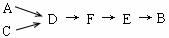
选用上述部分装置,按下列顺序连接成模拟尾气处理装置:
①A中反应的离子方程式: 。
②D装置作用有:使气体混合均匀、调节气流速度,还有一个作用是 。
③D装置中的液体可换成 (填序号)。
a.CuSO4溶液 b.H2O c.CCl4 d.浓H2SO4
④该同学所设计的模拟尾气处理实验还存在的明显缺陷是 。
25.(10分)化合物A是制玻璃的主要原料之一。常温下,化合物B、H、I为气体,B不
溶于水,H、I易溶于水,H的水溶液呈碱性,I的水溶液呈酸性。D元素是地壳中含量仅次
于氧的非金属元素。化合物J是一种可用于制造发动机的新型无机非金属材料,其相对分子
质量为140,其中D元素的质量分数为60 %。上述物质间的转化关系如下图所示。


 w_w w. k#s5_u.c o*
w_w w. k#s5_u.c o*
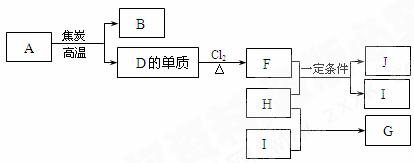
(1)除A外,制玻璃的主要原料还有物质(填化学式) 、 。
盛放NaOH溶液的试剂瓶不能用玻璃塞,原因是(用化学方程式表示)
。
(2)D元素在元素周期表中的位置是 。
(3)F和H反应生成J和I反应的化学方程式是 。
(4)下列说法正确的是(填选项序号) 。
a.上述由A生成D的单质的反应属于置换反应
b.D元素在自然界中主要以单质形式存在
c.G是含有极性共价键的离子化合物
d.I是强电解质,G是弱电解质,二者的水溶液都显酸性
24.(7分)(1)在常温下浓度均为0.1mol/L的下列6种溶液的pH如下表:

 w_w w. k#s5_u.c o*
w_w w. k#s5_u.c o*
|
溶质 |
NaHSO3 |
CH3COONa |
NaHCO3 |
Na2CO3 |
NaClO |
NaCN |
C6H5ONa |
|
pH |
5.8 |
8.8 |
9.7 |
11.6 |
10.3 |
11.1 |
11.3 |
① 多元弱酸的正盐是分步水解的,第一步水解比第二步水解程度大得多,产生此规律的原因是_________________________________________________________________。
② 根据表中数据判断,常温时下列反应不能成立的是___________(填编号)。
a.CO2 + NaHSO3→NaHCO3+ SO2 b.CO2 +H2O +2C6H5ONa→Na2CO3+2C6H5OH
c.Na2CO3+C6H5OH→NaHCO3+C6H5Ona d.CH3COOH+NaCN→CH3COONa+HCN(2)已知在t℃,某Ba(OH)2稀溶液中,c(H+)=10-amol/L,c(OH-)=10-bmol/L,且a+b=16。
向该溶液中逐滴加入pH=c的盐酸,t℃下测得混合液的pH如下表所示:
|
序号 |
Ba(OH)2溶液体积/mL |
盐酸体积/mL |
混合液pH |
|
1 |
22.00 |
0 |
10 |
|
2 |
22.00 |
18.00 |
9 |
|
3 |
22.00 |
22.00 |
8 |
假设混合时体积变化忽略不计,则c为 。
23.(10分)A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、
W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数
与主族序数相等。

 w_w w. k#s5_u.c o*
w_w w. k#s5_u.c o*
(1)由A、B、W三种元素组成的18电子微粒的电子式为 。
(2)用B单质、E单质分别作电极,与浓KOH溶液组成原电池,其正极上的电极反应为 。
(3)由W、D、E三元素组成的盐加入水中,恢复至室温,则Kw (填“增大”、“减
小”或“不变”) ;溶液中各离子浓度从大到小的顺序为 。
(4)废印刷电路反上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶
解。现改用A2W2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出反应的离子方程式 。
(5)已知:B、E的单质各1 mol完全燃烧,分别放出热量a kJ和b kJ;E单质能和B
的最高价氧化物发生置换反应。在298K时,若生成3 mol B的单质,则该置换反应的
 =
。
=
。
22.将15.6 g Na2O2和5.4 g Al同时放入一定量的水中,充分反应后得到200 mL溶液,再向该溶液中缓慢通入标准状况下的HCl气体6.72 L,若反应过程中溶液的体积保持不变,则下列说法正确的是

 w_w w. k#s5_u.c o*
w_w w. k#s5_u.c o*
A.标准状况下,反应过程中得到6.72L的气体 B.最终得到7.8g沉淀
C.最终得到的溶液中只含NaCl溶质 D.最终得到的溶液中c(Na+)=1.5mol/L
Ⅱ卷(56分)
21. 由短周期元素组成的中学常见无机物A、B、C、D、E、X
由短周期元素组成的中学常见无机物A、B、C、D、E、X 存在如在右图转化关系(部分生成物和反应条件略去)
存在如在右图转化关系(部分生成物和反应条件略去) 下列推断错误的是
下列推断错误的是

 w_w w. k#s5_u.c o*
w_w w. k#s5_u.c o*
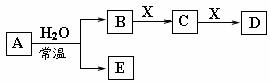
A.若X是Na2CO3,C为含极性键的非极性分子,则A一定是氯气,且D和E不反应
B.若A是单质,B和D的反应是OH-+HCO3-=H2O+CO32-,则E是一种清洁的能源
C.若D为CO,C能和E反应,则A一定为Na2O2
D.若D为白色沉淀,与A摩尔质量相等,则X一定是铝盐
20.X、Y、Z是三种气态物质,在一定温度下其变化符合下图。下列说法一定正确的是
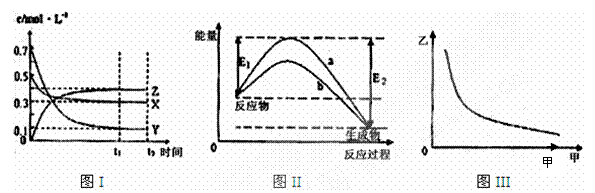
图I 图II 图III
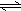 A.该反应热化学方程式为X(g)
+3Y(g)
2Z(g) △H= ―(E2―E1)
A.该反应热化学方程式为X(g)
+3Y(g)
2Z(g) △H= ―(E2―E1)
B.若图III中甲表示压强,乙表示Z的含量,则其变化符合图III中曲线
C.该反应达平衡后,若升高温度,Y的转化率降低
D.图II中曲线b是加入催化剂时的能量变化曲线,曲线a是没有加入催化剂时的能量变化曲线
19.下列溶液中微粒的物质的量浓度关系正确的是

 w_w w. k#s5_u.c o*
w_w w. k#s5_u.c o*
A.氯水中:c(Cl2)=2[c(ClO-)+c(Cl-)+c(HClO)]
B.Na2CO3溶液:c(OH-)-c(H+)=c(HCO3-)+2 c(H2CO3)
C.等浓度的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+ c(H2CO3)
D.室温下,向0.01 mol·L-1 NH4HSO4溶液中滴加NaOH溶液至中性:
c(NH4+)>c(Na+)>c(SO42-)>c(OH-)=c(H+)
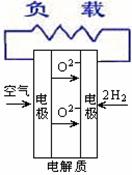
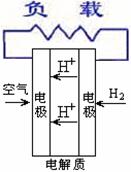
18. 燃料电池不是把还原剂、氧化剂物质全部贮藏在电池内,而是在工作时,不断从外界输入,同时将电极反应产物不断排出电池。下面有4种燃料电池的工作原理示意图,其中正极的反应产物为水的是
燃料电池不是把还原剂、氧化剂物质全部贮藏在电池内,而是在工作时,不断从外界输入,同时将电极反应产物不断排出电池。下面有4种燃料电池的工作原理示意图,其中正极的反应产物为水的是

 w_w w. k#s5_u.c o*
w_w w. k#s5_u.c o*
A.固体氧化物燃料电池
|
B.碱性燃料电池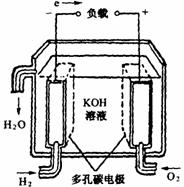 |
||||
C.质子交换膜燃料电池
|
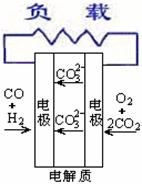
D.熔融盐燃料电池
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com