
题目列表(包括答案和解析)
19.(9分)Ⅰ. 固体氧化物燃料电池(SOFC)以固体氧化物作为
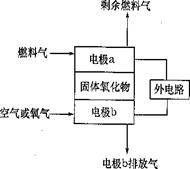 电解质介质,其工作原理如图所示。
电解质介质,其工作原理如图所示。
(1)电极b的电极反应式是
(2)假设外电路是电解硫酸铜溶液的装置。
若以C2H4为燃料气,工作一段时间后
燃料电池中消耗了标准状况下的2.24LC2H4,
则外电路阴极区的产物及其物质的量分别
是 。
Ⅱ.下列试剂均可用于除去NaCl溶液中混有
的少量Na2S。
A. CaCl2 B.AgCl C.HCl
(1)最好的试剂是 (填写序号字母)。
写出加人该试剂时反应的离子方程式 。
(2)选用另外两种试剂实验时存在缺陷,简叙其主要缺陷:
18.(10分)现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子Na+、Al3+、Mg2+、Ba2+、Fe3+和五种阴离子Cl-、OH-、NO 、CO、X中的一种。
(1)某同学通过比较分析,认为无须检验就可判断其中必有的两种物质是
和 。
(2)物质C中含有离子X。为了确定X,现将(1)中的两种物质记为A和B,当C与B的溶液混合时,产生红褐色沉淀和无色无味气体;当C与A的溶液混合时也产生沉淀,向该沉淀中滴入稀HNO3,沉淀部分溶解。则:
①X为 (填字母)。 a.Br- b.SO c.CH3COO- d.HCO
②A中含有的阴阳离子个数之比
③将0.02 mol的A与0.01 mol的C同时溶解在足量的蒸馏水中,充分反应后,最终所得沉淀的质量为 (精确到0.1 g)。
④利用上述已经确定的物质,可以检验出D、E中的阳离子。请简述实验操作步骤、现象及结论: 。
(3)将Cu投入装有D溶液的试管中,Cu不溶解;再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现。则物质D一定含有上述离子中的 (填相应的离子符号)。有关反应的离子方程式为
17.(7分) 某反应体系中的物质有:Cr2(SO4)3、K2S2O8、K2Cr2O7、K2SO4、H2SO4、H2O。
已知K2S2O8的氧化性比K2Cr2O7强。
(1)请将以上反应物与生成物编写成一个氧化还原反应方程式(不要求配平)
(2)反应中,被还原的物质是 ,Cr2(SO4)3是 。
(3)请将氧化剂与还原剂的化学式及配平后的系数填入下列空格中,并标出电子转移方向和数目:




+ +……
(4)在酸性条件下K2Cr2O7与草酸(H2C2O4)反应的产物是:Cr2(SO4)3、CO2、K2SO4和H2O,则还原剂与氧化剂物质的量之比为 。
16.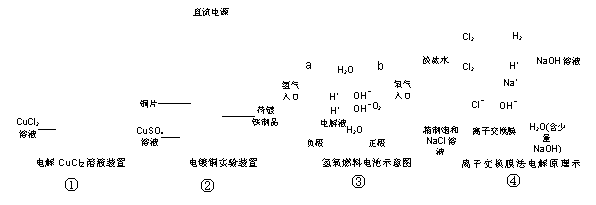 下列关于下图的说法是 ( )
下列关于下图的说法是 ( )
A.①装置中阴极处产生的气体能够使湿润淀粉KI试纸变蓝
B.②装置中待镀铁制品应与电源正极相连
C.③装置中电子由b极流向a极
D.④装置中的离子交换膜可以避免生成的Cl2与NaOH溶液反应
15.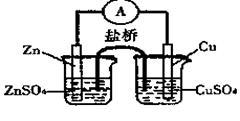 关于右图所示的原电池,下列说法正确的是 ( )
关于右图所示的原电池,下列说法正确的是 ( )
A.电子从锌电极通过检流计流向铜电极
B.盐桥中的阴离子向硫酸铜溶液中迁移
C.锌电极发生还原反应,铜电极发生氧化反应
D.铜电极上发生的电极反应是
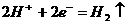
14. 一种碳纳米管(氢气)二次电池
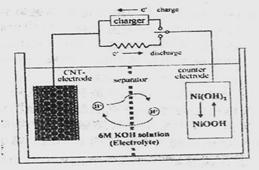
一种碳纳米管(氢气)二次电池
原理如右图,该电池的电解质为
6mol·L-1KOH溶液,下列说法
不正确的是 ( )
A.储存H2的碳纳米管放电时为
负极,充电时为阴极
B.放电时负极附近pH减小
C.放电时电池正极的电极反应为:
NiO(OH)+H2O+e-===Ni(OH) 2+OH-
D.放电时,电池反应为
2H2+O2===2H2O
13.化学在生产和日常生活中有着重要的应用。下列说法不正确的是 ( )
 A.工业制AlN: Al2O3+N2+3C
A.工业制AlN: Al2O3+N2+3C 2AlN+3CO反应中,Al2O3是氧化剂
2AlN+3CO反应中,Al2O3是氧化剂
 B.在海轮外壳上镶入锌块,可减缓船体的腐蚀速率
B.在海轮外壳上镶入锌块,可减缓船体的腐蚀速率
 C.MgO的熔点很高,可用于制作耐火耐高温材料
C.MgO的熔点很高,可用于制作耐火耐高温材料
 D.明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
D.明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
12.在稀硫酸中加入铜粉,铜粉不溶,再加入下列固体粉末:①FeCl2; ②Fe2O3; ③Zn;
④KNO3; ⑤HCl; ⑥H2O2 ;铜粉可溶解的是
A.①②⑤ B.②④⑥ C.②③⑤ D.①④⑥
11.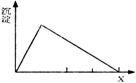 将溶液(或气体)X,逐渐加入(或通入)到一定量溶液Y中,产生沉淀的量与加入X的量的关系如下图,符合题意的一组物质是 ( )
将溶液(或气体)X,逐渐加入(或通入)到一定量溶液Y中,产生沉淀的量与加入X的量的关系如下图,符合题意的一组物质是 ( )
|
|
A |
B |
C |
D |
|
X |
H2S |
HCl |
NH3 |
NH3·H2O |
|
Y |
Na2SO4 |
Na[Al(OH)4] |
AlCl3 |
AgNO3 |
10.高铁酸钾K2FeO4是一种新型、高效、氧化性比Cl2更强的水处理剂,工业上常用下列反应先制高铁酸钠:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,然后在低温下,在高铁酸钠溶液中加KOH固体至饱和就可析出高铁酸钾,下列有关说法不正确的是
( )
A.Na2O2在反应中既作氧化剂,又作还原剂
 B.制取高铁酸钠时,每生成lmolNa2FeO4反应中共有4mol电子转移
B.制取高铁酸钠时,每生成lmolNa2FeO4反应中共有4mol电子转移
C.高铁酸钾在该温度下的溶解度比高铁酸钠的溶解度小
D.K2FeO4能消毒杀菌,其还原产物水解生成的Fe(OH)3胶体能吸附水中的悬浮杂质
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com