
题目列表(包括答案和解析)
23.下列反应的离子方程式正确的是 ( )
A.向NaOH溶液中通入过量的CO2气体:CO2+2OH-=HCO3-+H2O
 B.Na2S溶液呈碱性:S2-+H2O HS-+OH-
B.Na2S溶液呈碱性:S2-+H2O HS-+OH-
C.Fe3O4与稀硝酸反应:Fe3O4+8H+=Fe2++2Fe3++4H2O
D.偏铝酸钠溶液中加入过量盐酸:AlO2-+4H+=Al3++2H2O
22.下列除去杂质的方法正确的是 ( )
|
|
物质(杂质) |
除杂方法 |
|
A |
CO2(HCl) |
将气体通过盛有饱和NaHCO3溶液的洗气瓶 |
|
B |
Cl2(HCl) |
将气体通过盛有NaOH溶液的洗气瓶 |
|
C |
CaCO3(SiO2) |
加入足量盐酸后过滤、洗涤 |
|
D |
Mg(Al) |
加入足量NaOH溶液后过滤、洗涤 |
12.有关下图所示化合物的说法不正确的是:
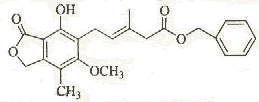
A.既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2发生取代反应
B.1 mol该化合物最多可以与3 mol NaOH反应
C.既可以催化加氢,又可以使酸性KMnO4溶液褪色
D.既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体
11. X、Y、Z三种短周期元素在周期表中的位置如图, Y原子的最外层电子数是次外层电子数的3倍,下列说法中错误的是 ( )
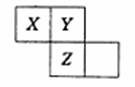 A.氢化物稳定性:X<Y
A.氢化物稳定性:X<Y
B.Z元素的最高价氧化物对应的水化物是一种强酸
C.三种元素原子半径的大小顺序为:X>Y>Z
D.X元素可以形成多种氧化物
10.已知高氯酸铵是火箭的一种燃料,加热时发生反应: NH4ClO4 -----N2↑+ H2O↑+Cl2↑+ O2↑(方程式未配平),该反应放出大量的热。下列有关叙述不正确的是 ( )
A.该反应的氧化产物只有氮气 B.在标准状态下,生成22.4L Cl2得到了14mole-
C.该反应中被还原的元素位于元素周期表中第三周期第VIIA族
D.该反应属于分解反应,又属于氧化还原反应
9.设NA为阿伏加德罗常数的数值,则下列说法正确的是 ( )
A.2.24LCl2中含有的原子数一定为0.2 ×6.02×1023
B.在标准状态下,11.2L NO与11.2L O2混合后气体分子数为0.75NA
C.常温常压下,足量的Fe在1molCl2中充分燃烧,转移的电子数为2NA
D.106gNa2CO3固体中的阴离子数大于NA
8.在下述条件下,一定能大量共存的离子组是: A.无色透明的水溶液中:K+、Ba2+、I-、MnO4- B.含有大量NO3-的水溶液中:NH4+、Fe2+、SO42-、H+ C.c(HCO3-)=0.1mol·L-1的溶液中:Na+、K+、CO32-、Br- D.强碱性溶液中:ClO-、S2-、HSO3-、Na+
7.生活中的某些问题常常涉及化学知识。下列叙述错误的是
A.合金材料中可能含有非金属元素
B.汽油、柴油和植物油都是碳氢化合物
C.废弃的塑料、金属、纸制品及玻璃都是可回收再利用的资源
D.造成大气污染的S02、CO和NO等,主要来源于煤、石油等化石燃料的燃烧和汽车尾气的排放
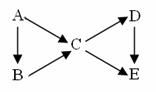
22.(14分)A为单质,B、C、D、E为与A含有相同元素的化合物,它们之间有如下转化关系:
(1)若上图中B、C均为氧化物、D、E均为盐,则A可能是__________。
 ①Na ②N2 ③C
④S
①Na ②N2 ③C
④S
(2)若五种物质的焰色反应均为黄色,其中C、D、E的水溶液均显碱性,且等浓度时碱性C>D>E,B可做生氧剂,则B中含有的化学键类型为__________________;
A转化成C的离子方程式为: ________________________________,
D转化成E的离子方程式为_______________________________________。
(3)若常温下B、C、D均为气体,且B气体能使湿润的红色石蕊试纸变蓝
①在工业上生产B气体时为了加快反应速率应选择的条件是______________,其中能提高反应物的转化率的条件是___________。
②C、D是汽车尾气中的有害成分,用NaOH溶液吸收可消除污染,反应的化学方程式为__________________________________。
21.(12分)已知2A2(g)+B2(g) 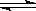 2C3(g);△H=-Q1 kJ/mol(Q1>0),在一个有催化剂的固定
2C3(g);△H=-Q1 kJ/mol(Q1>0),在一个有催化剂的固定
容积的容器中加入2 molA2和1 molB2,在500℃时充分反应,达平衡后C3的浓度为
w mol/L,放出热量Q2 kJ。
(1)若在原来的容器中,只加入2mol C3,500℃时充分反应达平衡后,吸收热量Q3 kJ,C3浓度 (填>、=、<)w mol/L,Q1、Q2、Q3 之间满足何种关系 (用代数式表示)。
(2)能说明该反应已经达到平衡状态的是 。
 a.v(C3)=2 v (B2);
b.容器内压强保持不变
a.v(C3)=2 v (B2);
b.容器内压强保持不变
c.v逆(A2)=2 v正(B2) d.容器内的密度保持不变
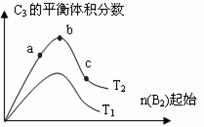
(3)改变某一条件,得到如图的变化规律(图中T表示温度,n表示物质的量),可得出的结论正确的是 ;
A.反应速率c>b>a
B.达到平衡时A2的转化率大小为:b>a>c
C.T2>T1
D.b点时,平衡体系中A、B原子数之比接近2∶1
(4)若将上述容器改为恒压容器(反应前体积相同),起始时加入2 molA2和l molB2,500℃时充分反应达平衡后,放出热量Q4 kJ,则Q2 Q4 ( 填 > 、 = 、 < ),理由是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com