
题目列表(包括答案和解析)
29.(15分)
某氮肥厂氨氮废水中的氮元素多以NH4+和NH3·H2O的形式存在,该废水的处理流程如下:

(1)过程I:加NaOH溶液,调节pH至9后,升温至30℃,通空气将氢赶出并回收。
①用离子方程式表示加NaOH溶液的作用 。
②用化学平衡原理解释通空气的目的: 。
(2)过程Ⅱ:在微生物作用下,NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如下:(参看图17)
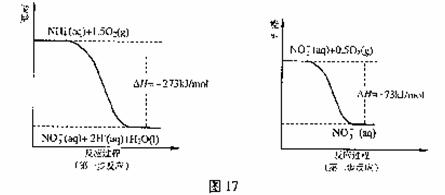
①第一步反应是 反应(选填“放热”或“吸热”),判断依据是 。
1 mol NH4+(aq)全部被氧化成NO3-(aq)的热化学方程式:
(3)过程Ⅲ,在一定条件下,向废水中加入CH3OH将NHO2还原成N2,若该反应消耗1 mol CH3OH,转移6 mol电子,则参加反应的还原剂和氧化剂的质量之比为 。
28.(16分)
为了测定实验室长期存放的Na2SO3固体的纯度,某化学活动小组准确称取Wg固体样品,配成250mL溶液,分别取25.00mL上述溶液进行下列三组实验:
甲组:加入足量的盐酸酸化的BaCl2溶液,过滤,洗涤和干燥沉淀,称得沉淀质量为m1g
乙组:加入足量的盐酸酸化的Ba(NO3)2溶液,过滤、洗涤和干燥沉淀,称得沉淀质量为m2g
丙组,用a mol.L 的酸性KMnO4溶液进行滴定。
(5SO52-+2MnO4-+6H+=5SO42-+2Mn2++3H2O),消耗KMnO4溶液b mL。
(1)配制250mL Na2SO3溶液时,必须用到的实验仪器有:烧杯、玻璃棒、托盘天平、胶头滴管、 。
(2)在丙组实验中,高锰酸钾溶液用 滴定管盛装,滴定时是否需要选择指示剂? (填“需要”或“不需要”)。滴定终点的颜色变化是 。
(3)用丙组的实验数据计算Na2SO4的纯度的表达式为 。
(4)若按乙组方案测定Na2SO3纯度,则其结果比甲组和丙组同学的结果都要 (选填“高”、“低”或“不变”),并分析产生上述的原因?
27.(14分)
有机化合物A为一元溴代有机酸,仅含C、H、O、Br元素,与A相关的反应框图如下:
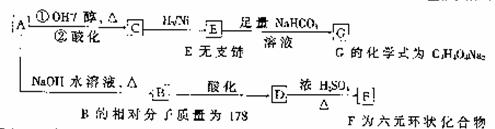
(1)写出A、E的结构简式:
A: E:
(2)写出下列有机反应对应的反应类型:
反应A→B: ;反应C→E: 。
(3)写出D→F的化学反应方程式: 。
(4)写出与C具有相同官能团的同分异构体的结构简式 。
13.a mol FeO与b mol FeS投入到V L、c mol·L-1的硝酸溶液中恰好完全反应,生成d mol NO气体,所得澄清溶液的成分可看作是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸不可能为 ( )
A.(a+b)×189g B.(21a+189b)g C.3(a+b)mol D.(Vc-d)mol
第Ⅱ卷(非选择题,共10个沔题,共174分)
原子序数从小到大排列的四种短周期元素W、X、Y、Z,四种元素的原子最外层电子数之和等于12,W是原子半径最小的元素;由X、Y元素可组成非极性分子A,A在常温下为气体;由Y、Z元素按原子个数比1:1可组成离子化合物B;A与B反应可生成Y2气体。
(1)元素W是 (写元素符号),写出B的电子式 ;
(2)写出金属镁在A中燃烧的化学方程式 ,该反应属于 (填写序号)
a.置换反应 b.化合反应 c.分解反应 d.复分解反应 e.氧化还原反应
(3)C是由X、Y、Z三种元素组成的盐,C能与盐酸反应生成A,则C的化学式是 ;
(4)D是由W、X、Y三种元素按原子个数比为1:1:2组成的一种酸,D在常温下为固体。已知在含1 mol D 的水溶液中加入1 mol C恰好反应生成1 mol A。则D的化学式是 ;D能使酸性高锰酸钾溶液褪色,说明D具有 性。
12.下列装置或操作能达到实验目的的是 ( )
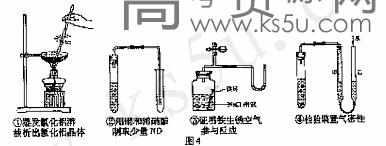
A.①②③④ B.③④ C.②③④ D.①②
11. 可逆反应:mA(g)+nB(g) pC(g)+qD(g),在T1、T2,在压强P1、P2下,产物D的物质的量n与反应时间t的关系如图3所示,下列各项中错误的是 ( )
可逆反应:mA(g)+nB(g) pC(g)+qD(g),在T1、T2,在压强P1、P2下,产物D的物质的量n与反应时间t的关系如图3所示,下列各项中错误的是 ( )
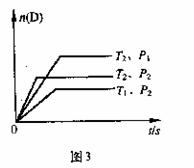 A.逆反应为吸热反应
A.逆反应为吸热反应
B.T1<T3
C.P1<P2
D.m+n<p+q
10.在常温时,将a1 mL b1 mol/L CH3COOH溶液中加玫到a2 mL b2 mol/L NaOH溶液中,下列结论中,错误的是 ( )
A.如果a1=a2,b1=b2,则混合溶液中c(CH3COO-)=c(Na+)
B.如果混合溶液的pH=7,则混合溶液中c(CH3COO-)=c(Na+)
C.如果混合溶液的pH>7,则可能a1b1=a2b2
D.如果a1=a2,且混合溶液的pH<7,则b1>b2
9.下列离子方程式中,不正确的是 ( )
A.向FeBr2溶液中通和少量的Cl2:2Fe2++Cl2=2Fe3++2Cl-
B.向NH4Al(SO4)2溶液中滴入Ba(OH)2恰好使SO42-反应完全
2Ba2++4OH-+Al3++2SO42- 2BaSO4↓+AlO2-+2H2O
C.向Mg(HCO3)2溶液中加入过量的 NaOH溶液
MG2++2HCO3-+4OH-=Mg(OH)3↓+2CO32-+2H2O
D.向Fe(NO3)2溶液中加入稀盐酸:3Fe2++4H++NO3- 3Fe3++NO↑+2H2O
8.X、Y、Z为三种短周期元素,X、Y同周期,X、Z的最低价离子分别为X2-、Z-、Y2+与Z+具有相同的电子层结构,下列叙述一定错误的是 ( )
A.离子半径X2->Z->Y2+ B.它们的原子半径Z>Y>X
C.它们的原子序数X>Y>Z D.原子最外层上的电子数Z>X>Y
7.在化学学科中经常使用下列物理量,其中跟阿伏加德罗常数(NA)无关的组合是( )
①原子质量(m)②摩尔质量(M)③原子半径(r)④键能(E)(断裂1 mol共价键时需吸收的能量)⑤物质的量(u)⑥化学反应速率(v)⑦气体摩尔体积(Vm)⑧溶解度(S)⑨燃烧热(△H)⑩溶质的质量分数( )
)
A.①③⑧⑩ B.②④⑤⑥⑦⑨ C.①②③④⑤ D.⑥⑦⑧⑨⑩
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com