
题目列表(包括答案和解析)
7.铝元素是金属元素,某同学认为铝也有一定的非金属性。下列描述中,你认为能支持该同学观点的是( )
A.铝片能与盐酸反应生成氢气 B.氢氧化铝能溶于强碱溶液
C.氯化铝溶液显酸性 D.铝能发生铝热反应
6.锌空气燃料电池具有安全、零污染、高能量、大功率、低成本及材料可再生等优点,因而被专家们认为是装备电动汽车等的理想动力电源。锌空气燃料电池,通常以NaCl溶液或NaOH溶液为电解液,锌为负极,空气电极为正极。下列说法正确的是( )
A.以NaOH溶液为电解液时,电池在工作过程中电解液的pH保持不变
B.以NaOH溶液为电解液时,负极反应为:Zn+4OH--2e-→ZnO2-+2 H2O
C.以NaCl溶液或NaOH溶液为电解液时,正极反应都为:O2+4e-→2O2-
D.电池工作时,电子通过外电路从正极流向负极
5.下列实验装置、试剂选用或操作正确的是( )
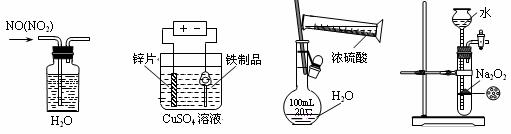
A.除去NO中的NO2 B.铁制品表面镀锌 C.稀释浓硫酸 D.制备少量O2
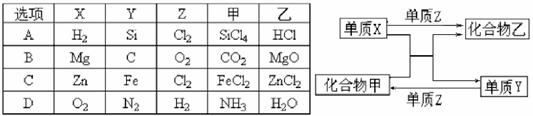
4.X、Y、Z是三种常见的单质,甲、乙是两种常见的化合物。下表各组物质之间通过一步反应不能实现如图所示转化的是( )
3.(NH4)2SO4在一定条件下发生如下反应:
4(NH4)2SO4 =N2↑+6NH3↑+3SO2↑+SO3↑+7H2O
将反应后的混合气体通入BaCl2溶液,产生的沉淀为( )
A.BaSO4 B.BaSO3 C.BaS D.BaSO4和BaSO3
2.下列有关物质的性质或应用的说法不正确的是( )
A.二氧化硅是生产光纤制品的基本原料 B.水玻璃可用于生产黏合剂和防火剂[
C.亚硝酸钠可以用作食品添加剂 D.石油分馏可获得乙烯、丙烯和丁二烯
1.下列说法正确的是( )
A.阴极射线、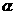 -粒子散射现象及布朗运动的发现都对原子结构模型的建立作出了贡献
-粒子散射现象及布朗运动的发现都对原子结构模型的建立作出了贡献
B.纤维素、PLA、纤维二糖、甲壳素、硝化纤维等都是高分子化合物
C.高容量储氢材料的研制是推广应用氢氧燃料电池的关键问题之一
D.硫、白磷、臭氧、碳-60、氩、水等物质固态时都是分子晶体,分子内都存在共价键
26.(8分)将2.5克碳酸钠、碳酸氢钠和氢氧化钠的固体混合物完全溶于水制成溶液,然后向该溶液中逐滴加入1mol/L盐酸。所加入的盐酸溶液的体积与产生的二氧化碳气体的体积(标准状况)的关系如图所示:
(1) 写出OA段所反应的离子方程式___________________________________________
(2) 当加入35mL盐酸时,所产生的二氧化碳体积(标准状况)是_______________mL。
(3) 计算原混合物中碳酸钠的质量分数(写出计算过程)。
|
|
|
|
|





25.(6分)常温下,将20.0 g 14%的NaCl溶液跟30.0 g 24%的NaCl溶液混合,得到密度为1.17 g/cm3的混合溶液。计算:
(1)该混合溶液中NaCl的质量分数。
(2)该混合溶液中NaCl的物质的量浓度。
(3)在1 000 g水中需加入多少摩尔氯化钠,才能使其浓度恰好与上述混合溶液浓度相等。(保留1位小数)
24.(8分)某反应体系中反应物与生成物有: K2SO4、CaSO4、MnSO4、CaC2O4、KMnO4、H2SO4、H2O和一种未知气体X。
(1)已知CaC2O4在反应中失去电子,则该反应的氧化剂是 。
(2)在标准状况下生成11.2LX时,有0.5mol 电子转移,共消耗0.25mol CaC2O4,X的化学式为 。
(3)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方向和数目:
+
(4) 反应中CaC2O4表现 性,发生 反应,生成 产物(选填“氧化”或“还原”),氧化还原反应的本质是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com