
题目列表(包括答案和解析)
5. 用于净化汽车尾气的反应:2NO(g)+2CO(g) CO2(g)+N2(g),己知该反应速率极慢,570K时平衡常数为1×1059。下列说法正确的是 ( )
用于净化汽车尾气的反应:2NO(g)+2CO(g) CO2(g)+N2(g),己知该反应速率极慢,570K时平衡常数为1×1059。下列说法正确的是 ( )
A.装有尾气净化装置的汽车排出的气体中不再含有NO或CO
B.提高尾气净化效率的常用方法是升高温度
C.提高尾气净化效率的最佳途径是研制高效催化剂
D.570K时及时抽走CO2、N2,平衡常数将会增大,尾气净化效率更佳
4.下列有关金属及其化合物的说法正确的是 ( )
A.由于铝在常温下不能与氧气反应,所以铝制品具有一定的抗腐蚀性能,是一种应用广泛的金属材料
B.住FeCl3溶液中滴入KI一淀粉溶液,溶液变蓝色
C.向紫色石蕊试液中加入过量的Na2O2粉末,振荡,溶液变为蓝色并有气泡产生
D.装修门窗使用的铝合金材料的硬度比铝小,熔点比铝低
3.下列离子方程式正确的是 ( )
A.住碳酸氢钙溶液中滴入少量氢氧化钠溶液:OH-+HCO Ca2+=CaCO3↓+H2O
Ca2+=CaCO3↓+H2O
B.将一小块金属钠投入到硫酸铜溶液中:2Na+Cu2+====Cu+2Na+
 C.NaHCO3溶液显碱性:HCO
C.NaHCO3溶液显碱性:HCO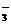 +H2O OH-+CO
+H2O OH-+CO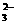
 D.氯气溶解于水:Cl2+H2O 12H++Cl-+ClO-
D.氯气溶解于水:Cl2+H2O 12H++Cl-+ClO-
2.下列说法正确的是 ( )
A.将25g CuSO4·5H2O溶于1L水中,可配制成0.1 mol·L-1CuSO4溶液
B.用盐析法除去氢氧化铁胶体中混有的氯离子
C.用向下排空气法收集NH。,并用湿润的蓝色石蕊试纸检验NH。是否收集满了
D.制乙炔时,用饱和食盐水代替水是为了减缓电石与水的反应速率
1.下列有关生活和生产中的化学知识描述不正确的是 ( )
A.使用纤维素和淀粉为原料制成的微生物降解塑料,可治理“白色污染”
B.发电厂的煤在燃烧时加入适量生石灰,有利于环境保护
C.泄露在美国墨西哥湾海洋中的大量原油能被海洋生物迅速分解,不会导致生态灾难
D.大力开发风能、太阳能、核能,有利于实现“低碳经济”,减少温室气体的排放
29.(14分)下图所示装置是用于气体制备、干燥、性质验证、尾气处理的部分仪器装置(加热及夹持固定装置均已略去)。请根据下列要求回答问题。

⑴若烧瓶中盛装Na2O2,分液漏斗中盛装浓氨水,则:
①烧瓶内除了能产生O2外,还能产生大量NH3。能产生大量NH3的原因是:
a.Na2O2与水反应,使溶剂减少,降低NH3的溶解量,使氨气逸出;
b.Na2O2与水反应,放热,使氨气逸出;
c. ;
②用产生的气体做氨的催化氧化实验,各仪器装置按气流方向(从左到右)连接顺序是:A→_______→_________→_______.
⑵若烧瓶中盛装Zn片,分液漏斗中盛装稀H2SO4,则:
当制备H2、验证H2还原性并检验H2的氧化产物,仪器连接顺序A→C→B→B→D时,两次使用B装置,第二个B装置中所盛的药品是
(写化学式);D装置的作用是 。
② 上述实验中为了使H2产生的速率不至于过快,在不改变现有药品及其浓度的条件下,可采取的方法有 、 等。
③甲同学认为,若锌片完全溶解,且第一个B中固体足量,能与进入气体充分反应,则可测定第一个B装置质量的变化来计算锌片的纯度。乙同学反对此观点,你认为他反对的理由是 。
28.(15分)A.B.C.D.E、F是中学化学中常见的气体,它们均由短周期元素组成,具有如下性质:
①B能使湿润的红色石蕊试纸变蓝, D.F不能使湿润的石蕊试纸变色;
②A能使湿润的蓝色石蕊试纸先变红,后褪色;将红热的铜丝放入装有A的瓶中,瓶内充满棕黄色的烟;
③将点燃的镁条放入装有E的瓶中,镁条剧烈燃烧,生成白色粉末,瓶内壁附着黑色颗粒;
④将A和D 在瓶中混合后于亮处放置几分钟,瓶内壁出现油状液滴并产生C;
⑤将A和B混合,得到F和C。
回答下列问题:
(1)B分子的空间构型为 , E的电子式是 ;
(2)③中发生反应的化学方程式是 ;
(3)⑤中发生反应的化学方程式是 ;
(4)已知标准状况下体积为1.12L的D完全燃烧生成E和液态水时,放出热量44.5kJ,写出表示D燃烧热的热化学方程式______________________________________.
(5)一定条件下,向废水中加入CH3OH,将HNO3还原成F。若该反应消耗16 gCH3OH转移3 mol电子;该反应的化学方程式为__________________________________.
27.(17分)已知如下信息:
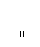
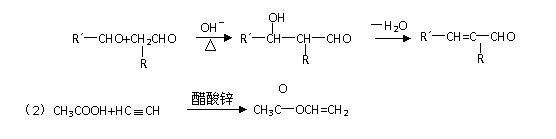 (1)
(1)
下图表示一些有机物之间的相互转化关系, A能发生银镜反应,欲使A与M发生信息(1)所示的反应,且M为能与A发生此类反应中分子量最小的物质;G不可使溴水褪色;在物质H中,除苯环外另有一个四元环。试回答:

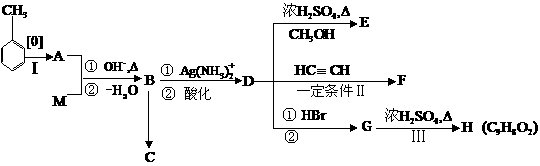
(1)写出有机物的结构简式:M ,H ,
(2)反应II的类型为: ;D→G的条件②是
(3)完成化学方程式:
B的银镜反应:
(4)F与G都能作为单体形成高分子化合物。F在一定条件下通过加聚反应生成高聚物的链节的结构简式可能为 (任写一种);
G形成高聚物的结构简式为________________________________________.
(5)在G的多种同分异构体中,满足以下条件的同分异构体共有 种
①不可使FeCl3溶液显色 ②能与Na反应放出H2 ③水解产物可发生银镜反应
④苯环上只有两个侧链且苯环上的一卤代物只有两种;
26.(14分)下图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的HCl溶液、CuSO4溶液和K2SO4溶液,电极均为石墨电极。
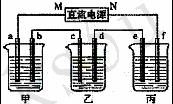
(1)接通电源后,观察到甲中b电极上产生刺激性气味气体。据此回答问题:
① 电源的N端为 极;
② 电极c上的现象为________________________________________________;
③ 电极f上的电极反应式为 ;
④ 乙中加入_______________________,可使其恢复至原溶液。
(2)若丙中盛装19g质量分数为10%的K2SO4溶液,当电极b上产生的刺激性气味气体在标准状况下的体积为11.2L时,则丙中质量分数变为: ;(过程中无晶体析出)
(3)如果乙装置电解过程中铜全部析出,此时电解能否继续进行,_______________。为什么? 。
13.人们通常把拆开1mol化学键所吸收的能量或是形成1mol化学键所放出的能量看成该化学键的键能,某些化学键键能如下表所示,
|
化学键 |
H-H |
O=O |
H-O |
|
键能/kJ·mol-1 |
436 |
497 |
463 |
下列叙述正确的是 ( )
A.2H2(g)+O2(g)===2H2O(g);ΔH=+483 kJ·mol-1
B.H2(g)+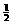 O2(g)===H2O(g);ΔH=-241.5kJ·mol-1
O2(g)===H2O(g);ΔH=-241.5kJ·mol-1
C.2H2(g)+O2(g)===2H2O(g);ΔH=+470kJ·mol-1
D.2H2(g)+O2(g)===2H2O(g);ΔH=-470kJ·mol-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com