
题目列表(包括答案和解析)
21.(12分)A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大。A原子核内无中子;A和E、D和F分别同主族,且B与D最外层电子数之比为2:3。试回答下列问题:
(1)E元素在周期表中的位置是 ;
(2)已知101KPa时,A单质的燃烧热为285。8kJ/m01,请写出A单质完全燃烧生成液态水时的热化学方程式: ;
(3)E单质在足量D单质中燃烧生成的化合物的电子式是 ;
(4)化合物X、Y均由A、D、E、F四种元素组成。
①X、Y均属于 化合物(填“离子”或“共价”):
②X与Y的水溶液相混合发生反应的离子方程式为 ;
(5)化合物E2F的水溶液中滴入双氧水和稀硫酸,加热,有单质生成。其离子反应方程式为: 。
20.关于下列图示的说法中正确的是 ( )
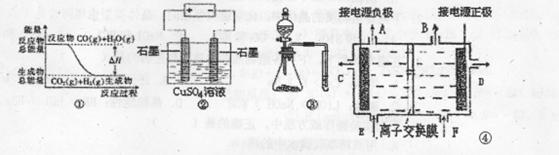
 A.图①表示可逆反应“CO(g)+H2O(g) CO2(g)+H2(g)”中的△H于0
A.图①表示可逆反应“CO(g)+H2O(g) CO2(g)+H2(g)”中的△H于0
B.图②为电解硫酸铜溶液的装置,一定时间内,两电极产生单质的物质的量之比一定为1:l
C.图③中锥形瓶内装碳酸钠固体,可用该装置比较稀硫酸、碳酸、苯酚酸性强弱
D.图④是电解饱和食盐水装置,饱和食盐水由E口进入
第Ⅱ卷(非选择题 共60分)
19.丁子香酚可做香味剂,萨罗可做消毒剂,二者的结构简式如下图所示,下列说法不正确的是 ( )
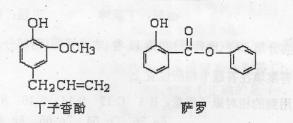
A.萨罗的分子式为C13H10O3
B.丁子香酚与浓溴水只发生取代反应
C.萨罗和丁子香酚均能发生氧化反应
D.丁子香酚和萨罗均能与氯化铁溶液发生显色反应
18. 己知298K时反应2SO2(g)+O2(g) 2SO3(g);△H=-197 kJ·mol-1,在相同温度下向一固定体积的密闭容器中加入2 mol SO2和1 mol O2,达化学平衡时放出热量为a1 kJ;向同样的另一容器中通入1 mol SO2和0.5 mol O2,达化学平衡时放出热量为 a2kJ,则下列关系式中正确的是 ( )
己知298K时反应2SO2(g)+O2(g) 2SO3(g);△H=-197 kJ·mol-1,在相同温度下向一固定体积的密闭容器中加入2 mol SO2和1 mol O2,达化学平衡时放出热量为a1 kJ;向同样的另一容器中通入1 mol SO2和0.5 mol O2,达化学平衡时放出热量为 a2kJ,则下列关系式中正确的是 ( )
A.2a2=a1>197 B.2a2>a1>197 C.2a2<a1<197 D.2a2=a1=197
17.一定条件下,体积为2L的密闭容器中,1mol A和1m01 B进行反应:
 A(g)+3B(g) 2C(g)
经2分钟反应达到平衡,此时生成0.2mol C。
A(g)+3B(g) 2C(g)
经2分钟反应达到平衡,此时生成0.2mol C。
下列说法正确的是 ( )
A.反应开始至2分钟时,以B浓度变化表示的反应速率为0.05mol/(L.min)
B.反应开始至2分钟时,A的转化率为5%
C.若其他条件不变,升高温度,A的体积分数增大,则该反应的△H<0
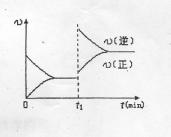
D.若其他条件不变,增大压强,化学反应速率的变化符合右侧示意图
16.下列实验能达到预期目的的是 ( )
|
编号 |
实验内容 |
实验目的 |
|
A |
将SO2通入溴水,溴水褪色后加热观察能否恢复原色 |
验证SO2漂白的可逆性 |
|
B |
将氯水加入淀粉KI溶液中 |
验证C1的非金属性比I强 |
|
C |
把铁块和铜块用导线连接插入浓硝酸中 |
组成原电池验证Fe比Cu活泼 |
|
D |
加热氯化铵和碘单质的固体混合物 |
分离除去碘单质 |
15.在25℃时,用铂电极电解一定量的Na2SO4饱和溶液。一段时间后,电极上转移的电子为2m mol,同时溶液中析出n g Na2SO4·10H2O。如果在这一过程中温度不变,则此时Na2SO4溶液中溶质的质量分数为 ( )
A.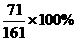 B.
B.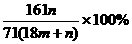
C.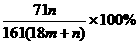 D.
D.
14.用铂作电极电解500 mL含KN03和Cu(NO3)2的混合溶液一段时间后,在两极均生成11.2L标准状况下的气体,原溶液中Cu2+的物质的量浓度为 ( )
A.0.5 mol/L B.l mol/L C.2 mol/L D.无法确定
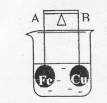
13.杠杆AB两端通过导线分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡(如下图),小心地向烧杯中央滴入浓CuSO4溶液,著反应一段时间。下列判断正确的是(不考虑实验过程中导线的反应及两球浮力的变化)( )
|
选项 |
杠杆材料 |
 杠杆偏向 杠杆偏向 |
|
|
绝缘体 |
A端高B端低 |
|
|
绝缘体 |
仍保持平衡 |
|
|
导体 |
A端高B端低 |
|
|
导体 |
A端低B端高 |
12.下列有关钢铁腐蚀与防护的说法正确的是 ( )
A.钢管与电源正极连接,钢管可被保护
B.铁遇冷浓硝酸表面钝化,可保护内部不被腐蚀
C.钢管与铜管露天堆放在一起时,钢管不易被腐蚀
D.钢铁发生析氢腐蚀时,负极反应是Fe一3e-=Fe3+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com