
题目列表(包括答案和解析)
20.将一定质量的镁和铝混合物投入200 mL硫酸中,固体全部溶解后,向所得溶液
中加入NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如
右图所示。则下列说法不正确的是 ( )
 A.镁和铝的总质量为9 g
A.镁和铝的总质量为9 g
B.最初20 mLNaOH溶液用于中和过量的硫酸
C.硫酸的物质的量浓度为2.5 mol·L–1
D.生成的氢气在标准状况下的体积为11.2 L
第Ⅱ卷(非选择题 共40分)
19.铜虽既不和稀硫酸反应,也不与硝酸盐反应,但可溶于其混合溶液。现有1.7克
NaNO3固体,加入到30mL 2mol/L的硫酸中,则该混合溶液最多可溶解铜的物质
的量为: ( )
A. 0.225mol B. 0.045 mol C. 0.02 mol D.0.03 mol
18.向Fe、FeO和Fe2O3组成的混合物中加入100mL 2mol/L的盐酸,混合物恰好完全溶解,放出448mL气体(标况),此时溶液中无Fe3+。则下列判断正确的是:
A.混合物中三种物质反应时消耗盐酸的物质的量之比为1:1:3
B.反应后所得溶液中的Fe2+和Cl–的物质的量之比为1:3
C.混合物中,FeO的物质的量无法确定,但Fe比Fe2O3的物质的量多
D.混合物中,Fe2O3的物质的量无法确定,但Fe比FeO的物质的量多
17.在t℃时,将a gNH3完全溶解于水,得V mL饱和溶液,测得该溶液的密度为ρg/cm3,质量分数为ω,其中n(NH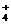 ) 为b mol。则下列叙述中错误的是( )
) 为b mol。则下列叙述中错误的是( )
A.溶液中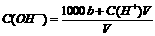 mol/L
mol/L
B.溶质的物质的量浓度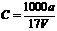 mol/L
mol/L
C.溶质的质量分数: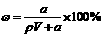
D.上述溶液中再加入V mL水后,所得溶液的质量分数小于0.5ω
16.向一定量的K2CO3溶液中缓慢滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液
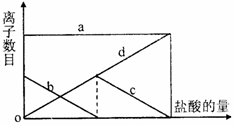 中离子数目也相应地发生变化。如图所示,四条曲线与溶液中的离子的对应关系,
中离子数目也相应地发生变化。如图所示,四条曲线与溶液中的离子的对应关系,
完全正确的是 ( )
|
|
a |
b |
c |
d |
|
A |
Cl- |
K+ |
CO32- |
HCO3- |
|
B |
K+[来源:高&考%资*源#网] |
CO32- |
Cl- |
HCO3- |
|
C |
K+ |
CO32- |
HCO3- |
Cl- |
|
D |
K+ |
HCO3- |
Cl- |
CO32- |
15.在一定条件下,把2.3克的Na分别投入1000 mL pH=2的硫酸、盐酸和醋酸中,
产生氢气的体积分别为V1、V2 、V3,则下列关系中正确的是: ( )
A. V1>V2>V3 B. V1=V2=V3 C. V1=V2 >V3 D. V1=V2 <V3
14.氯化铜(CuCl2·2H2O)中含FeCl2杂质。为制得纯净氯化铜晶体,首先将其制成水溶
液,然后按下面所示操作步骤进行提纯.
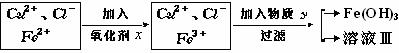
↓蒸发结晶
CuCl2·2H2O(纯)
氧化剂x与物质Y的化学式分别是(已知完全成氢氧化物所需pH值:Fe3+为3.7,Cu2+为6.4,Fe2+为9.6。) ( )
A.H2O2、CuO B.KMnO4、Na2O C.NaClO、Cu(OH)2 D.K2Cr2O7、NaOH
13.下列各组物质相互混合进行反应,既有气体生成最终又有白色沉淀生成的是( )
A.金属钠投入CuSO4溶液中 B.过量的NaOH溶液和明矾溶液反应
C.少量电石投入过量的NaHCO3溶液中 D.金属铝投入KOH溶液中
12.钾是活泼的碱金属,钾和氧气反应时可以生成氧化钾(K2O)、过氧化钾(K2O2)
和超氧化钾(KO2)等多种化合物,现将钾与氧气在一定条件下的反应产物1.1g溶
于水,所得溶液用0.5mol/L的HCl溶液进行滴定,终点时消耗HCl溶液40.00mL,
则钾与氧气反应产物的成份可能是 ( )
A.K2O B.KO2 C.K2O和K2O2 D.K2O和KO2
11.将一小块钠投入饱和NaOH溶液中,充分反应后恢复到原来温度,下列叙述中不
可能的是: ( )
A.NaOH溶液浓度增大,并放出H2 B.溶液质量减小,并放出H2
C. 溶液的pH不变 D.钠熔成小球并在液面上游动。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com