
题目列表(包括答案和解析)
5.下列各组物质相互混合后,最终既有气体生成又有沉淀生成的是( )
①Al投入NaOH溶液 ②Na投入CuSO4溶液 ③Ba(OH)2溶液和(NH4)2CO3溶液共热④过量Na2O2加入AlCl3溶液 ⑤少量电石投入Na2CO3溶液 ⑥镁投入NH4Cl溶液
A.①②③ B.②③⑤ C.②④④ D.④⑤⑥
4.下列除杂质的操作中不正确的是( )
A.铁粉中混有铝粉:加入过量烧碱溶液充分反应后过滤
B.FeCl2溶液中混有FeCl3:加入过量铁粉充分反应后过滤
C.Na2CO3固体中混有少量NaHCO3:加入适量NaOH溶液
D.Al(OH)3中混有Mg(OH)2:加入足量烧碱溶液后过滤,向滤液中通入过量CO2后过滤
3.下列物质存放方法错误的是( )
A.铝片长期放置在不密封的纸盒里
B.碳酸钠溶液盛放在带磨口玻璃塞的细口瓶中
C.FeSO4溶液存放在加有少量铁粉的试剂瓶中
D.金属钠存放于煤油中
2.金属及其化合物生产和日常生活中有着重要的应用。下列有关金属及其化合物的说法不正确的是( )
A.明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
B.目前我国流通的硬币是由合金材料制造的
C.MgO的熔点很高,可用于制作耐高温材料
D.生铁、普通钢和不锈钢中的碳含量依次增加
1.2007年诺贝尔化学奖授予德国化学家格哈德·埃特尔是因为他在表面化学所作的研究。以下事实或现象与表面化学无密切关系的是( )
A.配制FeCl3溶液时将FeCl3固体溶于浓盐酸中再加水稀释
B.用还原性铁粉和石棉绒的混合物与水蒸气反应制得Fe3O4和H2
C.在水处理过程中用明矾来作净水剂
D.将铝箔在酒精灯火焰上灼烧时熔化的铝不易滴落下来
25.(8分)某合金铜和铁的物质的量均为0.3mol ,将其全部投入bmL 4mol·L-1的
HNO3溶液中,使其充分反应(假设NO是唯一的还原产物)。
⑴若金属有剩余,其质量为m1g ,在溶液中再滴入稀硫酸后,剩余金属为m2g ,
则m1与m2的关系为:m1 m2 (填“>”“<”“=”)。
⑵若b=450,则溶液中的阳离子为: 。
⑶若合金与硝酸恰好反应完全,求b的取值范围(要计算过程)。
24. (12分)铝镁合金已成为轮船制造、化工生产等行业的重要材料。研究性学习小组的三位同学,为测定某含镁3%-5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列三种不同实验方案进行探究。填写下列空白。
[探究一]实验方案:铝镁合金 测定剩余固体质量
测定剩余固体质量
实验中发生反应的化学方程式是
实验步骤:
(1)称取5.4g铝镁合金粉末样品,投入VmL 2.0mol·L-1NaOH溶液中,充分反应。NaOH溶液的体积V≥
(2)过滤、洗涤、干燥、称量固体。该步骤中若未洗涤固体,测得镁的质量分数将 (填“偏高”或“偏低”)。
 [探究二]实验方案:铝镁合金
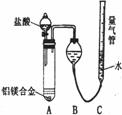
[探究二]实验方案:铝镁合金 测定生成气体的体积。实验装置如右图:
测定生成气体的体积。实验装置如右图:
问题讨论:
(1)某同学提出该实验装置不够完善,应在A、B之间添加一个干燥、除酸雾的装置。你的意见是: (填“需要”或“不需要”)。
 (2)为使测定结果尽可能精确,实验中应注意的问题是(写出两点):
(2)为使测定结果尽可能精确,实验中应注意的问题是(写出两点):
① ② 。
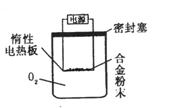
[探究三]实验方案:称量x g铝镁合金粉末.放在如右图所示装置的惰性电热板上,通电使其充分灼烧。 问题讨论:
(1)欲计算Mg的质量分数,该实验中还需测定的数据是 。(2)若用空气代替O2进行实验,对测定结果是否有影响? (填“是”或“否”)。
[实验拓展]参照探究一、探究二实验方案,请你另设计一个实验方案,测定该铝镁合金中镁的质量分数。
。
23.(10分)A-L是由6种短周期元素且成的物质,各物质之间有如下转化关系:

已知:
(a)C、E是气体单质,E是一种理想的清洁能源,F是日常生活中的常用金属;
(b)J是能使澄清石灰水变浑浊的无色无味气体;
(c)化合物A、D、I、L的焰色反应显黄色;
(d)白色沉淀K既溶于H溶液,又能溶于D溶液;
(e)反应①是工业上生产D和C的重要方法
请回答下列问题:
(1)写出F的化学式: ,D的电子式: ,B形成晶体时属于 晶体
(2)写出下列有关反应的化学方程式:
反应①: ;
反应②:
(3)G溶液呈 性(填“酸”、“碱”或“中”),请用离子方程式表示其原因:
22. (6分)化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该种有害物质。例如:

(l)在上述的步骤中,需用还原剂的是 ,需用氧化剂的是 (填编号)。
(2)在上述循环中,既能与强酸反应又能与强碱反应的两性物质是 (填化学式)
(3)完成并配平步骤①的化学方程式,标出电子转移的方向和数目:
Na2Cr2O7+□KI+□HCl→□CrCl3+□NaCl+□KCl+□I2+□
21.(4分)以下各种溶液不用任何外加试剂,就能实现鉴别的是____________________
(1)Al(NO3)3 FeCl3 NaOH FeSO4 NaHCO3
 (2)Na2CO3 BaCl2 AgNO3 Na2SO4 NH3·H2O
(2)Na2CO3 BaCl2 AgNO3 Na2SO4 NH3·H2O
(3)KOH NaCl NaHCO3 MgSO4 KNO3
(4)CuSO4 KHSO4 NaHCO3 KOH
(5)NaAlO2 Na2SiO3 Na2CO3 NaHSO4 NaCl
(6)NH4Cl Na2SO4 (NH4)2SO4 Ba(OH)2 AlCl3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com