
题目列表(包括答案和解析)
6.下列离子方程式正确的是
A.向NaHCO3溶液中加入足量的澄清石灰水:HCO3-+OH-+Ca2+=CaCO3↓+H2O
B.氨水吸收少量的二氧化硫:NH3·H2O+SO2=NH4++HSO3-
C.向AgCl悬浊液中加入饱和NaI溶液反应的离子方程式:Ag++I-=AgI↓
D.用稀硝酸溶解 FeS固体:FeS+2H+=Fe2++H2S↑
5.将铁、铝、硅的混合物分为等质量的两份,一份跟足量的NaOH溶液反应,另一份跟足量稀H2SO4反应,最终产生的H2一样多,则铁与硅物质的量之比为( )
A.2∶1 B.4∶1 C.1∶1 D.3∶1
4.下列物质反应后一定有+3价铁生成的是( )
①过量的Fe与Cl2反应;
②Fe与过量稀H2SO4反应后,再向其中加KNO3;
③Fe(NO3)2溶液中加少量盐酸;
④Fe和Fe2O3的混合物溶于盐酸中。
A.只有①② B.只有②③ C.只有①②③ D.全部
3.随着卤素原子半径的增加,下列递变规律正确的是( )
A.单质的熔沸点逐渐降低 B.卤素离子的还原性逐渐增强
C.气态氢化物的稳定性逐渐增强 D.单质的氧化性逐渐增强
2.下列说法不正确的是( )
A.食品添加剂种类很多,其中的一种为苯甲酸钠,但它不是苯的同系物
B.氮化硅(Si3N4)是一种新型无机非金属材料,可用来制作轴承、陶瓷柴油机等
C.低碳生活已成为人们的共识。因而从碳原子数考虑,提倡使用聚乙烯(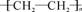 )
)
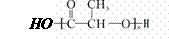
塑料生产生活制品,少使用或不使用聚乳酸酯( )绿色塑料生活制品
D.侯氏制碱法是利用NaHCO3的溶解度较小,先制得NaHCO3,再利用其热不稳定性分解制得纯碱
1.下列变化一定属于化学变化的是( )
①导电 ②爆炸 ③缓慢氧化 ④品红褪色 ⑤无水硫酸铜由白变蓝 ⑥工业制O2 ⑦白磷转化为红磷 ⑧久置浓硝酸变黄
A.②③④⑦⑧ B.③⑤⑦⑧ C.②③⑥⑦ D.④⑤⑦⑧
22.(10分)NaHCO3在潮湿的空气中会缓慢分解,Na2CO3会吸收空气中的水分:
Na2CO3+nH2O=Na2CO3·nH2O(n为平均值,n≤10)。取没有妥善保管已部分变质的NaHCO3样品A 9.16g,溶于水配成溶液,慢慢滴入稀盐酸并不停地搅拌,加入盐酸的体积与生成的CO2的体积(标准状况)如下表。(不考虑CO2气体在水中的溶解)
|
盐酸体积(mL) |
8 |
15 |
20 |
50 |
x |
120 |
150 |
|
生成CO2体积(mL) |
0 |
112 |
224 |
896 |
2240 |
2240 |
2240 |
试求:
(1)当加入盐酸后,生成CO2体积不再增加时,x的最小值为 。
(2)未变质前NaHCO3的质量。
(3)部分变质后样品A中的成分及各成分的物质的量。
21.(10分)A、B、C、D、E、F六种常见的单质或化合物在一定条件下有如下图所示的相互转化关系,所有反应物和生成物均已给出。
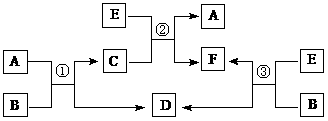
(1)若B在常温下为液态;C是一种有磁性的化合物;E是一种无色、无味的有毒气体。则反应③的化学方程式______________。
(2)若B由两种元素组成,其简单离子的电子层结构相同;绿色植物的光合作用和呼吸作用可实现自然界中D、E的循环。则B的电子式为_________________,11.6gA和E组成的混合气体与足量的B固体反应,固体增重3.6g,则A、E混合气中E 的体积分数为_________________________。
(3)若A和E都是第四周期常见的金属单质,其余都是常见的盐,反应①②③都在溶液中进行,则B、C、F氧化性由强到弱顺序为(用离子符号表示)_________________。
20. (12分)同学们利用右图装置探究SO2与Na2O2的反应。
(12分)同学们利用右图装置探究SO2与Na2O2的反应。
(1)同学们认为该反应类似CO2与Na2O2的反应,有氧气生成,当通入气体后,如果把带火星的木条伸到导管口,预期现象为带火星的木条复燃。可是,当他们把带火星的木条伸到导管口后,木条并没有复燃,你分析其原因是 ,改进的方法是 。
(2)反应完毕后,硬质玻璃管中的固体变为白色。大家认为固体成分有多种可能:
假设Ⅰ:全部为Na2SO3; 假设Ⅱ:为Na2SO3和Na2O2 的混合物;
假设Ⅲ:全部为 ; 假设Ⅳ:为Na2SO3 和Na2SO4的混合物;
假设Ⅴ:为Na2O2和Na2SO4的混合物。
假设Ⅲ、Ⅳ、Ⅴ的共同理由是 。
(3)现有下列实验用品:几支试管、带胶塞的导管(单孔)、滴管、药匙、品红溶液、蒸馏水、Ba(NO3)2溶液、BaCl2溶液、稀硫酸、稀盐酸、稀硝酸、浓硫酸、浓盐酸、浓硝酸,请你从中选出合适的用品对“假设Ⅳ”进行验证,完成下表(可以不填满):
|
实验步骤编号 |
实验操作 |
预期现象和结论 |
|
① |
,用药匙取少量白色固体于试管中。 |
 |
|
② |
向①的试管中加入
,塞紧带导管的胶塞,并将导管
。 |
|
|
③ |
|
|
|
④ |
|
|
19.(12分)
I.下列操作一定会导致实验结果偏高的是________________
A、用pH试纸测定某氯化物溶液pH时,先用蒸馏水湿润试纸
B、在测定硫酸铜晶体结晶水含量实验中,晶体尚呈淡蓝色就停止加热
C、用25℃代替标准状态,测定气体的摩尔体积
D、中和热测定实验中,用60mL0.55 mol·L-1NaOH与60mL0.50 mol·L-1盐酸反应代替教材中50mL0.55 mol·L-1NaOH与50mL0.50 mol·L-1盐酸反应,所测定中和热的数值
E、用盐酸滴定NaOH实验中,锥形瓶中有少量水就开始装NaOH,所测NaOH浓度
G、配制一定物质的量浓度溶液时,定容时仰视读数,所得溶液的浓度
H、在80mL水中加入18 mol·L-1的硫酸20mL,配制3.6mol·L-1的硫酸溶液
II.现有下列仪器或用品:a.铁架台(含铁圈、铁夹)b. 锥形瓶 c.滴定管 d.烧杯(若干)e.玻璃棒 f.胶头滴管 g.托盘天平(含砝码) h.滤纸 i.量筒 j.漏斗 k.温度计
现有下列试剂:A、NaOH固体 B、碳酸钠溶液 C、氯化镁溶液 D、蒸馏水
试填空:
 (1)如图分别是温度计、量筒、滴定管的一部分,下述判断及读数(虚线刻度)不正确的是__________________。
(1)如图分别是温度计、量筒、滴定管的一部分,下述判断及读数(虚线刻度)不正确的是__________________。
A、①是量筒,读数为1.5mL B、②是量筒,读数为2.5mL
C、③是滴定管,读数为2.50mL D、②是温度计,读数是2.5℃
(2)若要进行上述(I)中H操作,还缺少的仪器是________。
(3)除去固体Mg(OH)2中混有的少量Ca(OH)2,可选用的试剂是:________(选填序号),操作方法是_______________、洗涤。完成上述操作,上述仪器或用品用到的有__________(从上述仪器或用品中选择,并填上相应序号)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com