
题目列表(包括答案和解析)
20.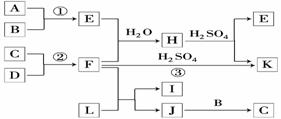 (8分)如图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去).
(8分)如图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去).
已知:
(a)A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体.
(b)反应①、②是化工生产中的重要反应.
(c)化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥.
(d)化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得.
(e)化合物J由两种元素组成,其相对分子质量为32.
请按要求填空:
(1)反应③的化学方程式_______________________________________________.
(2)C的结构式__________________________;H的化学式____________________.
(3)L的溶液与化合物E反应的离子方程式:____________________________.
(4)化合物J的化学式____________________.
19.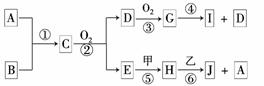 (8分)已知:A、B为常见的非金属单质且均为气体;甲、乙为金属单质,乙在I的浓溶液中发生钝化;C、H、J的溶液均呈碱性.各物质间的转化关系如下(部分生成物未给出,且未注明反应条件):
(8分)已知:A、B为常见的非金属单质且均为气体;甲、乙为金属单质,乙在I的浓溶液中发生钝化;C、H、J的溶液均呈碱性.各物质间的转化关系如下(部分生成物未给出,且未注明反应条件):
(1)写出反应②的化学方程式_________________________________________
(2)反应④中每消耗1 mol G,转移电子的物质的量为______________.
(3)反应⑥的离子方程式是___________________________________________.
(4)实验室中保存I的方法是____________________________________________.
18.(6分)A、B、C、D、E为短周期的五种元素,它们原子序数依次递增,B是构成有机物的主要元素;A与C可形成10电子化合物W,它可使紫色石蕊试液变蓝;D元素的原子最外层电子数是其次外层电子数3倍;E是同周期元素中原子半径最大的元素;A、B、C、D可形成化合物X,在X晶体中阳离子与阴离子个数比为1∶1;A、D、E可形成化合物Y。A、C、D可形成离子化合物Z。
回答下列问题:
(1)Y的电子式: ;W的空间构型: ;
(2)写出Z的水溶液中各离子浓度由大到小的顺序: ;
(3)写出常温下X与足量的Y在溶液中反应的离子方程式: 。
17.(10分)硅和氮均是自然界含量丰富的元素,其单质及其化合物在环境、能源及材料科学中有着重要影响和广泛应用.试回答下列问题:
(1)向大气中排放NOx可能导致的环境问题有____________________.(答两点)已知足NaOH溶液能完全吸收NO2生成氮的含氧酸盐.试写出该反应的离子方程式___________________.
(2)光导纤维的作用,让人们的生活更加丰富精彩,____________是制备光导纤维的基本原料.
(3)氮化硅陶瓷是一种新型无机非金属材料,其化学式为__________,可由硅粉(用Al2O3和Y2O3作助剂)在氮气中高温烧结而成,氮气在反应中既是反应物,同时又起了______________作用.由于使用的硅粉表面含二氧化硅,在反应中需加入碳粉.在烧结过程中,二氧化硅、碳、氮气以物质的量之比3∶6∶2反应生成两种化合物,该反应的化学方程式为___________________________________.
(4)硅燃烧放出大量热量,“硅能源”有望成为二十一世纪的新能源.与“氢能源”比较“硅能源”具有________________________________等更加优越的特点,从而得到全球的关注和期待.
16.将一定量的钠铝合金置于水中,合金全部溶解,得到20 mL pH=14
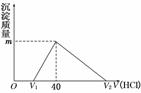 的溶液,然后用1
mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关
的溶液,然后用1
mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关
系如图所示,则下列选项正确的是 ( )
A.原合金质量为0.92 g
B.标准状况下产生氢气896 mL
C.图中m值为1.56 g
D.图中V2为60 mL
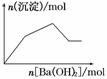
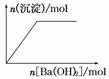
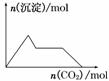
15.下列示意图与对应的反应情况正确的是 ( )
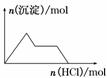
A B C D
A.含0.01 mol KOH和0.01 mol Ca(OH)2的混合溶液中缓慢通入CO2
B.NaHSO4溶液中逐滴加入Ba(OH)2溶液
C.KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液
D.NaAlO2溶液中逐滴加入盐酸
14.1.92 g Cu投入到一定量的浓HNO3中,Cu完全溶解,生成气体颜色越来越浅,共收集到标准状况下672 mL气体,将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的O2,恰好使气体完全溶于水,则通入O2的体积为 ( )
A.504 mL B.336 mL C.224 mL D.168 mL
13. X、Y、Z、W有如图所示的转化关系,则X、W可能是 ( )
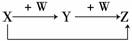
①C、O2 ②AlCl3、NaOH ③Fe、HNO3 ④S、O2
A.①②③ B.①② C.③④ D.①②③④
12.青海昆仑玉被定为2008年北京奥运会奖牌用玉,昆仑玉主要成分是由“透闪石”和“阳起石”组成的纤维状微晶结合体,透闪石(Tremolite)的化学成分为Ca2Mg5Si8O22(OH)2.下列有关说法不正确的是 ( )
A.透闪石的化学式写成氧化物的形式为: 2CaO·5MgO·8SiO2·H2O
B.透闪石中Mg元素的质量分数是Ca元素质量分数的1.5倍
C.1 mol Ca2Mg5Si8O22(OH)2与足量的盐酸作用,至少需要14 mol HCl
D.透闪石是一种新型无机非金属材料,难溶于水
11.下列关于实验中颜色变化的叙述正确的是 ( )
A.将二氧化硫通入品红溶液中,溶液显红色,加热后变为无色
B.向溶液中加入新制氯水,再滴加KSCN溶液,若溶液变红色,则证明溶液中一定含
有Fe2+
C.将湿润的红纸条放进盛有氯气的集气瓶中,红纸条褪色
D.用标准高锰酸钾溶液滴定Na2SO3溶液,终点时溶液由紫色变为无色
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com