
题目列表(包括答案和解析)
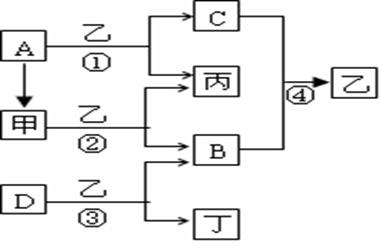
27.(12分)已知A、B、C、D为常见单质,其中B、C、D常温常压下为气体,甲、乙、丙、丁为常见的化合物,乙常温下为液体,丙的焰色反应为
黄色,右图为各种物质之间的转化关系。请回答下列问题:
(1)写出下列物质的化学式:A ,B ,D 。
(2)甲的电子式为 ,反应②中若有11.2L(标准状况下)B生成,则发生转移的电子的物质的量为 。
(3)写出反应③的离子方程式: 。
四:计算
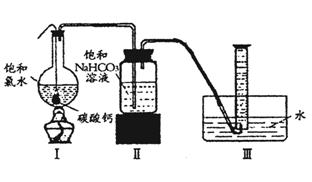 在圆底烧瓶底部,有一用塑料网包住的过量块状碳酸钙和150mL饱和氯水,按如图所示装置实验,待不再产生气泡后,将塑料网中剩余的石灰石提出液面,密封后再加热、煮沸烧瓶中的液体,直到量筒中的气体不再增加(不考虑HClO的分解)。
在圆底烧瓶底部,有一用塑料网包住的过量块状碳酸钙和150mL饱和氯水,按如图所示装置实验,待不再产生气泡后,将塑料网中剩余的石灰石提出液面,密封后再加热、煮沸烧瓶中的液体,直到量筒中的气体不再增加(不考虑HClO的分解)。
请回答:
(3)为减少用装置Ⅲ收集气体过程中CO2因溶解而造成的损失,且水槽中仍然为水,请你对装置Ⅲ进行改进,最简单的方法是
。
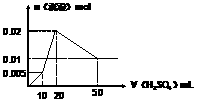
(4)用改进后的装置进行上述实验,测得塑料网内的碳酸钙质量减少Ag,总共收集到标准状况下的CO2气体BL,发现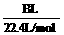 明显小于
明显小于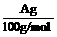 。若不考虑实验操作和CO2的溶解等因素造成的误差,从化学反应原理来看,导致这一大小关系的原因是____________
。若不考虑实验操作和CO2的溶解等因素造成的误差,从化学反应原理来看,导致这一大小关系的原因是____________
。
(5)实验后发现,装置Ⅱ中的液体增多了,其原因是________ ________ 。
三:推断题
26、(16分)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M原子最外层电子数与次外层电子数之比为3∶4;N-、Z+、X+离子的半径逐渐减小;化合物XN常温下为气体。据此回答:
(1)M、N的最高价氧化物的水化物中酸性较强的是(写出化学式) 。
(2)Z与M可形成常见固体化合物C,用电子式表示C的形成过程 。
(3)已知通常状况下1g X2在Y2中完全燃烧放出a kJ的热量,请写出表示X2燃烧热的热化学方程式 。
(4)X与Y、X与M均可形成18电子分子,这两种分子在水溶液中反应有黄色沉淀生成,写出该反应的化学方程式 。
(5)化合物A、B均为由上述五种元素中的任意三种元素组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比为1∶1∶1,A溶液中水的电离程度比在纯水中小。则化合物A中的化学键类型为 ;若B为常见家用消毒剂的主要成分,则B的化学式是 。
(6)均由X、Y、Z、M四种元素组成的两种盐发生反应的离子方程式是 ;其中一种是强酸所成的酸式盐,写出Ba(OH)2溶液中逐滴加入该盐溶液至中性的离子方程式 。
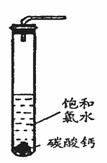 ①在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,有少量气泡产生,溶液浅黄绿色褪去;
①在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,有少量气泡产生,溶液浅黄绿色褪去;
②过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强;
③为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体;
将第三份加热,看到溶液变浑浊且有大量无色气体产生。
经检测,上述实验中产生的无色气体均为CO2。
请回答:
(1)反应后所得的溶液漂白性增强的原因是______ ___________ ____ ________ 。
(2)依据上述实验可推知:②的滤液中的溶质除CaCl2、HClO外,还含有______ __ _ 。
24、(1) Al(OH)3 + OH-=[Al(OH)4] - (2)0.5mol/L(3)30.8%
(4)(5)1.07g (5)
23、(1)除去水蒸汽 除去CO2 (2)氧化铜(CuO)
CuO+H2=Cu+H2O CuO+CO=Cu+CO2 (3)无水硫酸铜(CuSO4) 检验 H2O
(4)(g-ab)-kj-hi-cd(或dc)-fe-lm (5)原混合气中中的CO2已被除去,其中CO与CuO反应生成的CO2使澄清石灰水变混浊。
(6)原混合气中的H2O已被除去,其中H2与CuO反应生成的H2O使无水硫酸铜由白色变为蓝色
22、(1)SO42-、Al3+、Fe2+、NH4+ Fe3+ ⑤
(2)NH3 Fe(OH)3 Al(OH)3 气体由无色变成红棕色
(3)Ba2++SO42-=BaSO4↓ 3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O
(4)4∶2∶1
21、(1)I2+5Cl2+6H2O=2HIO3+10HCl (2)KI、I2
(3)橙色;HBrO3、Cl2、HIO3
(4)2I- + ClO-+2 H+ = I2 + Cl-+ H2O
24、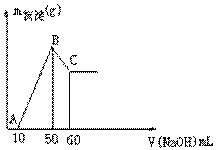 (12分)把一小块镁铝合金溶于100mL盐酸中,
(12分)把一小块镁铝合金溶于100mL盐酸中,
然后向其中滴入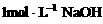 溶液,生成沉淀
溶液,生成沉淀
的质量和加入NaOH溶液的体积如右图所示。
(1)写出B--C段的离子方程式:
(2)盐酸的物质的量浓度为
(3)合金中镁的质量分数为 (4)B点沉淀的质量 。
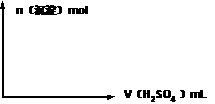 (5)若将此小块镁铝合金先加入10mL 1mol/LBa(OH)2
(5)若将此小块镁铝合金先加入10mL 1mol/LBa(OH)2
溶液中,充分反应后过滤,在滤液中逐滴滴入0.5mol/L
H2SO4,完成右边图像(横坐标表示H2SO4体积,纵坐标表
示沉淀的物质的量)。
答案:1、 D 2、C 3、B 4、B 5、D 6、C 7、C 8、B 9、C10、C 11、B 12、D 13、B14、B 15、 C 16、B 17、A 18、C 19 B 20、C
23、(15分)水蒸气通过灼热的焦炭后,流出气体的主要成分是CO和H2,还有CO2和水蒸气等。请用下图中提供的仪器,选择必要的试剂,设计一个实验,证明上述混合气体中有CO和H2。(加热装置和导管等在图中略去)
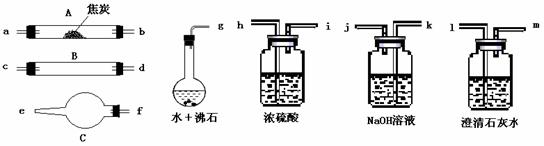
回答下列问题:
⑴ 盛浓硫酸的装置的用途是 ;
盛NaOH溶液的装置的用途是 。
⑵ 仪器B中需加入试剂的名称(或化学式)是: ,
所发生反应的化学方程式是: 。
⑶ 仪器C中加试剂的名称(或化学式)是 ,
其目的是 。
⑷ 按气流方向连接各仪器,用字母表示接口的连接顺序:
g-ab 。
⑸ 能证明混合气中含有CO的实验依据是 。
能证明混合气中含H2的实验依据是 。
22、(15分)某强酸性溶液X,含有Ba2+、Al3+、SiO32-、NH4+、Fe2+、Fe3+、
CO32-、SO42-、NO3-中的一种或几种离子,取溶液进行连续实验,能实现如下转化:
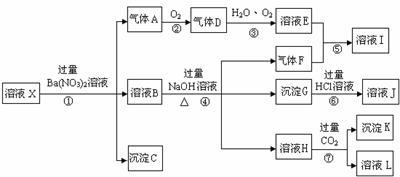
依据以上信息,回答下列问题:
(1)上述离子中,溶液X中肯定含有的是:_____________________________;不能肯定的是:_________________。对不能确定是否存在的离子,可以另取X溶液于一支试管中,选择下列试剂中的一种加入X溶液中,根据现象就可判断,则该试剂是:___________。(选填:①NaOH溶液,②酚酞试剂,③石蕊试剂,④pH试纸,⑤KSCN溶液,⑥KMnO4溶液)
(2)气体F的化学式为:_______________,沉淀G的化学式为:_____________,沉淀K的化学式为:____________,实验中,可以观察到反应②的现象是:________________。
(3)写出步骤①所有发生反应的离子方程式_________________、__________________。
(4)要使步骤③中,D、H2O、O2三种物质恰好发生化合反应,则D、H2O、O2物质的量之比是:______________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com