
题目列表(包括答案和解析)
9.三氧化二铁、氧化亚铜和铜都是红色固体。某校一化学实验小组通过实验来探究某红色固体成分。若固体粉末能完全溶解于稀硫酸且无固体存在,滴加 KSCN 试剂时溶液不变红色
(查阅资料:Cu2O是一种碱性氧化物, Cu+在溶液中不能存在 2Cu+== Cu+ Cu2+)
A. 此固体一定无三氧化二铁 B. 此固体一定是三氧化二铁和铜
C. 此固体可能是三氧化二铁和氧化亚铜 D. 此固体可能是铜和氧化亚铜
8、从海水中提取镁,可按如下步骤进行:①把贝壳制成石灰乳; ②在引入的海水中加入石灰乳,沉降、过滤、洗涤沉淀物; ③将沉淀物与盐酸反应,结晶过滤、在HCl气体氛围中干燥产物; ④将得到的产物熔融电解得到镁。下列说法不正确的是 ( )
A.此法的优点之一是原料来源丰富
B.①②③步骤的目的是从海水中提取MgCl2
C.以上提取镁的过程中涉及化合、分解和复分解反应
D.上述过程中涉及到的分解反应都是氧化还原反应
7.为了提纯下列物质(括号内为杂质),所选用的除杂试剂与分离方法都正确的是( )。
|
选项 |
不纯物质 |
除杂试剂 |
分离方法 |
|
A |
溴乙烷(乙醇) |
水 |
分液 |
|
B |
溴苯(溴) |
NaOH溶液 |
过滤 |
|
C |
Cu(NO3)2溶液(AgNO3) |
铜粉 |
结晶 |
|
D |
K2SO4(K2CO3) |
盐酸 |
蒸发 |
6.甲.乙为单质,丙 丁为氧化物,它们存在如下转变
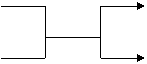 甲
丁
甲
丁
丙 乙
满足条件的乙为① Fe ② Cu ③ Al ④ C ⑤ Si
A.①② B.①④⑤ C.①②③⑤ D.①②④⑤
5.用水热法制备Fe3O4纳米颗粒的总反应如下:
3Fe2++ 2S2O32-+O2+4OH-= Fe3O4 + S4O62-+2H2O。下列说法正确的是
A.在反应中1molO2氧化了3mol Fe2+
B.还原剂是Fe2+,氧化剂是S2O32-和O2
C.每生成1mol Fe3O4,转移3mol电子
D.当转移1mol电子时,消耗56g S2O32-
4.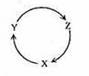 下列各组物质中,满足下图物质一步转化关系的选项是
下列各组物质中,满足下图物质一步转化关系的选项是
|
|
X |
Y |
Z |
|
A |
Na |
NaOH |
NaHCO3 |
|
B |
Cu |
CuSO4 |
Cu(OH)2 |
|
C |
C |
CO |
CO2 |
|
D |
Si |
SiO2 |
H2SiO3 |
3.过量CO2通入下列溶液最后无沉淀或固体析出的是( )
A.CaCl2与NaOH的混合溶液 B.Na2CO3饱和溶液
C. Na2SiO3溶液 D. NaAlO2溶液
2.地壳中含量第一和第二的两元素形成的化合物,不具有的性质是( )。
A.是酸性氧化物,它不溶于任何酸 B.熔点很高
C.可与纯碱反应 D.与碳在高温下反应可制取两元素中一种元素的单质
1.材料与化学密切相关,表中材料对应化学成分错误的是
|
|
材料 |
主要化学成分 |
|
A |
普通水泥、钢化玻璃 |
硅酸盐 |
|
B |
大理石、石灰石 |
碳酸钙 |
|
C |
刚玉、光导纤维 |
三氧化二铝 |
|
D |
沙子、石英 |
二氧化硅 |
21.(1)少量饱和氯化铁溶液分别滴加到如下图所示的三种物质中得到三种分散系①、②、③。试将①、②、③填入下右图方框中:
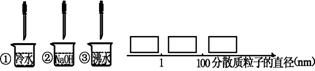
(2)在饱和氯化铁溶液中加入碳酸钙粉末,发现沉淀逐渐转变为红褐色,并产生无色气体。用离子方程式表示产生上述现象的原因 。
(3)在Fe(OH)3胶体中,逐滴加入HI稀溶液。出现的现象是:先产生红褐色沉淀,其原因是
,随后沉淀溶解,离子方程式为 。
(4)将用导线连接的碳棒和铜棒插入饱和氯化铁溶液中:碳棒( 极)反应式为
铜棒减轻3.2克导线上通过的电子总数为 。溶液的现象变化是 。
总反应的离子方程式为
班级______考 姓名______分数______
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com