
题目列表(包括答案和解析)
27、(11分)在2L密闭容器内,800℃时反应:2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
|
时间(s) |
0 |
1 |
2 |
3 |
4 |
5 |
|
n(NO(mol) |
0.020 |
0.
01 |
0.008 |
0.007 |
0.007 |
0.007 |
 (1)写出该反应的平衡常数表达式:K=
。
(1)写出该反应的平衡常数表达式:K=
。
已知: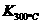 >
>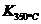 ,则该反应是 热反应。
,则该反应是 热反应。
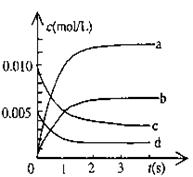
(2)右图中表示NO2的变化的曲线是 。
用O2表示从0-2s内该反应的平均速率v= 。
(3)能说明该反应已达到平衡状态的是 。
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是 。
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
26、(7分)美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电源,被称为21世纪的明星电池,其构造 如图所示:两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电。
(1)a是 极(填“正”或“负”),其电极反应式为 ,
b极的电极反应式 。
(2)某些碳氢化合物也可作为燃料电池的燃料,如天然气(甲烷)等。若将上图中H2换成CH4时,电池内总的反应方程式为 :CH4+2O2+2OH-=CO32-+3H2O。请写出a极的电极反应式 。
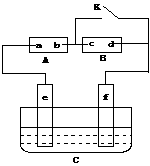
25、(8分)如图A为直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,请填空:
(1)电源A上的a为______________极
 (2)滤纸B上发生的总化学方程式为:
(2)滤纸B上发生的总化学方程式为:
________________________________
 (3)欲在电镀槽中实现铁上镀锌,接通K点,使c、d两点短路,则电极e上发生的反应为: ,电极f上发生的反应为:_____________________,槽中盛放的镀液可以是____________溶液。
(3)欲在电镀槽中实现铁上镀锌,接通K点,使c、d两点短路,则电极e上发生的反应为: ,电极f上发生的反应为:_____________________,槽中盛放的镀液可以是____________溶液。
24、(12分) 已知某溶液中只存在OH一、H+、NH4+、Cl一四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
①(Cl一)>c(NH4+)> c(H+)> c(OH-) ②c(Cl一) >c(NH4+)> c(OH-)> c(H+) ③c(NH4+)>c(Cl一)> c(OH-)> c(H+) ④ c(Cl一) >c(H+)> c(NH4+)> c(OH-) 填写下列空白: (1)由若溶液中只溶解了一种溶质,则该溶质是__________,上述四种离子浓度的大小顺序为_______________(填序号) (2)若上述关系中③是正确的,则溶液中的溶质为____________________; 若上述关系中④是正确的,则溶液中的溶质为________________________。 (3)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)___________c(NH3·H2O)(填“>”、“<”或“=” 下同),混合前酸中c(H+)和碱中c(OH-)的关系:c(H+)____________ c(OH-)。
23、(4分)发射卫星时可用肼(N2H4)为燃料,用NO2作氧化剂,两者反应生成氮气和水蒸气。已知:N2(g)+2O2(g)=2NO2(g);△H=+67.7kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-534kJ·mol-1
(1)写出肼和二氧化氮反应的热化学方程式 。
(2)又知1mol液态水气化时需吸收44kJ的热量,则16g肼和二氧化氮完全反应生成液态水时放出的热量为 kJ。
22、某研究小组研究了其他条件不变时,改变条件对以下可逆反应的影响:
2SO2(g)+O2(g) 2SO3(g);△H<0 下列说法正确的是 ( )
2SO3(g);△H<0 下列说法正确的是 ( )
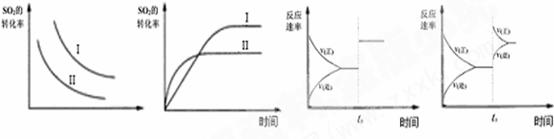
图一 图二 图三 图四
A.图一研究的是温度、压强对平衡的影响,横坐标表示压强
B.图二研究的是温度对平衡的影响,Ⅰ采用的温度更高
C.图三中t0时使用了催化剂,使平衡向正反应方向进行
D.图四中t0时增大压强,使平衡向正反应方向进行
第Ⅱ卷 非选择题(共56分)
21、某溶液中大量存在五种离子:NO3- 、SO42-、Fe3+ 、H+ 、X ,其物质的量之比为:n(NO3-) :n(SO42-) :n(Fe3+) :n(H+) :n (X) = 2 :3 :1 :3 :1,则X可能为 ( )
A.Fe2+ B. Mg2+ C.Cl- D.Ba2+
20、用石墨电极电解含有相同物质的量的Na2SO4和CuSO4的溶液。一段时间后,溶液颜色变浅。此时若要使溶液中的Na2SO4和CuSO4都恢复到电解前的浓度,应向电解后的溶液中加入适量的: ( )
A.Na2SO4和CuSO4 B.CuO C.Na2O和CuO D.H2O和CuSO4
19、在一个容积为1L的密闭容器中,加入2mol A和1mol B发生如下反应:
2A(g)+B(g)  3C(g)+D(s) 达到平衡时,C物质的物质的量浓度为1.2mol·L-1。若维持容器体积和温度不变,按下列方法改变起始物质,达到平衡时C的浓度仍为1.2mol·L-1的是( )
3C(g)+D(s) 达到平衡时,C物质的物质的量浓度为1.2mol·L-1。若维持容器体积和温度不变,按下列方法改变起始物质,达到平衡时C的浓度仍为1.2mol·L-1的是( )
A.4molA+2molB B.3molC+1molD+1molB
C.3molC+0.5molD D.1.6molA+0.8molB+0.6molC+0molD
18、盐酸、醋酸和碳酸氢钠是生活中常见的物质。下列表述正确的是 ( )
A在NaHCO3溶液中加入与其等物质的量的NaOH,溶液中的阴离子只有CO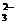 和OH-
和OH-
B.NaHCO3溶液中:C(H+)+C(H2CO3)=C(OH-)
C.10 mL0.10 mol·L-1CH3COOH溶液加入等物质的量的NaOH后,溶液中离子的浓度由大到小的顺序是:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗的NaOH物质的量相同
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com