
题目列表(包括答案和解析)
7.下列物质中,不属于合金的是( )
A.硬铝 B.黄铜 C.钢铁 D.水银
6.下列物质不能通过化合反应直接制得的是 ( ) A.FeCl2 B.NaHSO3 C.CuS D.Fe(OH)3
5.下列物质中既能跟稀H2SO4反应,又能跟氢氧化钠溶液反应的是 ( )
①NaHCO3 ②Al2O3 ③Al(OH) ④Al
A.③④ B.②③④ C.①③④ D.全部
4.将Fe,Cu,Fe2+,Fe3+和Cu2+盛于同一容器中充分反应,如Fe有剩余,则容器中只能有 ( )
A.Cu Fe3+ B.Fe2+ Fe3+ C.Cu Cu2+ Fe D.Cu Fe2+ Fe
3.为防止FeSO4被氧化变质,实验室配制FeSO4溶液时,常在溶液中加入少量的( )A.铜粉 B.铁粉 C.锌粉 D.Fe2(SO4)3
2.下列有关纯铁的描述正确的是
A、熔点比生铁的低
B、与相同浓度的盐酸反应生成氢气的速率比生铁的快
C、在潮湿空气中比生铁容易被腐蚀
D、在冷的浓硫酸中可钝化
1.铊(Tl)是某超导材料的组成元素之一,与铝同族,位于第6周期。Tl3+与Ag在酸性介质中发生反应:Tl3+ + 2Ag = Tl+ + 2Ag+ 。下列推断正确的是 ( )
A、Tl+的最外层有1个电子 B、Tl3+的氧化性比Al3+弱
C、Tl 能形成+3价和+1价的化合物 D、Tl+的还原性比Ag强
20、(12分)氯气是一种重要的化工原料。
(1)实验室可用二氧化锰和浓盐酸反应制取氯气,反应的化学方程式是 。
(2)资料显示:Ca(ClO)2+CaCl2+2H2SO4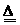 2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
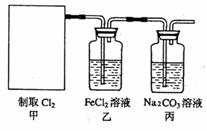
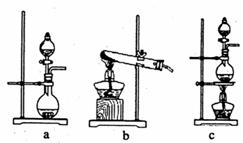
 和氢元素总的质量百分含量约为81.8%。
和氢元素总的质量百分含量约为81.8%。
(1)1个Y分子中应该有 个氧原子。
(2)X的分子式是 。
(3)G和X互为同分异构体,且具有相同的官能团,用芳香烃A合成G路线如下:
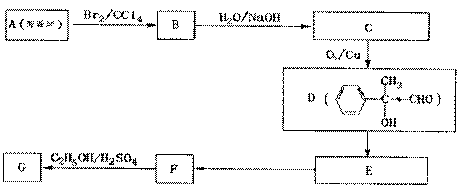
①写出A的结构简式 。
②E→F的反应类型是 反应,该反应的化学方程式为 。
③写出所有符合下列条件的F的同分异构体的结构简式: 。
i.分子内除了苯环无其他环境结构,且苯环上有2个对位取代基。
ii.一定条件下,该物质既能与银氨溶液发生银镜反应也能和FeCl3溶液发生显色反应。
19.(8分)
(1)已知:N2(g)+O2(g)=2NO(g); △H=+180.5 kJ·mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g);△H=-905 kJ·mol-1
2H2(g)十O2(g)=2H2O(g):△H=--483.6 kJ·mol-1
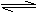 则N2(g)+3H2(g)
2NH3(g)的△H=
。
则N2(g)+3H2(g)
2NH3(g)的△H=
。
(2)在一定条件下,将2mol N2与5mol H2混合于一个10 L的密闭容器中,反应情况如图1所示:
①求5min内的平均反应速率v(NH3) ;
②达到平衡时NH3的体积分数为 。
图1 图2 电解法合成氨装置
(3)近年来科学家采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多品薄膜做电极,实现了高转化率的电解法合成氨(装置如图2)。钯电极A上发生的电极反应式是 。
17(9分)下列各图中的纵坐标表示沉淀的物质的量,横坐标表示加入x的物质的量,请将各图一一对应的反应的代号填入每图下方的括号内。
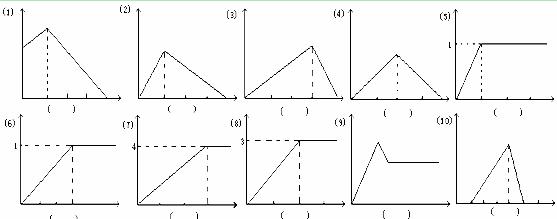
A.Ca3(PO4)2悬浊液中滴入H3PO4 B.NaAlO2溶液中通入HCl
C.Ba(OH)2溶液中通入SO2 D.石灰水中通入CO2
E.AlCl3溶液中滴入氨水 F.AlCl3溶液中滴入NaAlO2溶液
G.SO2溶液中通入H2S气体 H.稀硫酸中滴入Ba(OH)2溶液
I.AlCl3、MgSO4的混合溶液中加入过量NaOH溶液
J.在盐酸酸化的AlCl3溶液中,滴入KOH溶
K.AlCl3溶液中滴入NaOH溶液
18.(11分)原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。
(1)X元素是
(2)X与W组成的化合物中存在 键(填“离子”“共价”)。
(3)由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液能与铜反应,离子方程式为 。
(4)由X、Y、Z、W四种元素组成的一种离子化合物A
①已知1mol A能与足量NaOH浓溶液反应生成标准状况下44.8L气体。写出加热条件下A与NaOH溶液反应的离子方程式 。
②又知A既能与盐酸反应,又能与氯水反应,写出A与氯水反应的离子方程式
。
(5)由X、Y、Z、W和Fe五种元素组成的式量为392的化合物B,1 mol B中含有6mol结晶水。对化合物B进行如下实验:
a 取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体。过一段时间白色沉淀变为灰绿色,最终变为红褐色;
b 另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解
① B的化学式为 。
② 已知1 mol·L-1 100mL B的溶液能与1 mol·L-1 20mLKMnO4溶液(硫酸酸化)恰好反应。写出反应的离子方程式 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com