
题目列表(包括答案和解析)
4.从海水中提取单质镁,下列正确的途径是
A.海水Mg(OH)2Mg B.海水MgCl2Mg
C.海水Mg(OH)2MgCl2Mg D.海水MgCl2Mg
3.下列说法正确的是
A.Li、Na、K元素的原子核外电子层数随着核电荷数的增加而增多。
B.某物质灼烧时,焰色反应为黄色,该物质一定含有钠元素,不含钾元素。
C.碱金属的单质中锂的密度最小,熔点最低。
D.用电解铯盐溶液的方法冶炼金属铯。
2.下列有关物质结构的表述正确的是
 A.次氯酸的电子式
A.次氯酸的电子式 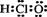 B.二氧化硅的分子式 SiO2
B.二氧化硅的分子式 SiO2
C. 碳-12原子 126C D.钠离子的结构示意图
1. 分类是化学学习和研究的常用手段。下列分类依据和结论都正确的是
A.H2O、HCOOH、Cu2(OH)2CO3均含有氧元素,都是氧化物
B.HClO、浓硫酸、HNO3均具有氧化性,都是氧化性酸
C.HF、CH3COOH、CH3CH2OH都易溶于水,都是电解质
D.HCOOH、H2CO3、H2SO4分子中均含有两个氢原子,都是二元酸
30.(15分)香豆素是一种用途广泛的香料,它可以利用乙醇和B通过以下途径合成,其中B的分子式为C7H6O2。
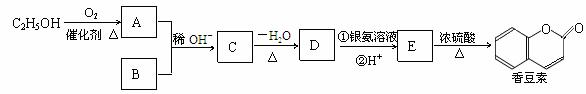
已知: 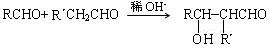 (R、R´为烃基)
(R、R´为烃基)
(1) A的名称为: ,C→D的反应类型为: ,C含有的官能团名称为: 。
(2)D的结构简式是 ;
(3)完成下列反应的化学方程式:
E在一定条件下发生加成聚合反应: ;
E→香豆素: ;
(4)B有多种同分异构体,其中苯环上只有一个侧链的所有同分异构体的结构简式是 ; (5)有关香豆素的说法正确的是 (填字母)。
a.只能与溴单质发生加成反应,不能发生取代反应
b.1 mol香豆素可与5 mol H2发生加成反应
c.1 mol香豆素可与2 mol NaOH发生反应
d.1 mol香豆素完全燃烧消耗9.5mol O2
29.(18分)实验一:某化学小组为比较盐酸和醋酸的酸性,设计了如下实验方案。装置如图:
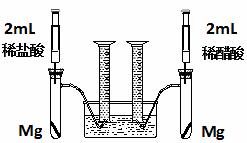 实验方案:在两试管中分别加入过量镁条,同时将两注射器中的溶液注入相应试管中,观察产生氢气的速率和体积。
实验方案:在两试管中分别加入过量镁条,同时将两注射器中的溶液注入相应试管中,观察产生氢气的速率和体积。
(1)盐酸与镁反应的离子方程式为 。
(2)在上述实验方案中有一明显欠缺,该欠缺是
。
(3)在欠缺已经改正的方案下,反应起始时,产生氢气的速率关系应是 ;最终产生氢气的体积关系应是 。
(4)实验中产生的氢气体积比理论值高,可能原因是 。
(5)通过比较起始反应的速率可以得出的结论是 。
(6)除上述方法外,还可以通过其他方法比较盐酸和醋酸的酸性,请写出其中一种更简单的方法
。
实验二:某二元酸(H2B)在水中的电离方程式是: H2B=H++HB- HB- H++B2-
H++B2-
回答下列问题:
(1)请判断H2B是强电解质还是弱电解质?
(2)已知0.1mol·L-1 NaHB溶液的pH=2,则0.1mol·L-1 H2B溶液中氢离子的物质的量浓度应 0.11 mol·L-1(填“<”,“>”或“=”)
(3)在0.1mol/L的Na2B溶液中,下列离子浓度关系式正确的是_______。
A.c(H+)+c(HB-)+c(H2B)=0.1mol/L B.c(Na+)+c(OH-)=c(H+)+ c(HB-)
C.c(Na+)+ c(H+)= c(OH-)+ c(HB-)+2c(B2-) D.c(Na+)=2c(B2-)+2 c(HB-)
(4)0.1mol/LNaHB溶液中各种离子浓度由大到小的顺序是_______________________。
28.(12分)原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。
(1)X元素是 。
(2)由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液能与铜反应,离子方程式为
。
(3)由X、Y、Z、W四种元素组成的一种离子化合物A
①已知1mol A能与足量NaOH浓溶液反应生成标准状况下44.8L气体。写出加热条件下A与NaOH溶液反应的离子方程式 。
②又知A既能与盐酸反应,又能与氯水反应,写出A与氯水反应的离子方程式
。
(4)由X、Y、Z、W和Fe五种元素组成的式量为392的化合物B,1 mol B中含有6mol结晶水。对化合物B进行如下实验:
a 取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体。过一段时间白色沉淀变为灰绿色,最终变为红褐色;
b 另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解
① B的化学式为 。
② 已知1 mol·L-1 100mL B的溶液能与1 mol·L-1 20mL KMnO4溶液(硫酸酸化)恰好完全反应。写出反应的离子方程式 。
27.(15分)硝酸是一种重要的化工原料,工业上生产硝酸的主要过程如下。
 (1)以N2和H2为原料合成氨气。反应N2(g)+3H2(g) 2NH3(g)△H<0
(1)以N2和H2为原料合成氨气。反应N2(g)+3H2(g) 2NH3(g)△H<0
①下列措施可以提高H2的转化率是(填选项序号)
 。
。
a.选择适当的催化剂 b.增大压强
c.及时分离生成的NH3 d.升高温度
②一定温度下,在密闭容器中充入1molN2和3molH2发生反应。若容器容积恒定,达到平衡状态时,气体的总物质的量是原来的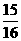 ,则N2的转化率a1=
;
,则N2的转化率a1=
;
若容器压强恒定,达到平衡状态时,N2的转化率为a2,则a2 a1(填“>”、“<”或“=”)。
(2)以氨气、空气为主要原料制硝酸。
①NH3被氧气催化氧化生成NO的反应的化学方程式是 。
 ②在容积恒定的密闭容器中进行反应2NO(g)+O2(g) 2NO2(g):△H>0
②在容积恒定的密闭容器中进行反应2NO(g)+O2(g) 2NO2(g):△H>0
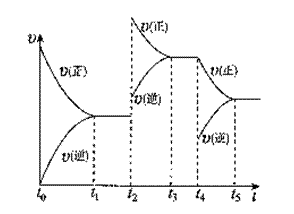 该反应的反应速率(v)随时间(t)变化的关系如右图所示。若t2、t4时刻只改变一个条件,下列说法正确的是(填选项序号)
。
该反应的反应速率(v)随时间(t)变化的关系如右图所示。若t2、t4时刻只改变一个条件,下列说法正确的是(填选项序号)
。
a.在t1~t2时,可依据容器内气体的压强保持不变判断反应已达到平衡状态;
b.在t2时,采取的措施可以是升高温度;
c.在t3~t4时,可依据容器内气体的密度保持不变判断反应已达到平衡状态;
d.在t5时,容器内NO2的体积分数是整个过程中的最大值。(3)硝酸厂常用如下2种方法处理尾气。
①催化还原法:催化剂存在时用H2将NO2还原为N2。
已知:2H2(g)+O2(g)=2H2O(g): △H=-483.6kJ/mol
N2(g)+2O2(g)=2NO2(g): △H=+67.7kJ/mol
则H2还原NO2生成水蒸气反应的热化学方程式是 。
②碱液吸收法:用Na2CO3溶液吸收NO2生成CO2。
若每9.2gNO2和Na2CO3溶液反应时转移电子数为0.1mol,则反应 的离子方程式是
。
的离子方程式是
。
13. 25°C时,下列关于分别由等体积0.1mol/L的2种溶液混合而成的溶液的说法中,不正确的是
A.Ba(OH)2溶液与Na2SO4溶液:pH=13
B.醋酸与CH3COONa溶液:c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
C.Na2CO3溶液与NaOH溶液:c(Na+)>c(CO32-)>c(OH-)>c(H+)
D.Na2CO3溶液与NaHCO3溶液:2c(Na+)=3c(CO32-)+3c(HCO3-)+3c(H2CO3)
12.足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.68 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5 mol/L NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
A.60 mL B.45 mL C.30 mL D.15 mL
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com