
题目列表(包括答案和解析)
5.下列有机物命名正确的是B
A. 2-乙基丙烷 B.CH3CH2CH2CH2OH 1-丁醇
2-乙基丙烷 B.CH3CH2CH2CH2OH 1-丁醇
C.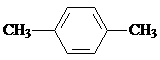 间二甲苯 D.
间二甲苯 D.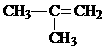 2-甲基-2-丙烯
2-甲基-2-丙烯
4.具有下列电子排布式的原子中,半径最大的是 A
A.ls22s22p63s23p2 B.1s22s22p3
C.1s22s2sp2 D.1s22s22p63s23p4
3.下列叙述正确的是 D
A.有新单质生成的化学反应,一定都属于氧化还原反应
B.在氧化还原反应中,非金属单质一定是氧化剂
C.某元素从化合态转变为游离态时,该元素一定被还原
D.金属阳离子被还原不一定得到金属单质
2.下列判断标准肯定正确的是 B
A.pH<7:溶液一定显酸性
B.氧化还原反应:一定有化合价升高和降低
C.导电能力:强电解质溶液一定大于弱电解质溶液
D.非电解质:水溶液一定不能导电
1.化学在日常生活中具有广泛的应用,下列应用中不涉及氧化还原反应原理的是 A
A.用明矾[KAl(SO4)2·12H2O]净水 B.用“84”消毒液对环境进行消毒
C.交警用CrO3检验司机是否酒后驾驶 D.医务室用双氧水消毒
25.(11分)有一混合气体,可能由H2、O2、NH3、N2、CO2、HCl和He中的两种或多种组成。常温下,取此气体200mL进行实验,实验的过程和结果如下:
(1)观察此混合气体为无色。
(2)将此气体通过浓H2SO4,气体体积减少了40mL。
(3)将(2)中剩余的气体,通过Na2O2固体,气体体积变为120mL。
(4)将(3)中剩余的气体引燃充分反应后,冷却至常温,气体体积又减少了105mL。
(5)又将(4)中剩余的气体通过炽热的铜网,气体的体积又减少了三分之一(上述气体的体积都是相同条件下测定的)。
根据上述实验,试推断:
(1)混合气体中肯定存在的气体是 ,它们的体积分别为
。
(2)混合气体中肯定不存在的气体是 。
(3)混合气体中可能含有的气体是 ,其体积共为
。
24.(11分)海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:
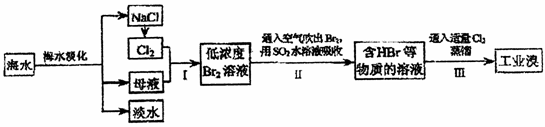
(1)从海水中可以得到食盐。为了除去粗盐中的Ca2+、Mg2+、SO2-4及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤,②加过量NaOH溶液,③加适量盐酸,④加过量NaCO3溶液,⑤加过量BaCl2溶液。正确的操作顺序是 。
A.①④②⑤③ B.④①②⑤③ C.②⑤④①③ D.②④⑤①③
(2)电解 NaCl溶液是氯碱工业的核心反应,请写出其化学方程式
。
(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为 。
(4)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为
,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是 。
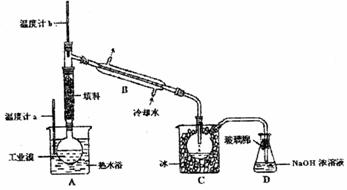 (5)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,绘制了如右装置简图,请你参与分析讨论:
(5)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,绘制了如右装置简图,请你参与分析讨论:
①整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是
。
②实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件:
。
③C中液体产生颜色为 。为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是 。
23.(8分)中学化学中几种常见物质的转化关系如下;
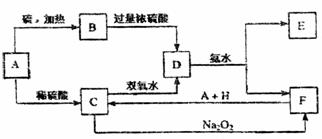
将D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:
(1)红褐色胶体F粒子直径大小的范围: 。
(2)A、B、H的化学式:A ,B ,H 。
(3)写出C的酸性溶液与双氧水反应的离子方程式: 。
(4)写出鉴定E中阳离于的实验方法和现象:
。
|
座号 |
|
22.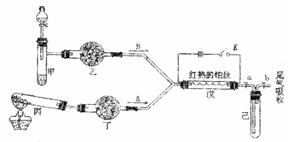 (10分)某化学课外小组设计了如下图(铁架台均已略去)所示的实验装置,进行气体性质实验。图中用箭头表示气体流向,A表示一种纯净、干燥的气体,B表示另一种气体。反应进行一段时间后,装置己中有红棕色气体生成。实验中所用的药品和干燥剂只能从下列物质中选取:Na2CO3、NaHCO3、MnO2、Na2O2、NaCl、无水CaCl2、NH4HCO3、碱石灰等固体和H2O2、蒸馏水。
(10分)某化学课外小组设计了如下图(铁架台均已略去)所示的实验装置,进行气体性质实验。图中用箭头表示气体流向,A表示一种纯净、干燥的气体,B表示另一种气体。反应进行一段时间后,装置己中有红棕色气体生成。实验中所用的药品和干燥剂只能从下列物质中选取:Na2CO3、NaHCO3、MnO2、Na2O2、NaCl、无水CaCl2、NH4HCO3、碱石灰等固体和H2O2、蒸馏水。
根据图中装置和反应现象请回答:
(1)丙中发生反应的化学方程式为 。
(2)丁中的干燥剂应选 ,不选另一种干燥剂的理由是
。
(3)甲中发生反应的化学方程式为 。
(4)戊中发生的主要反应的化学方程式为 ,此反应是(吸热、放热) 反应,可能发生的什么现象可以证明你的判断 。
21.(10分)(1)下列操作会导致实验结果偏高的是
A.配制一定物质的量浓度的硫酸溶液时,定容摇匀后,发现液面低于刻度线。
B.在配制一定物质的量浓度溶液时,用 10 mL的量筒量取5.0 mL液体溶质时俯视读数
C.用天平称量20.5g某物质,砝码和药品的位置放反,所得药品的质量
D.10%的硫酸和90%的硫酸等体积混合配制50%的硫酸溶液
E.配制一定物质的量浓度溶液时,定容时仰视读数,所得溶液的浓度
(Ⅱ)现有下列仪器或用品:a.铁架台(含铁圈、铁夹) b.锥形瓶c.滴定管 d.烧杯(若干) e.玻璃棒 f.胶头滴管 g.托盘天平(含砝码) h.滤纸 i.量筒 j.漏斗 k.温度计。
现有下列试剂:A.NaOH固体 B.碳酸钠溶液 C.氯化镁溶液 D.蒸馏水,试填空:
(1)如图分别是温度计、量筒、滴定管的一部分,下述判断及读数(虚线刻度)不正确的是
。
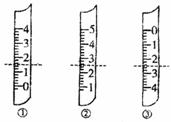 A.①是量简,读数为1.5mL
A.①是量简,读数为1.5mL
B.②是量筒,读数为2.5mL
C.③是滴定管,读数为2.50mL
D.②是温度计,读数是2.5℃
(2)配制一定物质的量浓度的氢氧化钠溶液时,还缺少的仪器是
(3)除去 Mg(OH)2中混有的少量 Ca(OH)2,可以用的试剂是: (选填序号),操作方法是 、 洗涤。完成上述操作,上述仪器或用品用到的有 (从上述仪器或用品中选择,并填上相应序号)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com