
题目列表(包括答案和解析)
4、设某元素某原子核内的质子数为m,中子数为n,则下述论断正确的是
(A)不能由此确定该元素的原子量 (B)这种元素的原子量为m+n
(C)若碳原子质量为W克,此原子的质量为(m+n)W克 (D)核内中子和质子共同决定元素种类
3、Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,而NaClO被还原为NaCl,若反应中Na2Sx与NaClO的物质的量之比为1:16,则x值是
A.2 B.3 C.4 D.5
2、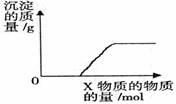 将溶液(或气体)X逐渐加入(或通入)到一定量Y溶液中,产生沉淀的质量与加入X的物质的量关系如右图,符合图中情况的一组物质是
将溶液(或气体)X逐渐加入(或通入)到一定量Y溶液中,产生沉淀的质量与加入X的物质的量关系如右图,符合图中情况的一组物质是
|
|
(A) |
(B) |
(C) |
(D) |
|
X |
Ba(HCO3)2 溶液 |
Na2CO3 溶液 |
KOH 溶液 |
CO2 气体 |
|
Y |
NaOH 溶液 |
CaCl2 溶液 |
Mg(HSO4)2 溶液 |
石灰水 |
1、下列有关物质分类或归类正确的是
①混合物:石炭酸、福尔马林、水玻璃、水银 ②化合物:CaCl2、烧碱、聚苯乙烯、HD
③电解质:明矾、胆矾、冰醋酸、硫酸钡 ④同系物: CH2O2、C2H4O2、C3H6O2、C4H8O2
⑤有机物:酒精、 油脂、蔗糖、蛋白质
A.①③④ B.②④ C.②③④ D.③⑤
31.工业上用丁烷氧化法制醋酸,反应的化学方程式可表示为:
2C4H10+5O2 4CH3COOH+2H2O
4CH3COOH+2H2O
现用58吨丁烷为原料制取醋酸,求:
(1)理论上需要标准状况下的空气____________m3(设空气中O2、N2的体积分数分别为0.2、0.8),同时生成水_____________吨。
(2)若生成的醋酸溶解在生成的水中,所得醋酸的质量分数为______________%。
(3)若同时生产质量分数为100%的冰醋酸m1吨和质量分数为50%的醋酸m2吨,且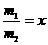 ,需补充水y吨,则y与x的关系式为________________;若不补充水,则m1+m2=__________
,需补充水y吨,则y与x的关系式为________________;若不补充水,则m1+m2=__________
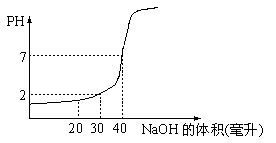
30.下图为20毫升一定物质的量浓度的盐酸,用一定物质的量浓度的氢氧化钠溶液滴定的图示,依据图示计算出盐酸和氢氧化钠的物质的量的浓度。
29.某有机物A(C4H6O5)广泛存在于许多水果内,尤以苹果、葡萄、西瓜、山楂内为多。该化合物具有如下性质:
① 在25℃时,电离常数K1=3.99×10-4,K2=5.5×10-6
②A+RCOOH(或ROH)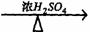 有香味的产物
有香味的产物
③1molA 慢慢产生l.5mol气体
慢慢产生l.5mol气体
④A在一定条件下脱水的产物B(不是环状化合物)可与溴水发生加成反应
⑤B在一定条件下可继续脱水生成内含五元环的化合物C
已知: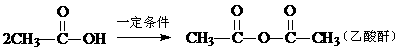
试回答:(l)根据以上信息,对A的结构可作出的判断是 (错选则本小题不得分)
(a)肯定有碳碳双键 (b)有两个羧基
(c)肯定有醇羟基 (d)有-COOR官能团
(2)有机物A的结构简式为
(3)B和溴水反应的化学方程式:
(4)写出与A同类别的同分异构体的结构简式
(5)已知1,3-丁二烯与乙烯反应生成环己烯(C6H10)。写出C与2-甲基-1,3-丁二烯发生反应的化学方程式:
。
28.据媒体报道,去年11月在上海、成都、香港等地,某些水产品相继被查出“染毒”,其体内含有禁用的鱼药孔雀石绿,其结构简式如图l,该物质在水生生物体中的代谢产物是无色孔雀石绿,其结构简式如图2,它的残留毒性比孔雀石绿更强。
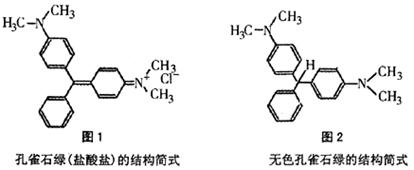
请根据上述有关信息回答下列问题:
(1)下列关于无色孔雀石绿(图2结构)的说法中正确的是( )
(A)该物质属于芳香族化合物
(B)该物质与孔雀石绿(图1结构)互为同分异构体
(C)该物质分子中的三个苯环处在同一平面上
(D)该物质能和溴水发生加成反应使溴水褪色
(2)合成孔雀石绿的有机原料是苯甲醛和二甲苯胺。苯甲醛在工业上有多种制法,其中有:
①甲苯在催化剂(五氧化二钒、三氧化钨或三氧化钼)作用和加热条件下直接被氧气氧化生成:其化学方程式为 。
②将甲苯氯化,然后再水解、氧化而生成。
写出上述有关反应条件:氯化 :水解
写出上述有关氧化过程的的化学方程式: 。
上述两种方法比较你认为较好的是 ,简述理由 。
27.某课外小组利用H2还原黄色的WO3粉末测定W的相对原子质量,下图是测定装置的示意图,A中的试剂是盐酸。
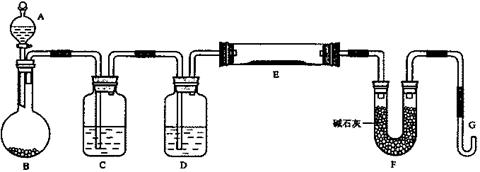
请回答下列问题。
(1)仪器中装入的试剂:B_________ 、C________、D___________;
(2)连接好装置后应首先_________________________;
(3)“加热反应管E”和“从A瓶逐滴滴加液体”这两步操作应该先进行的是_________。在这两步之间还应进行的操作是____________________________;
(4)反应过程中G管逸出的气体是____________,其处理方法是_____________;
(5)从实验中测得了下列数据:
①空E管的质量a
②E管和WO3的总质量b
③反应后E管和W粉的总质量c(冷却到室温称量)
④反应前F管及内盛物的总质量d
⑤反应后F管及内盛物的总质量e
由以上数据列出计算W的相对原子质量的计算式(除W外,其他涉及的元素的相对原子质量均为已知):
26.铁是人体必需的微量元素之一,没有铁,血红蛋白就不能结合氧分子进行输氧,医学上经常用硫酸亚铁糖衣片给患贫血的病人补铁。某研究性学习小组对某瓶硫酸亚铁片是否变质及含量进行了研究,请回答下列问题:
(1)可以检验硫酸亚铁是否被氧化的试剂的是 (填化学式)。
(2)检验硫酸盐可用的试剂是 ;检验亚铁盐可用的试剂是 ,现象是 。
(3)在含量测定时,该小组取药片10片,加稀硫酸6mL与新沸过的冷水适量使硫酸亚铁片溶解,再用新沸过的冷水稀释为200mL,用干燥滤纸迅速过滤,正确量取滤液30mL,立即用已知浓度的高锰酸钾溶液滴定。
①把水煮沸的原因是 ,操作时注意“迅速”“立即”,原因是 。
②滴定前,首先要精确配制一定物质的量浓度的高锰酸钾溶液200 mL,配制时需要的仪器除天平、洗瓶(装蒸馏水)、玻璃棒和胶头滴管外,还需要的仪器有 等;上述实验中的KMnO4溶液要进行酸化,用于酸化的酸是( )。
(A)稀硝酸 (B)稀硫酸 (C)稀盐酸 (D)浓硝酸
③本实验判断滴定是否到终点的方法为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com