
题目列表(包括答案和解析)
3.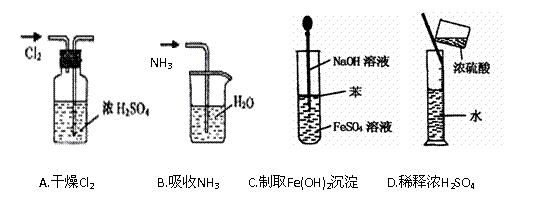 实验是研究化学的基础,下图所示的实验方法、装置或操作完全正确的是
实验是研究化学的基础,下图所示的实验方法、装置或操作完全正确的是
2.下列叙述正确的是
A.有单质参加或单质生成的化学反应一定是氧化还原反应 www.k@s@5@ 高#考#资#源#网
B.有阳离子存在的物质中一定存在阴离子
C.只有一种生成物的化学反应不一定是化合反应
D.离子反应一定是复分解反应
1.下列化学用语正确的是
A.白磷的分子式:P
B.Na+结构示意图是: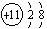
C.碳一12 的原子符号:612C D.HClO的电子式: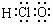
22、(12分)运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义。
 (1)合成氨反应N2(g)+3H2(g) 2NH3(g),若在恒温、恒压条件下,向平衡体系中通入氩气,平衡
移动(填“向左”“向右”或“不”);使用催化剂后反应的△H(填“增大”“减小”或“不改变”)
。
(1)合成氨反应N2(g)+3H2(g) 2NH3(g),若在恒温、恒压条件下,向平衡体系中通入氩气,平衡
移动(填“向左”“向右”或“不”);使用催化剂后反应的△H(填“增大”“减小”或“不改变”)
。
(2)一定温度下,在恒容密闭容器中N2O5可发生化学反应:
 2 N2O5(g) 4NO2(g)+O2(g) △H>0
2 N2O5(g) 4NO2(g)+O2(g) △H>0
①下表为反应T1温度下的部分实验数据:
|
t/s |
0 |
500 |
1000 |
|
C(N2O5)/mol·L-1 |
5.00 |
3.52 |
2.48 |
则500s内N2O5的分解速率为 。
②在T2温度下,反应1000s时测得NO2的浓度为4.98 mol·L-1,则T2 T1(填
“>”“<”“=” )
(3)已知肼分子(H2N-NH2)可以在氧气中燃烧生成氮气和水。
①利用肼、氧气与KOH溶液组成碱性燃料电池,请写出电池负极的电极反应式
②用电离方程式表示肼的水溶液呈碱性的原因
③肼是强还原剂,与氧化剂反应时放出大量的热,如:N2H4(1)+2H2O2(1)==N2(g)+4H2O(g) △H= -642.2kJ·mol-1
因此肼可以作为火箭推进剂。根据上述信息,你认为是否可以通过改变反应条件,由氮气和水蒸气来制取肼 。说明原因 。
2010学年第一学期十校联合体高三期中联考
21、(12分)有机物F(C13H16O2)是一种芳香酯,可用作香精的调香剂。如图是该有机物的合成路线:
Br Br
|
 | |
氧化
氧化
| |
氧化
氧化



 溴水 CH3-CH2-C-CH2
溴水 CH3-CH2-C-CH2
 反应① | 反应②
反应③
反应④
反应① | 反应②
反应③
反应④
CH3
OH
|
|



 -CH2CH2C1
CH3-CH2-C-COOH
-CH2CH2C1
CH3-CH2-C-COOH
|
反应⑦ CH3
|
请回答下列问题:
(1)反应②中另加的试剂是 ;反应⑤的一般条件是: 。
(2)反应③的化学方程式为 。
(3)反应⑦的化学方程为 。
(4)上述合成路线中属于取代反应的是 (填编号)。
(5)C的同分异构体有多种,其中能发生水解反应的有机物有 种。
20.(11分)都由短周期元素形成的常见非金属固体单质A与常见金属单质B,在加热条件下反应生成化合物C,C与水反应生成白色沉淀D和气体E,D既能溶于强酸,也能溶于强碱。E在足量空气中燃烧产生刺激性气味气体G,G在大气中能导致酸雨的形成。E被足量氢氧化钠溶液吸收得到无色溶液F,溶液F在空气中长期放置发生反应,生成物之一为H。 H与一种相对分子质量为78的供氧剂的结构和化学性质相似,其溶液显黄色.
请回答下列问题:
(1)组成单质A的元素位于周期表中的位置 。
(2)指出H物质中的化学键类型 。
(3)写出B与氢氧化钠溶液反应的离子方程式:______________________。
(4)E被足量NaOH溶液吸收得到溶液中的离子浓度由大到小关系是 。
(5)G与氯酸钠在酸性条件下反应可生成消毒杀菌剂二氧化氯.当生成2 mol二氧化氯时,转移电子________mol.
(6)溶液F在空气中长期放置生成H的化学反应方程式为: 。
19、(11分)硫酸铜是一种应用极其广泛的化工原料;以下是某工厂用含铁废铜为原料生产胆矾(CuSO4·5H2 O)和副产物石膏(CaSO4·2H2O)的生产流程示意图:
含铁废铜 石灰浆
 检验
检验
→ → → → → →产品
稀硝酸与稀硫酸 红棕色 石膏 母液
的混合液 滤渣
胆矾和石膏在不同温度下的溶解度(g/100g水)见下表。
温度( C) C) |
20 |
40 |
60 |
80 |
100 |
|
石膏 |
0.32 |
0.26 |
0.15 |
0.11 |
0.07 |
|
胆矾 |
32 |
44.6 |
61.8 |
83.8 |
114 |
请回答下列问题:
(1)红棕色滤渣的主要成分是 ;
(2)写出浸出过程中生成硫酸铜的离子方程式 ;
(3)操作I包括蒸发浓缩、 等操作,温度应该控制在  C左右;
C左右;
(4)从溶液中分离出硫酸铜晶体的操作Ⅱ应为 、 、洗涤、干燥;晶体用无水乙醇作洗涤液而不用蒸馏水的原因是 ;干燥时采用晾干,不用加热烘干的原因是 。
(5)取样检验是为了确认Fe3+是否除净。有同学设计了以下两种方案,在实验室分别对所取样品按下列方案进行操作:
方案一:取样于试管→滴加KSCN溶液; 方案二:纸层析→喷KSCN溶液;
①你认为上述两种方案设计更合理的是 ;
②指出你认为不合理方案存在的问题是 。
18、Na2O2、HC1、A12O3三种物质在水溶液中完全反应后,溶液中只含有Na+、H+、C1-、OH-,且溶液呈中性,则Na2O2、HC1、A12O3的物质的量之比可能( )A、3:2:1 B、2:4:1 C、2:3:1 D、4:2:1
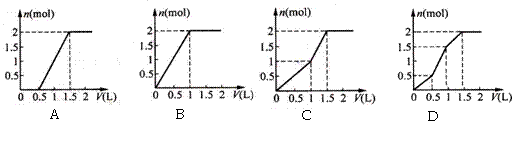
17、用含1 mol HCl的盐酸酸化含1 mol MgSO4的溶液,当向其中滴加1 mol/L 的Ba(OH)2 溶液时,产生沉淀的物质的量(n)与加入Ba(OH)2 溶液体积(V)间的关系图正确的是 ( )

16.有Fe2+、NO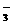 、Fe3+、NH
、Fe3+、NH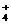 、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是
(
)
、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是
(
)
A. 氧化剂与还原剂的物质的量之比为1:8
B. 该过程说明Fe(NO3)2 溶液不宜加酸酸化
C. 若有1 mol NO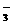 发生氧化反应,则转移8 mol电子
发生氧化反应,则转移8 mol电子
D. 若把该反应设计为原电池,则负极反应为Fe2+ - e- = Fe3+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com