
题目列表(包括答案和解析)
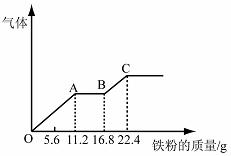
14.某稀硫酸和稀硝酸的混合溶液200 mL,平均分成
两份。向其中一份中逐渐加入铜粉,最多能溶解
13.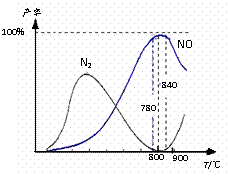 氨催化氧化是硝酸工业的基础,在某催化剂作
氨催化氧化是硝酸工业的基础,在某催化剂作
用下只发生主反应①和副反应②,有关物质产
率与温度的关系如右图。
4NH3(g)+5O2(g) 4NO(g)+6H2O(g)
4NO(g)+6H2O(g)
△H=-905 kJ·mol-1 ①
4NH3(g)+3O2(g) 2N2(g)+6H2O(g)
2N2(g)+6H2O(g)
△H=-1268 kJ·mol-1 ②
下列说法中正确的是 ( )
A.工业上氨催化氧化生成 NO时,温度应控制在
780-840℃之间
B.工业上采用物料比n(O2)/n(NH3)在1.7-2.0,主要是为了提高反应速率
C.加压可提高NH3生成NO的转化率
 D.N2氧化为NO的热化学方程式为:N2(g)+O2(g)
D.N2氧化为NO的热化学方程式为:N2(g)+O2(g) 2NO(g) △H=+181.5 kJ·mol-1
2NO(g) △H=+181.5 kJ·mol-1
12.设NA表示阿伏加德罗常数的值,下列有关NA的叙述中正确的有 ( )
①0.25molNa2O2中含有的阴离子数为0.5NA
②7.5gSiO2晶体中含有的硅氧键数为0.5NA
③1 mol α-氨基乙酸(甘氨酸)分子中存在10 NA对共用电子
④250mL2mol/L的氨水中含有NH3·H2O的分子数为0.5NA
⑤3.0 g淀粉和葡萄糖混合物中共含碳原子数为0.1NA
⑥18g D2O(重水)完全电解,转移NA个电子
⑦标准状况下,2.24L CHCl3含有的分子数为0.1NA
⑧电解精炼铜时,当阳极溶解32 g铜时,转移的电子数为NA个
A.2个 B.3个 C.4个 D.5个
11.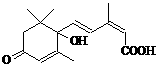 北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,
以保证鲜花盛开。S-诱抗素的分子结构如右图,下列
关于该物质的说法正确的是 ( )
A.其分子式为C15H22O4
B.1 mol该物质与NaOH溶液反应,最多消耗2 mol NaOH
C.既能发生加聚反应,又能发生缩聚反应
D.既可以与FeCl3溶液发生显色反应,又可以使酸性KMnO4溶液褪色
10.CsICl2是一种碱金属的多卤化物,这类物质在化学反应中既可表现氧化性又可表现还原性,有关该物质的说法正确的是 ( )
A.Cs显+3价,I、Cl均显-1价
B.Cs显+1价,Cl显+1价,I显-1价
C.在CsICl2溶液中通入Cl2,有单质碘生成
D.在CsICl2溶液中通入SO2气体,有硫酸生成
9.下列离子方程式正确的是 ( )
A.向Ag(NH3)2OH溶液中加足量氢溴酸:
Ag(NH3)2++ OH-+3H+=Ag++2NH4++H2O
B.Ba(HCO3)2溶液与Ba(OH)2溶液任意比混合:
Ba2++HCO3-+OH-═BaCO3↓+H2O
C.FeCl3溶液中撒入CaCO3粉末有气泡产生:
2Fe3++3CaCO3+3H2O=2Fe(OH)3↓+3Ca2++3CO2↑
D.向NH4HCO3溶液中加入足量NaAlO2溶液:
NH4++AlO2-+2H2O= NH3·H2O+ Al(OH)3↓
8.著名化学家徐光宪获得2008年度“国家最高科学技术奖”,以表彰他在稀土串级萃取理论方面作出的贡献。稀土铈(Ce)元素主要存在于独居石中,金属铈在空气中易氧化变暗,受热时燃烧,遇水很快反应。已知:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+。下列说法正确的是 ( )
A.电解熔融Ce02制Ce,铈在阳极获得
B.铈溶于氢碘酸的化学方程式可表示为:Ce+4HI=CeI4+2H2↑
C.用Ce(S04)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++2Fe2+=Ce3++2Fe3+
D.四种稳定的核素13658Ce、13858Ce、14058Ce、14258Ce,它们互称为同位素
7.某溶液既能溶解Al(OH)3,又能溶解H2SiO3,在该溶液中可以大量共存的离子组是( )
A.K+、Na+、HCO3-、NO3- B.Na+、SO42-、Cl-、 ClO-
C.H+、Mg2+、SO42-、NO3- D.Ag+、K+、NO3-、Na+
6.将Na2O2、HCl和Al2O3起溶于一定量的水中,完全反应后测得所得溶液中只含有Na+、AlO2一、Cl一 (不考虑AlO2一的水解和H2O的电离),则Na2O2、HCl、Al2O3的物质的量之比不可能是 ( )
A.2∶2∶1 B.3∶3∶1 C.3∶4∶1 D.4∶6∶1
5.向 和
和 的酸性混合溶液中通入
的酸性混合溶液中通入 气体,有白色沉淀生成。此沉淀是( )
气体,有白色沉淀生成。此沉淀是( )
A.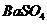 B.
B.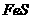 C.
C.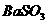 D.
D.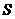
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com