
题目列表(包括答案和解析)
16.某学生设计了如图的方法对A盐进行鉴定:
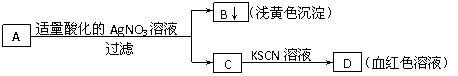
由此分析,下列结论中,正确的是
A.A中一定有Fe3+ B.C中一定有Fe3+
C.B为AgI沉淀 D.A一定为FeBr2溶液
15.某研究性学习小组为了探索镁粉与溴水反应的机理,做了如下四组实验:
①将镁粉投入冷水中,未见任何现象;
②将镁粉放入溴水中,观察到只是开始时产生极少量的气泡,但溴水的颜色逐渐褪去;
③将镁粉放入液溴中,未观察到任何明显现象;
④向含足量镁粉的液溴中滴加几滴水,观察到溴的红棕色很快褪去。
则下列关于镁与溴水的反应机理的论述中正确的是
A.镁粉只直接与溴水中的溴反应
B.镁粉只与溴水中的酸反应
C.产生极少量的气泡是由于镁粉与水反应得到
D.镁粉在水的催化下与溴发生反应
14.用足量盐酸处理1.68g某合金,放出448mL H2(标准状况下),有0.56g不溶物;用足量NaOH溶液处理该合金时放出896mL H2(标准状况下),有1.12g不溶物。则该合金的组成可能是 A.Al、Fe B.Fe、Si C.Al、Si D.Zn、Fe
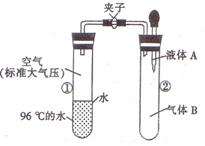
13、如图所示,夹子开始处于关闭状态,将液体A滴人
试管②与气体B充分反应,打开夹子,可发现试管①内
的水立刻沸腾了。则液体A和气体B的组合不可能是
下列的
A.氢氧化钠溶液.二氧化碳 B.水.氨气
C.氢氧化钠溶液.一氧化氮 D.水.二氧化氮
12.常温下,测得某无色溶液中由水电离出的C(H+)=1×10-13mol·L-1,则该溶液中一定能共存的离子组是
A.AlO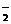 、NO
、NO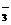 、Na+、Cl-
B.Mg2+、SO
、Na+、Cl-
B.Mg2+、SO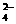 、Na+、CIO-
、Na+、CIO-
 C.Fe3+、NO3-、K+、SO
C.Fe3+、NO3-、K+、SO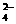 D.Ba2+、K+、NO
D.Ba2+、K+、NO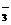 、Cl-
、Cl-
11.将S02通入Fe(NO3)3溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色;继续滴人BaC12 溶液,产生白色沉淀。在上述一系列变化过程中,最终被还原的是
A . S02 B . Cl- C . Fe3+ D . N03-
10.右图表示在某溶液中滴加Ba(OH)2溶液时,沉淀的
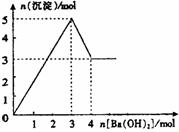 物质的量随Ba(OH)2的物质的量的变化关系。该
物质的量随Ba(OH)2的物质的量的变化关系。该
溶液的成分可能是
A、MgSO4 B、KAl(SO4)2
C、Al2(SO4)3 D、NaAlO2
9.水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O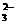 +O2+xOH-
+O2+xOH- Fe3O4+S4O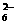 +2H2O,下列说法中,正确的是:
+2H2O,下列说法中,正确的是:
A.每生成1mol
Fe3O4,反应转移的电子总数为3mol B.Fe2+和S2O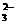 都是还原剂
都是还原剂
C.1mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为1/3mol D.x=2
8.下列除去杂质的方法正确的是
A.除去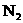 中的少量
中的少量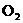 :通过灼热的CuO粉末,收集气体
:通过灼热的CuO粉末,收集气体
B.除去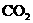 中的少量HCl:通入
中的少量HCl:通入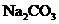 溶液,收集气体
溶液,收集气体
C.除去 溶液中的少量
溶液中的少量 :加入足量铁屑,充分反应后,过滤
:加入足量铁屑,充分反应后,过滤
D.除去KCl溶液中的少量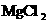 :加入适量NaOH溶液,过滤
:加入适量NaOH溶液,过滤
7.下列离子方程式,正确的是
A.Ca(ClO)2溶液中通入少量SO2气体:
H2O +SO2 + Ca2+ + 2ClO- === CaSO3↓+ 2HClO
B.向NH4HCO3 溶液中加入足量Ba(OH)2溶液
NH4+ +HCO3- + 2OH- === H2O + CO32- + NH3·H2O
C.向FeCl2溶液中加足量溴水
2Fe2+ + Br2 === 2Fe3++ 2Br-
D.NaAlO2溶液中通入过量CO2
2AlO2- +CO2+3H2O===2Al(OH)3↓+CO32-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com