
题目列表(包括答案和解析)
1、B 2、C 3、B 4、B 5、B C 6、A 7、B 8、C 9、B 10、B
16、海水中溴常以NaBr形式存在,从海水中提取溴的方法之一是:①通入通入Cl2至浓缩的溴化物溶液,氧化海水中的Br-,然后用空气把生成的溴吹出。②以氢氧化钠溶液吸收Br2 (Br2跟烧碱生成NaBr和NaBrO3)。③向所得含溴化合物溶液中加稀H2SO4,溴又重新析出。要求:⑴写出各步反应的化学方程式。(提示:第③步反应中生成物有硫酸钠)
⑵经分析海水中含溴0.0065%,则海水中含NaBr的质量百分含量为?试计算多少吨海水可制得1.0t溴?(假设提取过程中溴无损失)
第一单元 氯、溴、碘及其化合物
15、海水占地球总储水量的97.2%。若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源。试回答下列问题:
⑴海水中含有大量的氯化钠。氯化钠中的金属元素化合价为 。
⑵目前国际上实用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水,由此可判断蒸馏法是 (填物理变化、化学变化)
⑶工业上利用电解饱和食盐水可制得重要化工产品,反应式为:
 食盐+H2O NaOH+H2+Cl2(未配平)。该反应中食盐的化学式是_______________。利用电解所得气体制36.5%的浓盐酸100t,最少需要消耗食盐
t 。
食盐+H2O NaOH+H2+Cl2(未配平)。该反应中食盐的化学式是_______________。利用电解所得气体制36.5%的浓盐酸100t,最少需要消耗食盐
t 。
|
|
|
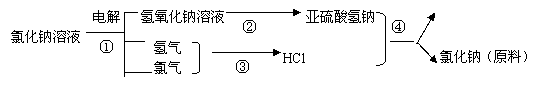
写出①③的化学反应方程式: ,
14、在实验室里制取某些有毒气体时,为了尽量防止毒气逸散造成空气污染,有人设计了如图所示的装置[Ⅰ]。并设想用[Ⅱ]或[Ⅲ]两种简易装置代替[Ⅰ]的b-c部分。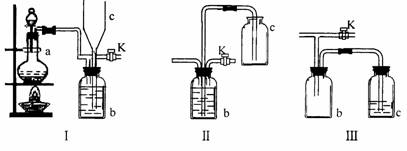
试回答:⑴若用[Ⅰ]制取氯气,b瓶中加入的液体一般为 ______________。在选取试剂正确且适量的前题下,反应开始后,当关闭活塞K时,如若发现c中液面不明显上升,你分析可能的原因是________________________,检查的简单方法是 。
⑵装置[Ⅰ]中b能防止多余气体逸散的原因____________________________ 。
⑶欲用[Ⅱ]或[Ⅲ]代替[Ⅰ]中的b-c部分(选用液体相同),是否可行?说明理由。
[Ⅱ]是否可行(填“是”或“否”) ___________理由是______________________;
[Ⅲ]是否可行(填“是”或“否”) ____________理由是______________ 。
13、某同学为了验证海带中含有碘,拟进行如下实验,请回答相关问题。
第1步:灼烧。将足量海带灼烧成灰烬。该过程中使用到的玻璃仪器有 (填代号)
A、试管 B、瓷坩埚 C、坩埚钳 D、三角架 E、泥三角 F、酒精灯 G、容量瓶H、玻棒
第2步:Iˉ溶液的获取。操作是_________________________________________。
第3步:氧化。操作是依次加入合适的试剂。下列氧化剂最好选用_________(填代号)。
A、浓硫酸 B、新制氯水 C、KMnO4溶液 D、H2O2
理由是__________________________________________________________________。
第4步:碘单质的检验。取少量第3步的溶液,滴淀粉溶液,若溶液显蓝色,则证明含碘。
12、已知:①A、B、C、D四种物质均含有元素X,可能还含有元素Y或Z。元素Y、X、Z的原子序数依次递增且不超过20。② X在A、B、C、D中的化合价分别为0、-1、+1、+5。③室温下单质A与某种常见一元强碱溶液反应,可得到B和C。④化合物D在二氧化锰催化下受热分解,可制得元素Y的单质。请回答下列问题:
⑴写出元素X、Y、Z的元素符号:X: ,Y: ,Z 。
⑵写出A、B、C、D的化学式:A ,B ,C ,D 。
⑶写出③中反应的化学方程式 。
⑷写出④中反应的化学方程式 。
11、洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。根据所学知识,回答下列问题:
⑴工业上将氯气通入石灰乳制取漂白粉,化学反应方程式为 。
⑵漂白粉的有效成分是(填化学式) 。漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为 。
⑶瓶装漂白粉久置空气中会呈稀粥状而失效。分析为什么?
⑷请问:⑴中反应和⑵中反应,属于氧化还原反应的是(填编号) 。
10、KCl和KBr的混合物3.87克,溶于水并加入过量的AgNO3溶液后,产生6.63克沉淀,则混合物中含钾为 ( )
A、24.1% B、40.3% C、25.9% D、48.7%
9、用MnO2和浓盐酸制取氯气。当4mol氯化氢被氧化,生成的氯气的体积(标准状况)是( )
A、22.4L B、44.8L C、67.2L D、89.6L
8、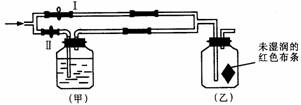 如图所示:若关闭Ⅰ阀,打开Ⅱ阀,让一种含有氯气的气体经过甲瓶后,通入乙瓶 ,布条不褪色;若关闭Ⅱ阀打开Ⅰ阀,再通入这种气体,布条褪色。甲瓶中所盛的试剂可能是( )
如图所示:若关闭Ⅰ阀,打开Ⅱ阀,让一种含有氯气的气体经过甲瓶后,通入乙瓶 ,布条不褪色;若关闭Ⅱ阀打开Ⅰ阀,再通入这种气体,布条褪色。甲瓶中所盛的试剂可能是( )
①浓H2SO4 ②NaOH溶液 ③KI溶液
④饱和NaCl溶液
A、② B、②③ C、①②③ D、①②④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com