
题目列表(包括答案和解析)
5.将钠.镁.铝各0.3 mol分别放入100 mL 1mol·L-1
的盐酸中,同温同压下产生的气体体积比是( )
A.1︰2︰3 B.6︰3︰2
C.3︰1︰1 D.1︰1︰1
4.新华网报导:三鹿9月11日晚发布声明称,经自检发现2008年8月6日前出厂的部分批次三鹿婴幼儿奶粉受到三聚氰胺的污染,市场上大约有700吨,将全部召回。中国卫生部提醒公众,立即停止使用该品种奶粉,已食用该奶粉的婴幼儿如出现小便困难等异常症状,要及时就诊。三聚氰胺的结构如右图所示,关于三聚氰胺的说法不正确的是
( )
 A.三聚氰胺属于有机物
A.三聚氰胺属于有机物
B.三聚氰胺属于高分子化合物
C.分子式C3N6H6,氮的质量分数为66.7%
D.溶于水呈弱碱性
3.近代化学常用CaH2作生氢剂,其化学方程式:CaH2+2H2O=Ca(OH)2+2H2↑其中水的作用是 ( )
A.氧化剂 B.还原剂
C.既不是还原剂也不是氧化剂 D.溶剂
2.根据反应式:①2Fe3++2I-=2Fe2++I2②Br2+2Fe2+=2Fe3++2Br-可判断离子的还原性从强到弱的顺序是 ( )
A.Br-.Fe2+.Cl- B.I-.Fe2+ .Br-
C.Br-.I-.Fe2+ D.Fe2+.I-.Br-
1.下列性质中,可以证明某化合物中一定存在离子键的是 ( )
A.可溶于水 B.具有较高的熔点
C.水溶液一定能够导电 D.熔融状态能够导电
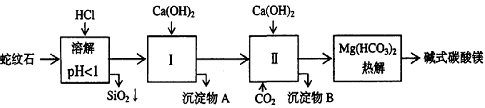
27.(13分)蛇纹石矿可以看作由MgO、Fe2O3、Al2O3、SiO2组成。由蛇纹石制取碱式碳酸镁的实验步骤如下:
|
氢氧化物 |
Fe(OH)3 |
Al(OH)3 |
Mg(OH)2 |
|
开始沉淀pH |
1.5 |
3.3 |
9.4 |
(1) 蛇纹石矿加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是________。
(2) 进行Ⅰ操作时,控制溶液pH=7-8(有关氢氧化物沉淀的pH见上表)Ca(OH)2不能过量,
若Ca(OH)2过量可能会导致 溶解、产生 沉淀。
(3) 从沉淀混合物A中提取红棕色氧化物作颜料,先向沉淀物A中加入_________ (填入物质的化学式),然后__________________________________ (依次填写实验操作名称)。
(4) 物质循环使用,能节约资源。上述实验中,可以循环使用的物质是______________(填写物质化学式)。
(5)若产品组成可表示为aMgCO3·bMg(OH)2·cH2O,己知18.2g产品完全分解后,产生6.6gCO2和8.0g MgO,由此可知,产品的化学式中:
a=_________、b=_________、c=_________。
惠安第一中学2011届高三年第一次月考化学学科试卷
26.(13分)已知A、B、C、D都是周期表中前四周期的元素,它们的原子序数依次增大。其中A、B原子的L层有2个未成对电子,C的三价阳离子与B的阴离子具有相同的电子层结构。D3+离子M层3d轨道电子为半满状态。请根据以上情况,回答下列问题:(答题时,用所对应的元素符号表示)
(1)写出B原子的核外电子排布式: ;D元素在周期表中处于_____
周期______族。
(2)A的最简单氢化物的分子空间构型是: ,其中心原子采取 杂化,属于 (填“极性分子”和“非极性分子”)。
(3)C元素最高价氧化物对应水化物可用于治疗胃酸过多,写出其反应的离子方式__________________________________;
(4)H2S和B元素的氢化物(分子式为H2B2)的主要物理性质比较如下
|
|
熔点/K |
沸点/K |
标准状况时在水中的溶解度 |
|
H2S |
187 |
202 |
2.6 |
|
H2B2 |
272 |
423 |
以任意比互溶 |
H2S和H2B2的相对分子质量基本相同,造成上述物理性质差异的主要原因: ;
(5)D和M(质子数为25)两元素的部分电离能数据列于下表:
元 素 素 |
M |
D |
|
|
电离能 (kJ·mol-1) |
I1 |
717 |
759 |
|
I2 |
1509 |
1561 |
|
|
I3 |
3248 |
2957 |
比较两元素的I2、I3可知,气态M2+再失去一个电子比气态D2+再失去一个电子难。对此,你的解释是 ;
25、(10分)北京市场销售的某种食用精制盐包装袋上有如下说明:
|
产品标准 |
GB5461 |
|
产品等级 |
一级 |
|
配 料 |
食盐、碘酸钾、抗结剂 |
|
碘含量(以I计) |
20~50mg/kg |
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于方框内)
□ KIO3 + □KI + □H2SO4 = □K2SO4 + □I2 + □H2O
(2)上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
已知Na2SO3稀溶液与I2反应后溶液显酸性,写出该反应的离子方程式:
。
(3)已知:I2+2S2O32-=2I-+S4O62-。某学生测定食用精制盐的碘含量,其步骤为:
a. 准确称取wg食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol·L-1的Na2S2O3溶液10.0mL,恰好反应完全。
①判断c中反应恰好完全依据的现象是:________________________________;
②b中反应所产生的I2的物质的量是: mol;
24、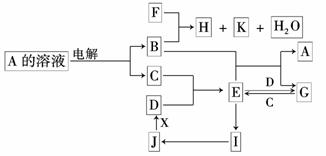 (12分)中学化学中几种常见物质的转化关系如下图所示(部分反应物、生成物及反应条件已略去):已知:B、C、D为常见单质,其中C为气体,B、D为金属;F为常见的强酸;K常温下为气体,且能使品红溶液褪色;将 E 溶液滴入沸水可制得一种红褐色胶体;B与E反应生成A与G是腐蚀法制作印刷电路版的反应原理; J 为红棕色固体.请回答下列问题:
(12分)中学化学中几种常见物质的转化关系如下图所示(部分反应物、生成物及反应条件已略去):已知:B、C、D为常见单质,其中C为气体,B、D为金属;F为常见的强酸;K常温下为气体,且能使品红溶液褪色;将 E 溶液滴入沸水可制得一种红褐色胶体;B与E反应生成A与G是腐蚀法制作印刷电路版的反应原理; J 为红棕色固体.请回答下列问题:
(1)实验室保存 G 溶液时要加入_____________________(写药品的名称),目的是:
___________________________________________________________;
(2)写出B与E反应生成A与G的离子方程式:
____________________________________________________________ ;
(3)为实现J→D的变化,若X是非金属氧化物,则X可能是:__________(写化学式) ; 若X是金属单质,请写出J→D 反应的化学方程式:_______________________________ ;
(4)写出B与F浓溶液反应的离子方程式:
_______________________________________________。
23、(8分)某无色透明溶液可能含有下列离子:K+、Al3+、Fe3+、Ba2+、NO3-、SO42-、HCO3-、Cl-等,取该溶液进行如下实验:
①用蓝色石蕊试纸检测该溶液,试纸显红色;
②取溶液少许,加入铜片和稀硫酸共热,产生无色气体,该气体遇到空气立即变为红棕色;
③取溶液少许,加入氨水有白色沉淀生成,继续加人过量氨水,沉淀不消失;
④取溶液少许,滴入氯化钡溶液产生白色沉淀;
⑤取实验 ④ 后的澄清溶液,滴人硝酸银溶液产生白色沉淀,再加人过量的稀硝酸,沉淀不消失。
请回答下列问题:
(1)在实验①中,下图所示的操作中正确的是___________________(填代号);
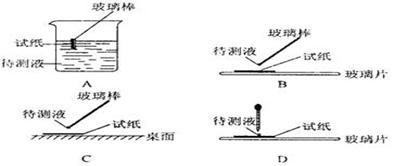
(2)根据上述实验判断原溶液中肯定存在的离子是____________________,肯定不存在的离子是_______________;
(3)写出与实验②有关的离子方程式:______ ______________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com