
题目列表(包括答案和解析)
9.下列说法正确的是
①离子晶体中每个离子周围均吸引着6个带相反电荷的离子
②二氧化碳晶体中,与一个二氧化碳分子距离最近且相等的二氧化碳分子有6个
③二氧化硅晶体中最小的环为12元环且每1mol二氧化硅晶体中含4mol的硅氧键
④石墨晶体为平面层状结构,每一层中最小的环为六元环,平均每个环中碳原子数与共价键数比为2:3
⑤白磷微粒间通过共价键结合形成分子晶体 ⑥C60比金刚石熔点高
⑦PCl3、HClO、CCl4分子中所有原子都满足8电子稳定结构
A.全部 B.③④⑤⑥ C.③④ D.①③⑤
8.右表为元素周期表中短周期的一部分。下列有关A、B、C、D、E五种元素的叙述中,不正确的是
A.与B形成的阴离子可能有:AB32-、A2B42-
B.A、B、C、D、E五种原子半径从大到小的顺序为:D>E>A>B>C
C.D在过量的B中燃烧的主要产物为DB3
D.由这5种元素中的几种元素形成只含极性键的非极性分子不少于4种
7.下列关于热化学反应的描述中正确的是
A.已知H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ·mol-1,
则H2SO4和Ba(OH)2反应的反应热△H=2×(-57.3)kJ·mol-1
B.燃料电池中将甲醇蒸气转化为氢气的热化学方程式是CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g);
△H=-192.9 kJ·mol-1,则CH3OH的燃烧热为192.9 kJ·mol-1
C.H2(g)的燃烧热是285.8 kJ·mol-1,则2H2O(g)=2H2(g)+O2(g);△H=+571.6 kJ·mol-1
D.葡萄糖的燃烧热是2800 kJ·mol-1,则1/2 C6H12O6 (s)+3O2 (g)=3CO2 (g)+3H2O ( l );
△H=-1400 kJ·mol-1
|
 |
|||
|
A |
|
B |
C |
|
|
|
|
D |
E |
|
6.将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀与通入CO2的量的关系可表示为
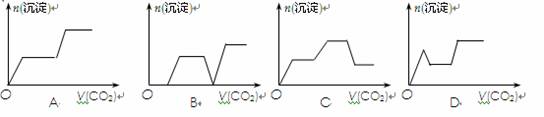
5.在一定的温度下,向饱和的烧碱溶液中放入一定量的过氧化钠,充分反应后恢复到原来的温度,下列说法正确的是
A.溶液中Na+浓度增大,有O2放出 B.溶液中OH-总数不变,有O2放出
C.溶液的pH增大,有O2放出 D.溶液中Na+总数减少,有O2放出,有晶体析出
4.混合下列各组物质使之充分反应,加热蒸干产物并在300℃灼烧至质量不变,最终残留固体为纯净物的是
A.向CuSO4溶液中加入一小块金属钠 B.等物质的量浓度、等体积的(NH4)2SO4与BaC12溶液
C.等物质的量的NaHCO3与Na2O2固体 D.在NaBr溶液中通入少量氯气
3.某溶液中,可能存在NH4+、Fe2+、Br-、CO32-、I-、SO32- 6种离子中的几种。①在原溶液中滴加足量氯水后,有气泡产生,溶液呈橙黄色;②向橙黄色溶液中加入BaCl2溶液时无沉淀生成;③橙黄色溶液不能使淀粉变蓝色。根据以上实验事实推断,该溶液中肯定不存在的离子为
A.NH4+、Br-、CO32- B.NH4+ 、SO32- 、I-
C.Fe2+ 、I- 、SO32- D.Fe2+、 CO32- 、I-
2.已知:①向黄色的FeCl3溶液中加入少量维生素C,溶液黄色褪去;
②向淀粉和KI的混合液中滴加FeCl3溶液,溶液颜色变蓝;
③取实验②生成的蓝色溶液,加入少量维生素C,溶液蓝色褪去。
下列判断不正确的是
A.上述实验证明维生素C有还原性
B.实验③能证明I2既有氧化性又有还原性
C.上述实验中涉及了三个氧化还原反应
D.上述实验证明还原性:维生素C > I- > Fe2+
1.化学知识广泛应用于生产、生活中,下列叙述正确的是
A.空气中的臭氧含量高于10-5%对人体健康有益无害
B.液氯罐泄漏时,可将其移入水塘中并加入生石灰
C.由硫铁矿制取硫酸的过程中,不涉及氧化还原反应
D.棉花和木材的主要成分都是纤维素,蚕丝和人造丝的主要成分都是蛋白质
21.5月12日四川汶川发生特大地震,为防止在大灾之后疫病流行,全国各地向灾区运送了大量的各种消毒剂、漂白剂等。(本题共7分)
(1)二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3在H2SO4存在下与SO2反应制得。请写出反应的离子方程式:
(2)过碳酸钠是一种有多用途的新型氧系固态漂白剂,化学式可表示为Na2CO3·3H2O2,它具有Na2CO3和H2O2的双重性质。过碳酸钠与下列物质均会发生化学反应而失效,其中过碳酸钠只发生了氧化反应的是
A.MnO2 B.KMnO4溶液 C.稀盐酸 D.Na2SO3溶液
(3)漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年,亚氯酸不稳定可分解,反应的离子方程式为:HClO2 → ClO2↑+ H+ +Cl-+H2O(未配平)。当1 mol HClO2发生分解反应时,转移的电子的物质的量是_________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com