
题目列表(包括答案和解析)
18.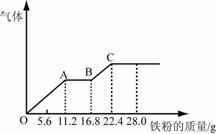 某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2 g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示。
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2 g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示。
(1)写出下列各反应阶段所发生的离子反应式:
①写出O-A段发生的离子反应式: 。
。
②A-B段发生的离子反应式: 。
③B-C段发生的离子反应式: 。
(2)分析A点溶液中主要存在那些离子: 。
(3)求原溶液中硫酸浓度是: 和硝酸的浓度是: 。
17.回答下列问题:
(1)有一种溶液除H+、OH-外,还有Na+、SO42-和Cl-,测得三种离子的浓度分别是0.01 mol·L-1、0.0035 mol·L-1和0.004 mol·L-1,该溶液的pH为 。
(2)液氨类似于水的电离,试写出液氨的电离方程式 ;
(3)下列离子方程式书写正确的是 。
A.石灰乳与Na2CO3溶液混合:Ca2++CO32-=====CaCO3↓
B.NH4HSO3溶液与足量的NaOH溶液混合加热:
NH4+ + HSO3-
+2OH-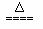 NH3↑+SO32- +2H2O
NH3↑+SO32- +2H2O
C.酸性条件下KIO3溶液与KI溶液反应生成I2: IO32- +5I-+3H2O====3I2+6OH-
D.AgNO3溶液中加入过量氨水:Ag++NH3·H2O=====AgOH↓+NH4+
E.H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-===== BaSO4↓+H2O
F.CuSO4溶液吸收H2S气体:Cu2++H2S======CuS↓+2H+
G.AlCl3溶液中加入过量的浓氨水:Al3++4NH3·H2O ===== AlO2- +4NH 4+ +2H2O
H.等体积、等浓度的Ba(OH)2稀溶液与NH4HCO3稀溶液混合:
Ba2++2OH-+NH4+ +HCO3-=== BaCO3↓+NH3·H2O+H2O
I.LiAlH4溶于适量水后得到无色溶液,则化学方程式可表示为:
LiAlH4+2H2O ===LiAlO2 +4H2↑
(4)Na2O2、HCl、Al2O3三种物质在水中完全反应后,溶液中只含有Na+、H+、Cl-、OH-,且溶液呈中性,则Na2O2、HCl、Al2O3的物质的量之比可能为 。
A.3∶2∶1 B.2∶4∶1 C.2∶3∶1 D.4∶2∶1
16. 某钠盐溶液中可能含有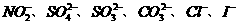 等阴离子。某同学取5份此溶液样品,分别进行了如下实验:
等阴离子。某同学取5份此溶液样品,分别进行了如下实验:
①用pH计测得溶液pH大于7
②加入盐酸,产生有色刺激性气体
③加入硝酸酸化的AgNO3溶液产生白色沉淀,且放出有色刺激性气体
④加足量BaCl2溶液,产生白色沉淀,该沉淀溶于稀硝酸且放出气体,将气体通入品红溶液,溶液不褪色。
⑤加足量BaCl2溶液,产生白色沉淀,在滤液中加入酸化的(NH4)2Fe(SO4)溶液,再滴加KSCN溶液,显红色
该同学最终确定在上述六种离子中仅含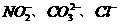 三种阴离子。
三种阴离子。
请分析,该同学只需要完成上述哪几个实验,即可得出此结论。
A. ①②④⑤ B. ③④ C. ③④⑤ D. ②③⑤
15.有3份等质量的小苏打,第1份直接与过量盐酸反应;第2份先加热,使其部分分解后,再与过量盐酸反应;第3份先加热,使其完全分解后,再与过量盐酸反应。假若盐酸的物质的量浓度相同,实际消耗盐酸的体积分别为V1、V2和V3,则V1、V2和V3的大小关系正确的是
A.V1>V2>V3 B. V1>V3>V2 C. V2>V3>V1 D. V1=V2=V3
14.下列实验操作或描述中错误的是
A.将NaNO3和KCl的混合液加热并浓缩至有晶体析出,趁热过滤时,可分离出NaCl晶体
B.溶剂蒸发的速度越快,或浓缩后的溶液冷却得越快,析出的晶体颗粒就越大
C.海带中碘元素的分离及检验时,需要向海带灰的浸取液中,加入少量稀硫酸和过氧化氢溶液
D.纸层析法分离铁离子和铜离子实验中,点样后的滤纸需晾干后,才能将其浸入展开剂中
13.下述实验能达到预期目的的是
|
编号 |
实验内容 |
实验目的 |
|
A |
将SO2通入酸性KMnO4溶液中 |
证明SO2的水溶液具有弱酸性 |
|
B |
向少量火柴头的浸泡液中滴加AgNO3、稀HNO3和NaNO2 |
验证火柴头含有氯元素 |
|
C |
在淀粉-KI溶液中滴加少量市售食盐配置的溶液 |
真假碘盐的鉴别 |
|
D |
在少量Fe(NO3)2试样加水溶解的溶液中,滴加稀H2SO4酸化,再滴加KSCN溶液 |
检验Fe(NO3)2试样是否变质 |
12.下列金属的工业制法正确的是
A.制钛:用金属钠置换出氯化钛(TiCl4)溶液中的钛
B.炼铁:用焦炭和空气反应产生的一氧化碳在高温下还原铁矿石中的铁
C.制钠:用海水作原料制得精盐,再电解纯净氯化钠溶液得到金属钠
D.炼铜:用黄铜矿经电解精炼得到纯度为99.9%的铜
11.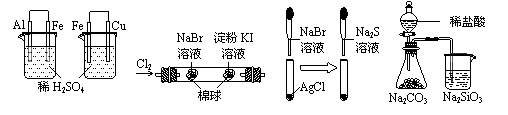 根据下列实验现象,所得结论不正确的是
根据下列实验现象,所得结论不正确的是
A B C D
|
实验 |
实验现象 |
结论 |
|
A |
左烧杯中铁表面有气泡,右边烧杯中铜表面有气泡 |
活动性:Al>Fe>Cu |
|
B |
左边棉花先变橙色再变无色,右边棉花先变蓝色后变无色 |
氧化性:Cl2>Br2>I2 |
|
C |
白色固体先变为淡黄色,后变为黑色 |
溶解性:AgCl>AgBr>Ag2S |
|
D |
锥形瓶中有气体产生,烧杯中液体有浑浊现象 |
非金属性:Cl>C>Si |
10.研究下表信息可直接得出的结论是
|
元素 |
F |
Cl |
Br |
I |
|
氢化物组成 |
HF |
HCl |
HBr |
HI |
|
氢化物形成难易程度 |
H2、F2混合,冷暗处剧烈化合并发生爆炸 |
H2、Cl2混合,光照或点燃时发生爆炸 |
H2与Br2混合,加热发生化合 |
H2、I2混合,加热化合,同时又分解 |
|
氢化物热稳定性 |
很稳定 |
稳定 |
较稳定 |
较不稳定 |
A.元素性质随原子序数的递增而呈周期性变化
B.同周期元素的非金属性随原子序数递增而增强
C.第VII A族元素的金属性随电子层数增加而减弱
D.第VIIA族元素的非金属性随电子层数的增加而减弱
9.将炭粉和铁粉均匀混合,撒入内壁分别用氯化钠溶液和稀醋酸溶液润湿过的具支试管中,并按下图装置好仪器,观察下图,示意正确的是
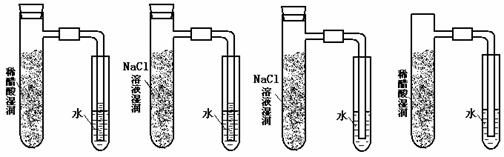
A B C D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com