
题目列表(包括答案和解析)
8.常温下,海水在浓缩过程中析出盐的种类和质量(表中为每升海水析出的各种盐的克数。单位g/L)如下:
|
海水密度 (g/mL) |
CaSO4 |
NaCl |
MgCl2 |
MgSO4 |
NaBr |
|
1.13 |
0.56 |
w.w.^w.k.&s.5*高.考.资.源.网 |
|
|
|
|
1.20 |
0.91 |
|
|
|
|
|
1.21 |
0.05 |
3.26 |
0.04 |
0.008 |
w.w.^w.k.&s.5*高.考.资.源.网 |
|
1.22 |
0.015 |
9.65 |
0.01 |
0.04 |
|
|
1.26 |
0.01 |
2.64 |
0.02 |
0.02 |
0.04 |
|
1.31 |
|
1.40 |
0.54 |
0.03 |
0.06 |
海水从密度为1.21 g/mL浓缩到密度为1.22g/mL时发生的变化是:
A.各种盐的溶解度增大 B.海水中水的质量分数减小
C.析出的粗盐中 NaCl的质量分数增大 D.海水中Br-浓度不变
7.有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期, Z、M同主族; X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料。下列说法中,正确的是
A.X、M两种元素只能形成X2M型化合物
B.由于W、Z、M元素的气态氢化物相对分子质量依次减小,所以其沸点依次降低
C.元素Y、Z、W的单质晶体属于同种类型的晶体w.w.^w.k.&s.5*高.考.资.源.网
D.元素W和M的某些单质可作为水处理中的消毒剂
 不定项选择题:本题包括7小题,每小题4分,共计28分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题的0分;若正确答案包括两个选项,只选一个且正确的的2分,选两个且都正确的得满分,但只要选错一个,该小题就得0分。
不定项选择题:本题包括7小题,每小题4分,共计28分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题的0分;若正确答案包括两个选项,只选一个且正确的的2分,选两个且都正确的得满分,但只要选错一个,该小题就得0分。
6.下列说法正确的是:
A.三角架、泥三脚、研钵、瓷坩锅等仪器名称的书写均不规范
B.用硫粉覆盖地下撒有的汞;用热碱溶液洗去试管内壁的硫;用二氧化碳扑灭金属钠引起的失火;用湿w.w.^w.k.&s.5*高.考.资.源.网
的红色石蕊试纸检验氨气是否集满;以上操作均合理
C.洗涤沉淀时,向漏斗中加适量水并不断搅拌以增加洗涤效果
D.用精密pH试纸测得0.1mol/LNa2CO3溶液的pH=11.6
5.常温下,下列各组离子在指定溶液中一定能大量共存的是
A.能使甲基橙变黄的溶液中:Na+、K+、SO42-、AlO2-
B.加铝粉放出大量H2的溶液中:Na+、NH4+、SO42-、CO32-w.w.^w.k.&s.5*高.考.资.源.网
C.c(OH-) /c(H+)=10-12的溶液中:NH4+、Cu2+、NO3-、Cl-
D.0.1 mol•L-1NaHCO3溶液中:K+、Ba2+、OH-、Cl-
4. 设NA表示阿伏加德罗常数的值,下列说法正确的是
设NA表示阿伏加德罗常数的值,下列说法正确的是
A.NA个氧气分子与NA个氖气分子的质量比是4∶5
B.14g14C和12g12C所含的质子数相等
C.用铝箔包裹0.23gNa,在铝箔上刺些小孔,投入足量水中,放出氢气的体积大于112mL
D.常温常压下,11.2LCO2与8.5gNH3所含分子数相等,均为0.5NA
3.下列离子方程式书写正确的是
A.用氢氧化钠溶液除去铝表面的氧化膜:Al(OH)3+OH-=AlO2-+2H2O
 B.用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl- Mn2++Cl2↑+H2O
B.用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl- Mn2++Cl2↑+H2O
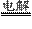 C.用惰性电极电解熔融氯化钠:2Cl-+2H2O Cl2↑+H2↑+2OH-
C.用惰性电极电解熔融氯化钠:2Cl-+2H2O Cl2↑+H2↑+2OH-
D.用稀氢氧化钠吸收氯气:2OH-+Cl2=Cl-+ClO-+H2O
2.下列叙述中不正确的是w.w.^w.k.&s.5*高.考.资.源.网
A.通过化合反应与置换反应均可以制得Fe3O4
B.通过化合反应与复分解反应均可以制得Fe(OH)3、NaHCO3
C.离子化合物的熔点不一定比共价化合物的熔点高
D.向含有1mol KAl(SO4)2的溶液中加入Ba(OH)2溶液至沉淀质量最大时,沉淀的总物质的量为3 mol
1.刚刚落幕的上海世博会,积极推行“低碳世博”。下列有关说法正确的是
A.大力发展绿色经济,告别含碳物质
B.尽量节约能源,推广使用新能源,减少二氧化碳的排放
C.尽量使用含12C的产品,减少使用含13C或14C的产品
D.逐步推广天然气,代替石油和煤的使用
25.(17分)短周期元素X、Y、Z的原子序数依次增大,X和Y同主族,Y和Z同周期,Y与Z能形成离子个数比为1︰1的离子化合物A,X与Z能形成原子个数比为1︰1的共价化合物B,它们之间能实现如图所示转化(部分产物已略去):

(1)Y在周期表的位置是___________________;Z2的电子式是____________________。
(2)反应①的化学方程式是__________________________________________________。
(3)D溶液呈碱性的原因是(用离子方程式表示)________________________________; D是很多漂白剂中含有的有效成分,这些产品不能与洁厕灵(含有有机酸和无机酸)一起使用,其原因就是在常温时能发生与反应②相似的反应。某校的学生在实验室利用反应②的原理来制备纯净、干燥的Z2,仪器装置如图所示(夹持固定装置的仪器已略去)。


I、写出反应②的离子方程式_____________________________。
II、上述实验装置不够完善,改进方法是 。
(4)Z2跟C在常温时发生反应③,在加热条件下发生的反应是

3Z2+6C 5A+YZO3+3H2O ,
3mol Z2与足量的C溶液反应,转移电子的物质的量n(e-)的取值范围是________________。
24.(12分)目前工业上有一种方法是用 生产燃料甲醇。一定条件下发生反应:
生产燃料甲醇。一定条件下发生反应:
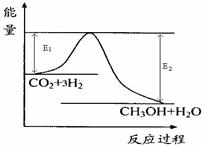
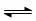

 ,右下图表示该反应进行过程中能量(单位为
,右下图表示该反应进行过程中能量(单位为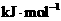 )的变化。
)的变化。
(1)关于该反应的下列说法中,正确的是 。
A.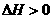 ,
,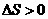 ; B.
; B.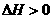 ,
,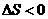 ;
;
C. ,
,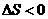 ; D.
; D. ,
,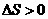 。
。
(2)该反应平衡常数 的表达式为
。
的表达式为
。
(3)温度降低,平衡常数 (填“增大”、“不变”或“减小”)。
(填“增大”、“不变”或“减小”)。
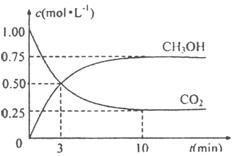 (4)为探究反应原理,现进行如下实验:在体积为
(4)为探究反应原理,现进行如下实验:在体积为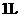 的密闭容器中,充入
的密闭容器中,充入
 和
和
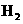 ,测得
,测得 和
和 的浓度随时间变化如下图所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率
的浓度随时间变化如下图所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率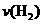 为:
为:
 。氢气的转化率
。
。氢气的转化率
。
(5)下列措施中能使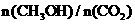 增大的有
。
增大的有
。
A.升高温度; B.加入催化剂; C.将 从体系中分离;
从体系中分离;
D.再充入
 和
和
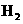 ; E.充入
; E.充入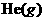 ,使体系总压强增大。
,使体系总压强增大。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com