
题目列表(包括答案和解析)
15.(12分)某校化学实验兴趣小组在“探究卤素单质的氧化性”的系列实验中发现:在足量的稀氯化亚铁溶液中加入l-2滴溴水,振荡后溶液呈黄色。
(1)提出问题:Fe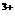 、Br2谁的氧化性更强?
、Br2谁的氧化性更强?
(2)猜想:
①甲同学认为氧化性:Fe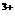 >Br2,故上述实验现象不是发生化学反应所致,则溶液里黄色是含
(填化学式,下同)所致。
>Br2,故上述实验现象不是发生化学反应所致,则溶液里黄色是含
(填化学式,下同)所致。
②乙同学认为氧化性:Fe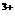 <Br2,故上述实验现象是发生化学反应所致,则溶液呈黄色是含
所致。
<Br2,故上述实验现象是发生化学反应所致,则溶液呈黄色是含
所致。
(3)设计实验并验证
丙同学为验证乙同学的观点。选用下列某些试剂设计两种方案进行实验,并通过观察实验现象,证明了乙同学的观点确实是正确的。
供选用的试剂:a、酚酞试液 b、四氯化碳 c、无水酒精 d、硫氰化钾溶液
请你在下列表格中写出丙同学选用的试剂及实验中观察到的现象。(试剂填序号)
|
|
选用试剂 |
实验现象 |
|
方案1 |
|
|
|
方案2 |
|
|
(4)结论氧化性:Fe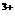 <Br2,在足量的稀氯化亚铁溶液中,加入1~2滴溴水,溶液呈黄色所发生的离子反应方程式为
。
<Br2,在足量的稀氯化亚铁溶液中,加入1~2滴溴水,溶液呈黄色所发生的离子反应方程式为
。
(5)实验后的思考
在2molFeBr2溶液中通入33.6L Cl2(标准状况),所发生的离子反应方程式为 。
14.
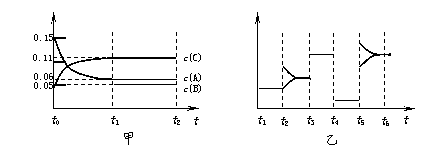 某密闭容器中加入0.3 mol A、0.1 mol C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图甲所示[t0-t1阶段 c(B)未画出]。图乙为t2后改变互不相同的某一条件反应速率随时间变化的关系图,t3-t4阶段使用了催化剂。下列说法错误的是 ( )
某密闭容器中加入0.3 mol A、0.1 mol C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图甲所示[t0-t1阶段 c(B)未画出]。图乙为t2后改变互不相同的某一条件反应速率随时间变化的关系图,t3-t4阶段使用了催化剂。下列说法错误的是 ( )
A.若 t1=15 s,生成物C在 t0-t1时间段的平均反应速率为 0.004mol·L-1·s-1
B.t4-t5阶段改变的条件为减小压强,t5-t6改变的条件是升高化学反应的温度
C.B的起始物质的量为0.02mol
D.该化学反应的表达式为:3A  B
+ 2C
B
+ 2C
第Ⅱ卷 非选择题(78分)
13.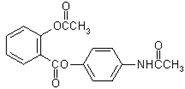 新型解热镇痛抗炎药扑炎痛的结构如图所示,下列关于扑炎痛的叙述正确的是 ( )
新型解热镇痛抗炎药扑炎痛的结构如图所示,下列关于扑炎痛的叙述正确的是 ( )
A.该物质的分子式为C17H16NO5
B.该物质的核磁共振氢谱上共有9个峰
C.该物质与浓溴水反应生成白色沉淀
D.该物质在酸性条件下水解最终可以得到3种物
质
12.下列溶液中有关微粒的物质的量浓度关系正确的是 ( )
A.常温下物质的量浓度相等的①(NH4)2CO3、②NH4Al(SO4)2、③(NH4)2Fe(SO4)2三种溶液中c (NH4+):③>①>②
B.0.1mol/LNa2S溶液:c(OH-)=c(H+)+c(HS-)+c(H2S)
C.常温下将NaHCO3和NaHSO3两溶液混合后,溶液显中性,则混合后的溶液中:c(Na+)=c (HSO3-)+ c (HCO3-)+ 2 c (CO32-)+2 c (SO32-)
D.相同条件下,pH=5的①NH4Cl溶液、②CH3COOH溶液、③稀盐酸溶液中由水电离出的c (H+):①>②>③
11.镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O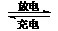 Cd(OH)2 + 2Ni(OH)2有关该电池的说法正确的 ( )
Cd(OH)2 + 2Ni(OH)2有关该电池的说法正确的 ( )
A.充电时阳极反应:Ni(OH)2-e-+ OH-= NiOOH+H2O
B.充电过程是化学能转化为电能的过程
C.放电时负极附近溶液的碱性不变
D.放电时电解质溶液中的OH-向正极移动
10.下列离子方程式书写正确的是 ( )
A.用铜作电极电解硫酸铜溶液: 2Cu2++2H2O通电4H++2Cu+O2↑
B.偏铝酸钠溶液中通入足量二氧化碳:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
C.过量的NaHSO4与Ba(OH)2溶液反应:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
D.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
9.某矿石由前20号元素中的4种组成,其化学式为WYZX4。X、Y、Z、W分布在三个周期,原子序数依次增大,W、Y为金属元素,X原子的最外层电子数是次外层电子数的3倍,W能与冷水剧烈反应,Y、Z原子的最外层电子数之和与X、W原子的最外层电子数之和相等,Y、Z位于同周期,Z单质是一种良好的半导体。下列说法正确的是( )
A.原子半径:W>Y>Z>X
B.气态氢化物的稳定性:X<Z
C.最高价氧化物对应水化物的碱性:Y<W
D.Y、Z的氧化物都有两性
8.下列化学实验事实及其解释都正确的是 ( )
A.氯气可以使湿润的有色布条褪色,是因为氯气具有漂白性
B.SO2溶于水,其水溶液能导电,说明SO2是电解质
C.滴有酚酞的Na2CO3溶液中滴加BaCl2溶液后红色变浅,说明BaCl2溶液有酸性
D.某溶液用盐酸酸化无明显现象,再滴加氯化钡溶液有白色沉淀产生,说明溶液中有SO42-
7.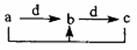 下表各组物质中,物质之间通过一步反应就能实现如图所示转化的是 ( )
下表各组物质中,物质之间通过一步反应就能实现如图所示转化的是 ( )
 物质 物质选项 |
a |
b |
c |
d |
|
A |
Al |
Al(OH)3 |
NaAlO2 |
NaOH |
|
B |
CH3CH2OH |
CH3CHO |
CH3COOH |
O2 |
|
C |
Na2CO3 |
NaHCO3 |
NaOH |
CO2 |
|
D |
Cl2 |
FeCl3 |
FeCl2 |
Fe |
6.三聚氰酸C3N3(OH)3可用于消除汽车尾气中的氮氧化物。当加热至一定温度时,它分解产生的HNCO(异氰酸,其结构是H-N=C=O)能和NO2反应:HNCO+NO2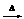 N2+CO2+H2O(未配平)。下列关于该反应的叙述正确的是 ( )
N2+CO2+H2O(未配平)。下列关于该反应的叙述正确的是 ( )
A.N2是还原产物,CO2是氧化产物
B.每生成1 molCO2需转移12 mol电子
C.反应中氧化剂和还原剂的物质的量之比为3:2
D.N元素既被氧化,也被还原
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com